近日,器械之家获悉,英特格拉生命科学(Integra LifeSciences)与苏州工业园区举行签约活动,其中国首个制造基地与测试中心正式落户苏州园区。

据了解,英特格拉生命科学创立于1989年,是全球领先的医疗科技公司,神经外科与再生医学并行的布局,奠定了其行业地位。其中,在神经外科领域,拥有最大的神经外科产品直销团队,且有14个神经外科医疗器械,在同产品中占据第一的市场份额。2022年度,Integra LifeSciences实现15.57亿美元营收,成为全球100强医疗器械企业之一。
在中国市场,2011年12月5日,英特格拉生命科学(Integra LifeSciences)在中国上海成立首个办事处,后成立了英特格拉生命科技(上海)有限公司。此次与苏州工业园区新签约项目,位于中新·星湾工业坊,是该公司在华设立的首个集生产、测试、服务等为一体的制造基地。
01
医械巨头,再生医学与神经外科并行
Integra LifeSciences的成立,可以说与人工皮肤技术密不可分。皮肤是人体最大的器官,当皮肤大面积受损时,传统的修复方法是进行自体或是异体植皮。但自体植皮往往来源有限,而异体植皮又会有排斥或者感染的风险。为了解决这个问题,麻省理工大学机械工程系的Dr. Yannas与麻省波士顿Shriners烧伤中心的Dr. Burke主任,共同开展了研究。

在1989年创立之时,Integra LifeSciences创始人Richard E. Caruso博士就将目标指向了开发可以促进患者自体组织,例如皮肤、神经、骨骼、肌腱等再生的医疗植入物。

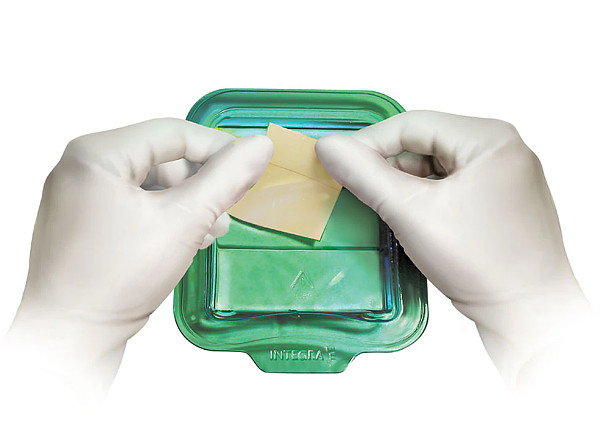
1996年, 基于Dr. Yannas与Dr. Burke的人工皮肤研究,Integra LifeSciences的产品Integra LifeSciences皮肤再生模板(IDRT)获得了FDA批准,这是Integra LifeSciences的第一个产品,也让 Integra LifeSciences成为了第一个将具有组织再生适应症产品推向市场的公司。

神经外科
之后,Integra LifeSciences开始对IDRT技术平台进行拓展,对新适应症以及新潜在科室进行探索。基于IDRT技术平台,Integra LifeSciences开发出了可以修复和促进自体脑膜再生的DuraGen人工硬脑膜,并于1999年获得FDA批准,成为它进入神经外科市场的敲门砖。

同年,Integra LifeSciences公司还上演了一出“小鱼吃大鱼”的戏码,以2500万美元收购了NeuroCare公司,进一步巩固了其在神经外科领域的市场地位。
在之后的几年里,该公司在神经外科开启了“买买买”模式,连续收购了10家小型神外领域创新公司,进一步扩大公司产品组合。2004正式成立神经外科事业部,稳步发展。
到了2017年,Integra LifeSciences在神经外科领域的发展再次迎来重要时刻,彼时该公司以超过10亿美元的金额,完成了对强生医疗器械公司Codman神经外科产品线的收购,进一步明确了在神经外科的领先优势。
再生医学
在推进神经外科领域产品发展的同时,Integra LifeSciences也没有放松对IDRT技术平台的产品拓展。对于皮肤修复产品,Integra LifeSciences从烧伤,拓展到急性、慢性创面修复,并且针对不同的适应症,一共推出了7款不同的产品。

另外,Integra LifeSciences还通过收购的方式,获得了脱细胞皮肤、人源羊膜技术平台、伤口修复产品开发平台,且针对伤口修复领域,不断通过并购和合作等方式,完善产业布局。此外,其还将产品线延伸至骨科领域。
两大部门
现今,Integra LifeSciences已发展成为再生组织技术和神经外科解决方案的全球领导者,拥有广泛的产品组合和解决方案,所生产的神经外科产品、手术器械和伤口护理产品遍及全球各地的医院重症监护室及手术室。主要通过两个部门运营,及科德曼专业外科(CSS)和组织技术(TT)。
其中CSS部门包括用于一系列专业的技术和仪器,如神经外科、神经重症监护和耳鼻喉科,拥有“Codman”、“DuraGen”、“DuraSeal”、“CUSA”、“Mayfield”和“Bactiseal”等品牌组合。

TT部门专注于三个领域,即复杂伤口手术、手术重建和周围神经修复。拥有“Integra Dermal Matrices”、“AmnioExcel”、“SurgiMend”、“MicroMatrix”和“NeuraGen”等品牌。
02
中国首个制造基地落户
历经三十多年发展,Integra LifeSciences业务足迹,已遍布全球多个国家/地区,并在加利福尼亚州、印第安纳州、马里兰州、马萨诸塞州、新泽西州、俄亥俄州、波多黎各、田纳西州、犹他州、加拿大、中国、法国、德国、爱尔兰和瑞士拥有庞大的生产和研究设施。2022年度,Integra LifeSciences实现15.57亿美元营收,成为全球100强医疗器械企业之一。
在中国上海成立首个办事处

其中在中国市场,该公司是较早进入我国发展的医疗器械企业之一。2011年12月5日,英特格拉生命科学(Integra LifeSciences)在中国上海成立首个办事处,后成立了英特格拉生命科技(上海)有限公司,之后上海公司逐渐成为了该公司的中国总部,中国市场也成为该公司的营收重要组成部分。
在华设立首个集生产、测试、服务等为一体的制造基地
近年来,英特格拉生命科学(Integra LifeSciences)也开始了在中国市场的本土化布局。此次与苏州工业园区新签约的项目,将成为英特格拉生命科学在华设立的首个集生产、测试、服务等为一体的制造基地,地点位于苏州工业园区中新·星湾工业坊。

对此,英特格拉集团总裁兼首席执行官Jan De Witte表示:“中国市场充满机遇,持续释放出强大的增长潜力。英特格拉期待与园区携手一道,将更多具有创新性的医疗科技解决方案引入中国,为提升患者生命质量而不断努力。”
DuraGen Plus正式在中国上市

另外,在今年第二季度,该公司的DuraGen产品组合的产品还获得了NMPA批准,即DuraGen Plus正式在中国上市。据悉,该产品是一种可吸收的硬膜缺损修复材料,由新西兰牛深屈肌(跟)腱提取的I型胶原蛋白制成。经环氧乙烷灭菌,一次性使用,适用于硬脑嵴膜的修补和替代。
CUSA Excel手柄的实现中国本地维修

此外,英特格拉生命科学(Integra LifeSciences)公司还在今年6月宣CUSA Excel手柄的实现中国本地维修。大大缩短维修周期,降低维修成本,有助于更快更好地解决客户需求。
03
全球第二大医械市场,巨头纷纷加码本土化
整体来看,伴随中国医疗器械供应能力的不断提升以及相关政策的支持,中国医疗器械行业也迎来快速发展,据《中国医疗器械行业发展现状与趋势》报告显示,2022年中国医疗器械市场规模预计达9582亿元(人民币),增速超过全球平均增速,已成为全球第二大市场。
在中国医疗器械市场,为提高医疗设备国产化水平,近年来国内从“鼓励国产”到“优先国产”相关的政策、措施密集出台。在此背景下,跨国医疗器械企业在中国市场的发展面临着挑战,多家跨国械企开始纷纷加大在华投资,推进产品生产和研发的国产化,部分企业的核心业务制造首次进驻中国。
除了投资建厂、增加产线外,跨国械企也在加大与本土企业的合作,通过收购、成立合资公司、达成战略合作等方式,增强竞争优势。其中包括美敦力、强生、西门子医疗、波士顿科学、GE医疗、飞利浦、直观外科、因美纳、奥林巴斯、宾得等跨国械企巨头加码布局,不断深入在中国的本土化布局。
因美纳首批本土化系列产品交付
2023年8月底,illumina因美纳宣布,其在中国本土生产制造基地的首批系列产品已成功完成交付。其中包括桌面式测序仪NextSeqTM 2000、超大规模量产型测序平台NovaSeqTM 6000Dx-CN以及5款CN NextSeqTM 550Dx临床应用测序试剂等在内的本土化生产组装产品即日起将正式面向中国客户全面接受预定。

据悉,该公司在中国首个生产制造基地位于上海临港浦江国际科技城,于2022年8月25日正式启用,并计划五年内逐步实现高端基因测序仪及耗材全面本土化生产。目前,该基地是因美纳全球第三个区域生产中心。
波士顿科学寻求在中国建立工厂

其中,波士顿科学已将部分生产制造服务委托给先瑞达。与此同时,还有媒体报道,该公司还将寻求在中国本土建造工厂。若工厂落地,也将成为这家医疗器械巨头司在中国首个落户的工厂。
GE医疗心血管超声全面国产
GE医疗也在不久前宣布心血管超声系列在无锡基地实现全面国产,给超声检查带来更多高质量的国产产品,帮助临床获取更好的心血管超声图像、更准确的心脏功能分析结果。

其中包括VividTM北极光旗舰心血管超声诊断系统、VividTM T系列、VividTM iq系列、VividTM极光系列在内的全线心血管超声产品实现了全面国产。
以此来看,生产制造和供应链本土化将会是跨国械企巨头本土战略的第一步,不仅体现了生产稳定性的要求,还能够进一步降低产品成本,未来几年,本土化依旧会是跨国医械巨头在中国市场发展的主要趋势之一。
作为全球领先的医疗器械巨头,英特格拉生命科学(Integra LifeSciences)集团此次与苏州工业园区签约落户,在中国的首个集生产、测试、服务等为一体的制造基地,将进一步加大其在中国市场销售、产品制造、研发的方面的本土化布局,以更好的耕植中国高速增长的医疗器械市场,对此器械之家将持续关注。
来源:器械之家
医疗器械ETF(159883)为目前A股规模最大的一只医疗器械行业ETF。该ETF追踪中证全指医疗器械指数,从概念上看不仅覆盖眼科、医美等消费医疗,还囊括了院内诊疗有关的高值耗材、IVD、医疗设备股,全面表征A股医疗器械行业发展,中长期受益于疫后医疗复苏及医疗新基建。
截至2023年9月12日,医疗器械ETF标的指数最新PE估值29.87倍,低于指数发布以来近81%的时间区间,板块布局性价比凸显。场内用户可通过医疗器械ETF(159883)进行投资,1手只需70元左右,免缴印花税。场外用户可通过联接基金(A份额013415,C份额013416)进行申购、定投。

风险提示:投资有风险,投资须谨慎。以上资料仅为服务信息,不作为个股推荐,不构成对投资人的任何实质性建议或承诺,也不作为任何法律文件。基金管理人承诺以诚实信用、勤勉尽责的原则管理和运用基金资产,但不保证本基金一定盈利,也不保证最低收益。本基金的过往业绩及其净值高低并不预示其未来业绩表现,基金管理人管理的其他基金的业绩并不构成对本基金业绩表现的保证。投资不同类型的基金将获得不同的收益预期,并承担不同程度的风险。通常基金的收益预期越高,风险越大。永赢医疗器械ETF属于中高风险(R4)产品,风险等级高于货币市场基金及债券型证券投资基金,适合经客户风险承受能力等级测评后结果为成长型(C4)及以上的投资者。基金风险等级与投资者风险承受能力等级对照表详见永赢基金官网。投资者通过代销机构提交交易申请时,应以代销机构的风险评级规则为准。本基金特有风险包括:标的指数回报与股票市场平均回报偏离的风险、标的指数波动的风险、基金投资组合回报与标的指数回报偏离的风险、跟踪误差控制未达约定目标的风险、基金份额二级市场交易价格折溢价的风险、IOPV计算错误的风险、退市风险、投资者申购失败的风险、投资者赎回失败的风险、基金份额赎回对价的变现风险、申购赎回清单标识设置风险、股指期货投资风险、资产支持证券投资风险、基金收益分配后基金份额净值低于面值的风险、标的指数变更的风险、指数编制机构停止服务的风险、成份股停牌的风险、第三方机构服务的风险、存托凭证投资风险、参与转融通证券出借业务的风险等。敬请投资者在做出投资决策之前,仔细阅读产品法律文件,充分认识本基金的风险收益特征和产品特性,充分考虑自身的风险承受能力,理性判断并谨慎做出投资决策。
#减肥药产业链持续活跃#
#医药工业、医疗装备大利好#
$医疗器械ETF(SZ159883)$$迈瑞医疗(SZ300760)$$新产业(SZ300832)$
本文作者可以追加内容哦 !

