随着ADC药物的兴起,多种偶联模式也随之出现。
近期,Seagen与Nurix达成降解抗体偶联药物(DAC)的开发合作,预付款6000万美元,里程碑付款共达34亿美元。
DAC相较于ADC来说,还处于新兴的,未经充分验证的初步开发阶段,本文将详细介绍DAC的概念、应用及最新进展。
目前PROTAC药物由三部分构成,包括目标蛋白结合物、泛素连接酶配体和连接子。但PROTAC通常面临细胞摄取差和生物利用度低的问题,在健康细胞和癌细胞之间缺乏区分可能会引发脱靶毒性,而DAC模式的出现为PROTAC药物提供了新的思路。

DAC结构设计
DAC和ADC结构比较相似,包括单抗、linker和有效载荷三部分。

最大区别在于有效载荷方面,ADC 通常用于输送小分子毒素,而 DAC 则用于输送 PROTAC 和分子胶。ADC 和 DAC 遵循相同的原则:选择性地转运payload,同时尽量减少脱靶效应。ADC中的有效载荷具有更强的细胞杀伤活性,因此,DAR通常为4-8或2-6,具体取决于偶联方法。
相比之下,DAC所需的DAR要高于ADC,因为TPD分子的药效通常弱于 ADC毒素。根据有效载荷的数量和连接子化学性质,会产生聚集、低效和药代动力学问题。最后,在制备TPD时,应考虑使用额外的官能团与连接子连接抗体。
DAC机制
DAC与ADC机制相似,DAC在血液循环中尽可能保持稳定,随后抗体特异性识别肿瘤相关抗原,DAC被内化至溶酶体,在蛋白水解和酸性环境中,DAC被降解,释放有效载荷(PROTAC),随后发挥作用。

研究进展
BRD4-Targeting DAC
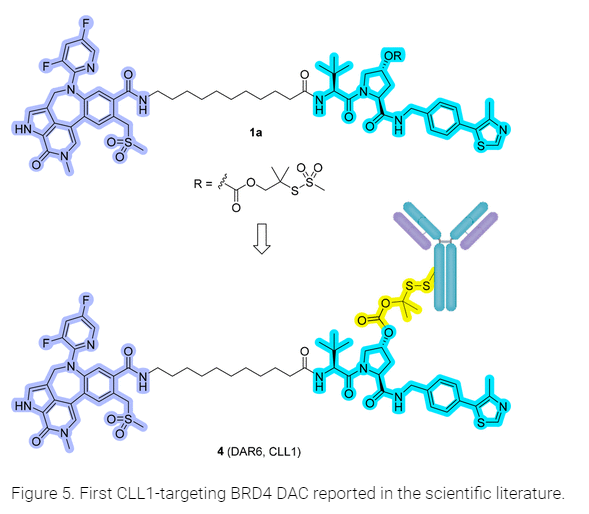
首次被研究报道的DAC是BRD4 DAC,由CLL1单抗和BRD4 PROTAC(GNE-987)构成,相关文章是由基因泰克和药明康德联合发表。
在研究中,GNE-987相较于MZ1和ARV-771具有更好的降解作用和AML癌细胞毒性,但由于体外和体内 DMPK 特性不佳,因此需要一种合适的递送方案。

由于CLL1在AML细胞表面高表达,之前对抗体半胱氨酸扫描的研究也发现,半胱氨酸残基的位置(LC-K149、HC-L174、HC-Y373)经过设计后,可表现出良好的体内稳定性。作者采用了“direct-disulfide”偶联策略,使用含有活化二硫化物的甲硫磺酰(MTS)基团与 CLL1 抗体上的六个半胱氨酸残基(DAR ≈ 6.0)偶联,没有出现明显的聚集问题。再利用降解剂原有的羟脯氨酸功能来连接linker,构建成DAC 4。
与靶向HER2的对照偶联物和降解剂GNE-987相比,DAC 4 对 HL-60 AML 和 EOL-1 AML 的疗效明显更强。表明DAC的构建可以克服degrader药代动力学的不良特性。DAC 4的药代动力学显示,其在体内的稳定性较高。
后续他们又开发了靶向STEAP1和靶向CLL1的BRD4 DAC,DAR为2,即DAC 5a和DAC 5b,但BRD4降解效果不佳。但通过提高DAR的方式构建的DAC 5c(DAR=6)显示,其具有更好的BRD4降解效果。

接下来,作者考虑将降解剂中的胺或苯胺作为偶联位点。

加入苯胺分子,同时使用强效降解剂,构建的DAC 9a单次静脉注射在PC3-S1小鼠模型中显示出剂量依赖性的肿瘤生长抑制作用

2020年,Maneiro等人报道了将ARV-711与HER2抗体(曲妥珠单抗)偶联的DAC 12,DAR为4。DAC 12 在PBS中很稳定,培养4小时后,其完好率为 98.8%,24 小时后可达 83.5%。DAC 12在 HER2+ 细胞中显示出对 BRD4 的选择性降解。


Er-Targeting DAC
Dragovich 等人还展示了两种不同的 Er 靶向降解剂13和15(图a,b)。13由连接酶配体 XIAP 和选择性雌激素受体调节剂他莫昔芬偶联,表现出对 Er 的强效降解作用。
在首次尝试中,他们利用他莫昔芬的游离羟基,通过缬氨酸-瓜氨酸-对氨基苄氧基连接子与 HER2 Ab偶联(14),成功证明了靶蛋白的降解。
之后构建了PROTAC 15 与 VHL 配体合成的 DAC。并利用 VHL 的羟基、通过碳酸基二硫连接子和焦磷酸二酯连接子合成了相应的DAC 16和 17。但这些偶联物仅表现出中等稳定性。

TGFR2, BRM-Targeting DAC
CRBN(cereblon)连接的降解剂 18 使用赖氨酸作为连接体连接到 HER2 上的不可裂解酰胺连接体上,构建了TGFR2 DAC(19),在 24 小时和 48 小时后显示出了所需的 TGFR2 靶向降解水平。
还有BRM降解剂(20),起初该降解剂是由 Arvinas 公司和基因泰克公司于 2019 年开发的。基因泰克公司进一步展示了基于降解剂20的DAC平台,该DAC使用二硫键连接子偶联与CD22细胞表面受体结合的单抗(21)。其异种移植数据显示,靶向 BRM 蛋白水平的降解具有高效性和抗原依赖性。

GSPT1-Targeting DAC
2022 年,Orum公司针对 GSPT1 蛋白开发的DAC(ORM-5029)进入了首个 I 期临床试验,其由高活性 GSPT1 降解剂 SMol006 通过 Val-Cit PABc 连接子与 pertuzumab 偶联,临床前数据中,与SMol006、Kadcyla和/或Enhertu治疗相比,ORM-5029治疗HER2表达细胞系的疗效增强了10-1000倍。
本文作者可以追加内容哦 !

