以下文章来源于医药地理 ,作者饮乐多
11月9日,和黄医药(中国)有限公司宣布,通过与合作伙伴日本武田制药共同努力,呋喹替尼已经被美国食品药品监督管理局批准,用于治疗经治转移性结直肠癌,这是首个在美国获批上市的小分子抗肿瘤原创新药。呋喹替尼是一种口服靶向疗法,用于治疗既往曾接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗、抗血管内皮生长因子(VEGF)治疗的患者以及抗表皮生长因子受体(EGFR)治疗的成人转移性结直肠癌患者。

据悉,结直肠癌是始于结肠或直肠的癌症,根据国际癌症研究机构(IARC)的数据,结直肠癌是全球第三大常见癌症。尽管早期结直肠癌能够通过手术切除,但转移性结直肠癌目前治疗结果不佳且治疗方案有限,仍然存在大量未被满足的医疗需求。虽然部分转移性结直肠癌患者或可受益于基于分子特征的个性化治疗策略,然而大部分患者未携带可作为治疗靶点的突变。
2023年1月23日,和黄医药宣布与武田制药达成独家许可协议,根据协议条款,武田制药将获得呋喹替尼在除中国大陆、香港及澳门地区以外的全球范围的针对所有适应症的开发及商业化独家许可,和记黄埔医药(上海)有限公司将可获得高达11.3亿美元的付款。
呋喹替尼的获批是基于两项大型III期临床试验的数据,包括:发表在《柳叶刀》的国际多中心临床试验FRESCO-2研究;以及于中国开展的FRESCO研究,其数据已发表于《美国医学会杂志》(JAMA)。上述研究探索了呋喹替尼联合最佳支持治疗对比安慰剂联合最佳支持治疗。FRESCO及FRESCO‑2研究均达到了其主要终点及关键次要终点,并在总共734名接受呋喹替尼治疗的患者中展现出了一致的获益。各项研究的安全性特征亦保持一致。
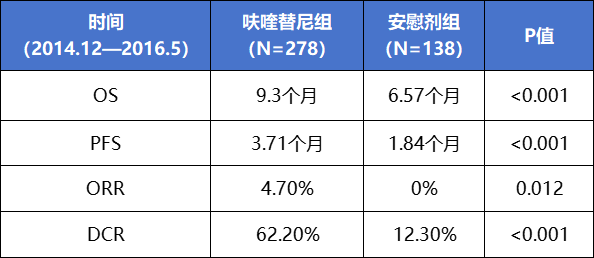
图2:FRESCO 研究试验结果
FRESCO研究共纳入共纳入416名受试者,278名被分配于呋喹替尼组,138名被分配于安慰剂组。在总生存期(OS)方面,呋喹替尼组达到了9.3个月,较之安慰剂组的6.57个月延长2.7个月,降低死亡风险35%;呋喹替尼组的无进展生存期(PFS)为3.71个月,较之安慰剂组的1.84个月延长1.9个月,降低疾病风险进展74%;呋喹替尼组的疾病控制率(DCR)为62.2%,也明显高于安慰剂组的12.3%。
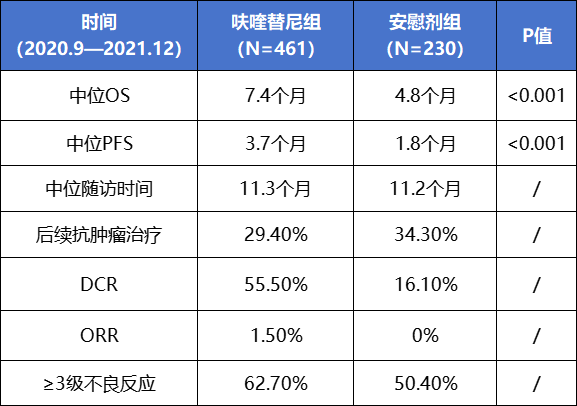
图3:FRESCO-2 研究试验结果
FRESCO-2研究则是一项在全球多地进行的随机、双盲、安慰剂对照的Ⅲ期临床试验,共纳入691名受试者,461名被分配于呋喹替尼组,230名被分配于安慰剂组。在中位生存期方面,呋喹替尼组患者达到了7.4个月,较之安慰剂组的4.8个月延长了2.6个月,降低死亡风险34%;呋喹替尼组患者的中位无进展生存期为3.7个月,较之安慰剂组的1.8个月延长了一倍,达到了1.9个月,降低了疾病进展风险68%;呋喹替尼组患者的疾病控制率为56%,也明显高于对照组的16%;在安全性风险,呋喹替尼组与安慰剂组相差不多。
据悉,呋喹替尼是中国首个从药物发现到临床开发均在本土自主完成的肿瘤药物,最新数据显示:其在我国晚期结直肠癌患者中的使用率,从2018年的2%升至2023年第二季度的47%,延长了约6万名患者的生存。
近日,据武田制药官网,武田/和黄医药合作的呋喹替尼定价出炉:美国一盒5mg*21粒的呋喹替尼定价为25200美元/盒,按照换算为人民币约为18万元左右。而呋喹替尼在国内的医保价格,2023年的数据,一盒一毫克21粒的呋喹替尼价格大约为1885.38元,而一盒五毫克7粒的呋喹替尼价格大约为2513.7元,同等数量的国内价格远低于美国价格。
2023年上半年,和黄医药实现销售收入5.33亿美金,同比增长164%,净利润1.69亿美金,实现扭亏为盈,营收大幅增长主要系上半年武田制药支付的首付款中确认2.59亿美元的收入。
据和黄医药方面介绍,2007年,上海浦东张江的一个实验室首次合成了最初有关呋喹替尼的一个小分子结构;2016年,FDA批准呋喹替尼可在国际开展临床试验,开创中国原创新药进入国际肠癌市场开展临床试验的第一记录;2018年,呋喹替尼获批在中国上市;该药2020年正式被纳入医保,获批适应症为三线及以上转移性结直肠癌,公司与礼来在国内达成合作;2023年1月,和黄医药与武田制药签订具里程碑意义的呋喹替尼在中国以外地区的许可协议。此次呋喹替尼在美获批触发了来自武田3500万美元的第一笔里程碑付款,以及基于净销售额特许权使用费,这刷新了中国小分子新药出海首付金额记录,提速中国医药创新的全球化之路。2023年上半年呋喹替尼终端市场销售为5630万美元,同比增长12%。
呋喹替尼作为在美国唯一获批用于治疗经治转移性结直肠癌的针对全部三种VEGF受体激酶的高选择性抑制剂,具有广阔的前景。呋喹替尼此次批准通过优先审评程序,较原定的审评日期提早了超过20天,预计呋喹替尼将于2024年相继在欧洲、日本上市,让我们拭目以待!
近期活动


本文作者可以追加内容哦 !

