【前列腺癌临床招募】丹瑞生物Sipuleucel-T注射液Ⅲ期临床进行时
尊敬的患者朋友:
您好!
国内mCRPC多以药物治疗为主,尚需更有效的、基于不同作用机制(如免疫)的治疗手段。目前丹瑞生物正在开展一项已经获得国家药品监督管理局(药物临床试验受理号:CXSL200009、通知书号:2020LP00163)和组长单位复旦大学附属肿瘤医院伦理委员会的批准,“Sipuleucel-T对比醋酸阿比特龙或恩杂鲁胺治疗无症状或轻微症状的转移性去势抵抗性前列腺癌(mCRPC)患者的有效性和安全性的多中心、随机对照临床试验”的III期临床研究。本临床研究已在全国多家医院开展,目前正在进行受试者招募。
关于Sipuleucel-T注射液Ⅲ期临床信息,请查看:
1、里程碑!前列腺癌细胞免疫治疗药物Sipuleucel-T中国Ⅲ期临床首例受试者回输成功
您若符合如下标准且有意愿,将有机会参与此次招募计划
前列腺腺癌,除外神经内分泌或小细胞特征;
疾病进展至CRPC阶段
1)酮水平去势:≤1.73 nmol/L(50 ng/dL)
2)a. PSA 进展:至少 2 次测量间隔时间≥1 周的PSA 水平升高,PSA≥ 1 ng/ml; 或 b.由实体瘤反应评价标准(RECIST)v1.1 定义的软组织病灶进展; 或 c. 骨病灶进展定义为骨扫描时发现至少两个新增病灶,针对模棱两可的结果采用另一种成像技术进行确认
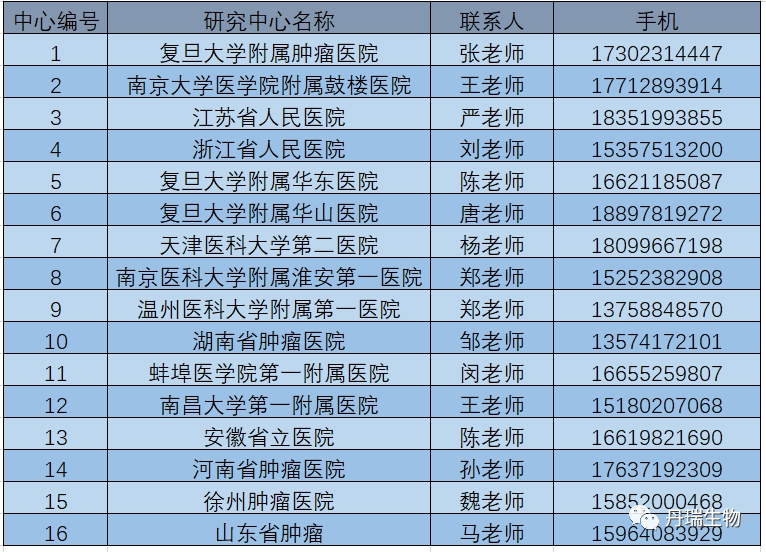
有参加研究意向的患者,可按下表就近到各个医院现场咨询或电话咨询或扫码报名。医生将会根据您的实际情况及研究方案要求来最终确定您是否可以参加本研究。

扫码报名
南京新百旗下的上海丹瑞生物医药科技有限公司(简称:丹瑞生物)是一家临床阶段的创新型生物医药公司,成立于2018年4月。丹瑞生物自成立之初便一直推动普列威(Provenge)在中国的上市,并致力于将丹瑞美国前沿的免疫细胞治疗技术转移到中国。在完成全套技术转移的过程中建立了一套覆盖细胞免疫产品全生命周期的管理体系,涵盖标准建立、细胞采集、生产工艺、质量控制、商业运营、信息管理、人才培养等。丹瑞生物将继续全力加速普列威的临床试验进程,力争早日服务中国晚期前列腺癌患者。
郑重声明:用户在财富号/股吧/博客社区发表的所有信息(包括但不限于文字、视频、音频、数据及图表)仅代表个人观点,与本网站立场无关,不对您构成任何投资建议,据此操作风险自担。请勿相信代客理财、免费荐股和炒股培训等宣传内容,远离非法证券活动。请勿添加发言用户的手机号码、公众号、微博、微信及QQ等信息,谨防上当受骗!

郑重声明:东方财富网发布此信息的目的在于传播更多信息,与本站立场无关。东方财富网不保证该信息(包括但不限于文字、视频、音频、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关信息并未经过本网站证实,不对您构成任何投资建议,据此操作,风险自担。











