来源:器械之家,未经授权不得转载,且24小时后方可转载。
3月5日,美国食品药品监督管理局(FDA)发布公告称,史密斯医疗(Smiths Medical)因与早期软件版本相关的问题正在美国地区召回Medfusion 3500型注射泵,共计85,961台。
此次召回是在公司收到FDA的警告信后发起的,值得注意的是本次召回是一种纠正,而不是产品删除。FDA将此次产品纠正归类为一类事件,这表明存在严重受伤或死亡的风险。
根据信件内容,Medfusion 3500注射泵的安全风险主要源于旧软件版本(v.6之前)。问题主要涉及到高优先级警报、输液重新启动时的参数错误、屏幕锁问题、输送中断、推进剂/装载剂信息的显示错误、未达到最低推荐速率、电机速率错误、上次设置错误记忆、配置损坏等方面。
目前史密斯医疗已经解决了一起与报告相关的受伤问题,并通过更新软件来解决此类问题。此外,公司在去年12月已经致信用户,建议他们检查是否安装了最新版本的软件,以确保设备的安全性和稳定性。
根据12月的信件来看,一共需要召回的是两个型号的输液泵。不过此前2月另一款型号的输液泵Medfusion 4000已经发布了召回通知。据器械之家统计,这两款产品合计在美召回数量达到13.67万台。
01
全美召回超13万台
据了解,Medfusion 3500注射泵是史密斯医疗推出的一款用于精确控制输液速率的注射泵,其输送速率可低至每小时0.01毫升,最大可达每小时1130毫升,输注精度为≤2%。适用于输注血液、脂肪、药物、抗生素和治疗性液体等液体,可用于多种输注途径,包括动脉、硬膜外、静脉、嵴髓内、皮下和肠道。
轻便是Medfusion 3500注射泵的一大特色,其重量仅有3.8磅(1.7千克)。高度为5.1英寸(13厘米),宽度为10.5英寸(27厘米),深度为5.5英寸(14厘米)。内部装有IPX3防潮等级和Type CF电击保护,同时采用了镍氢充电电池,在使用60毫升注射器、每小时连续输液速率为5毫升的情况下,可以运行至少6小时。
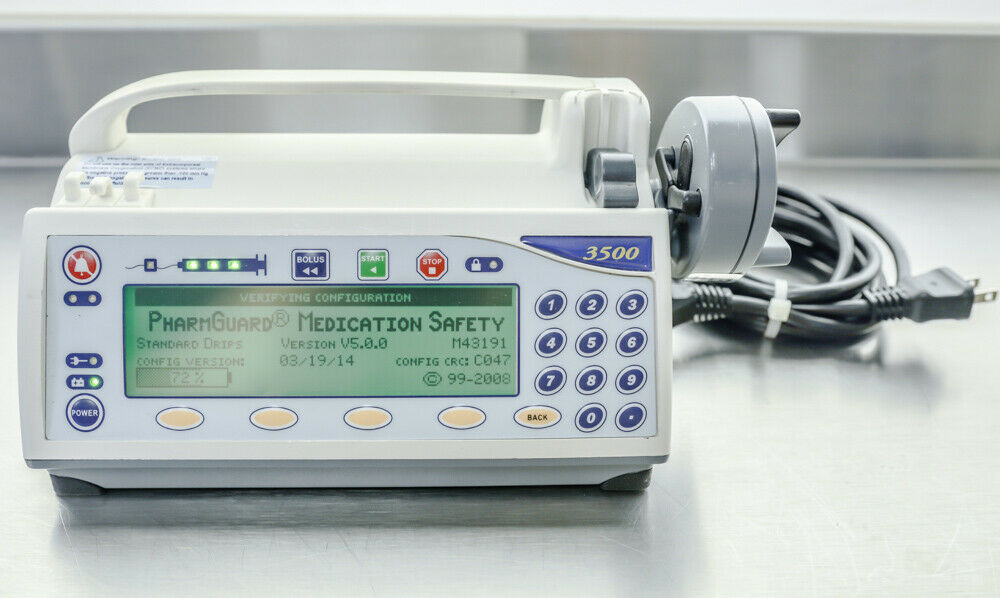
Medfusion 3500
软件方面,该注射泵采用了PharmGuard药物安全软件,可减少编程错误,确保治疗的安全性。同时具有FlowSentry的快速阻塞检测技术。FlowSentry是一系列与压力相关的安全功能,可及时检测管路阻塞,并发出警报,以确保输液过程的顺利进行。
值得一提的是,Medfusion 3500系统具有许多不同的功能。例如,具有记忆上次设置以便快速和简便设置的功能。使用此功能时,系统设置中的任何可选容量限制、KVO、推进剂剂量或装载剂剂量设置都将保留。临床医生可以重复使用相同的输送设置,向患者重复相同剂量的药物或液体。
此外,用户甚至可以将此设备设定为仅允许特定尺寸和型号的注射器,具体取决于指定的药物程序。这有助于减少注射错误并提高用户友好性。
Medfusion 4000召回
除了这次Medfusion 3500的召回,史密斯医疗还在今年2月14日时召回了另一款注射泵产品——Medfusion 4000。
与此次召回原因相似,Medfusion 4000同样是因为早期软件版本(v.6之前)存在一些问题,这些问题涉及到注射泵的多个方面,包括高优先级警报、输液重新启动时的参数错误、屏幕锁问题、输送中断、未达到最低推荐速率等方面。

Medfusion 4000
2023年12月19日,史密斯医疗发出过一封紧急医疗器械更正信。该信函要求客户:找到所有受影响的泵,并确保这些设备的所有用户立即了解此通知以及建议的缓解措施——确认所有泵均安装了最新的Medfusion软件。
此前召回11万台
而在2022年7月,Medfusion系列的这两款产品同样经历过一次大规模召回。根据当时FDA官方文书,该系统软件故障会影响不同的序列号和软件版本,这些故障可能会因输液不足或过度输液而对患者造成严重伤害或死亡,或延迟向患者提供关键药物。 并表示共有7起重伤和1起死亡报告与这些问题有关。
随后FDA发布一级召回通知,列出Medfusion 3500和4000输液泵在美国地区的召回设备共有11.8万台。
02
近170亿收购后,平凡召回
这次召回事件是史密斯医疗公司被ICU Medical以23.5亿美元(约合人民币169亿元)收购后所面临的一系列监管问题之一。
资料显示,史密斯医疗源自英国工业巨头史密斯集团,是一家全球领先的医疗设备和器材供应商,专注于生产和销售医疗器械和产品,如注射泵、氧气设备和外科产品等。2021年时,史密斯医疗在注射泵领域全球排名第一。

2018年11月,史密斯集团对外宣布将剥离医疗业务。官方给出的理由是2018年医疗部门拖累了集团的整体表现,并且与史密斯集团的工业业务相距甚远,不能形成矩阵效应。
从2018年史密斯集团的整体收入上看,史密斯医疗占比28%,排名第一;但营收同比下降7%,排名为第四;利润率为17.6%,排名第三。因新产品发布延迟,在新法规下一些产品失去认证资格以及在美国失去两份合同,史密斯医疗的2018年营收情况受到很大打击。
2022年1月6日,美国注射泵龙头ICU Medical宣布以24亿美元的价格将Smiths Medical纳入旗下,完成了“美国第一”对“全球第一”的蛇吞象式收购。并且ICU Medical表示,将两家公司的现有业务合并后,其将成为一家全球领先的输液治疗公司。
当然事实也确实如此,从ICU Medical的财报数据来看,我们可以发现在收购史密斯医疗后,公司业绩呈爆发式增长。
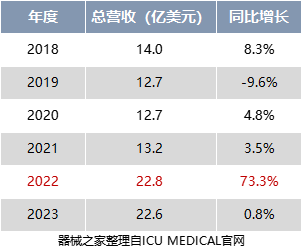
财报数据显示,2018年-2021年ICU Medical的平均营收在13亿美元每年,但自2022年收购后,增幅达到了73%,完成营收22.8亿美元。其中,史密斯医疗的产品贡献了9.5亿美元。
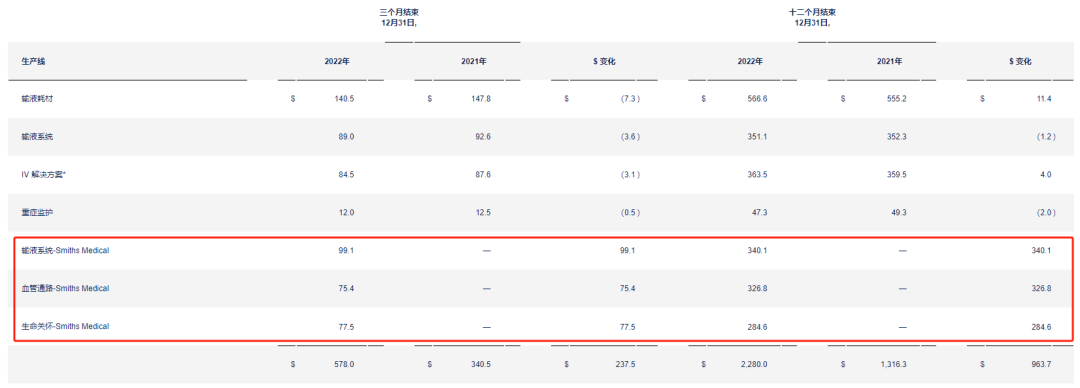
03
输液泵“扎堆召回”
近年来,输液泵召回事件并非个别案例。
据报道,在过去的五年里,美国食品药品监督管理局(FDA)收到了超过5万份与输液泵相关的医疗器械不良事件报告。其中不乏BD、费森尤斯等巨头企业。
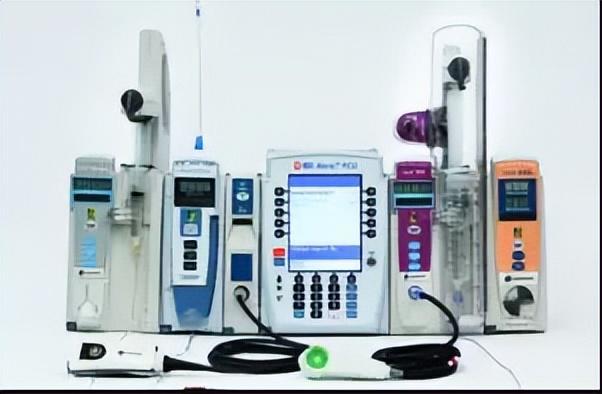
BD医疗77.4万台输液泵召回
据悉,2020 年初,BD公司曾发布了迄今为止范围最广泛的 Alaris 泵的一级召回,召回数量达77.4万台 Alaris 输液泵。召回原因涉及与嵌入式软件相关的少数系统、软件和使用相关错误。这些错误可能会导致输液延迟和中断,或者液体输送不足或过度输送。彼时,这些问题导致了至少 55 人受伤和 1 人死亡。
费森尤斯输超1500台液泵召回
2023年4月19日,美国FDA官网发布公告,决定将费森尤斯卡比此前一个月召回的1546台Ivenix输液系统定为最严重的一级召回。官方给出的召回原因是泄漏可能导致电气系统故障,治疗中断,患者可能受到严重伤害或死亡。
--
需要强调的是,医疗器械主动召回并不意味着公司陷入严重的医疗事故风波。但频繁的召回难免引发市场对企业品牌在生产研发、甚至管理之上的质疑,进而对整体的品牌形象造成影响。
那么,作为曾经全球输液泵龙头的史密斯医疗,面对频繁召回是否会做出改变?ICU Medical的业务及声誉会不会受到这一系列“召回风波”的影响?器械之家将持续关注。
本文作者可以追加内容哦 !

