歌礼制药(1762.HK)全资子公司甘莱制药正在全国开展一项“评价ASC41片在成人非酒精性脂肪性肝炎(NASH)受试者中的安全性和有效性的随机、双盲、多中心、安慰剂对照的II期研究”。
这项研究已得到国家药品监督管理总局的批准并通过中心伦理,正在全国招募。
试验药物简介
ASC41片是一种肝脏靶向性前体药物,其活性代谢产物可选择性激活甲状腺激素受体(THR),与FDA首款获批NASH药物同靶点。
本研究期中分析数据显示:
--患者服用ASC41片12周后,肝脏脂肪含量较基线的相对降幅平均值高达68.2%
--第12周时,高达93.3%的患者肝脏脂肪含量较基线相对降低30%及以上
--第12周时,经安慰剂校正后的丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)较基线相对降幅平均值分别高达37.8%和41.5%
--第12周时,经安慰剂校正后的低密度脂蛋白胆固醇(LDL-C)、总胆固醇(TC)和甘油三酯(TG)较基线相对降幅平均值分别高达27.7%、23.4%和46.5%
--服用ASC41片患者与服用安慰剂患者中的不良事件(AE)相似
主要入选标准:
1)年龄为18-80周岁(包括18周岁和80周岁)。
2)筛选期间或首次给药前6个月内进行且由中心阅片的放射科医生判读的MRI-PDFF筛选结果显示脂肪变≥7.5%。
3)首次给药前6个月内进行且由中心实验室判读的肝脏活检组织学确认的,NASH 纤维化1、2或3期,并伴有NAS≥4,且各组成部分(脂肪变、小叶炎症和肝细胞气球样变)的评分至少为1。(F1已入组完成)
4)研究入组前2周至6个月ALT和AST值与筛选期ALT和AST水平必须一致。
主要排除标准:
1)当前或既往患有肝硬化,或者有失代偿性肝病的证据(即腹水、静脉曲张出血、肝性脑病、肝肾综合征)或肝细胞癌。
2)未控制的2型糖尿病(T2DM)。
3)筛选期异常实验室检查值,定义如下:
筛选时血清AST>5倍正常上限(ULN)。
筛选时血清ALT>5倍ULN。
碱性磷酸酶≥ 2倍ULN(除非ALP不是肝源性的)。
血清肌酐升高≥ 2.0 mg/dL。
国际标准化比值(I NR)>1.4倍ULN。
总胆红素>1.2倍ULN。(Gilbert综合征患者有资格参加本研究。)
血小板计数<正常下限(LLN)。
4)筛选期存在甲状腺疾病包括甲状腺功能亢进症和甲状腺功能减退症
研究中心信息
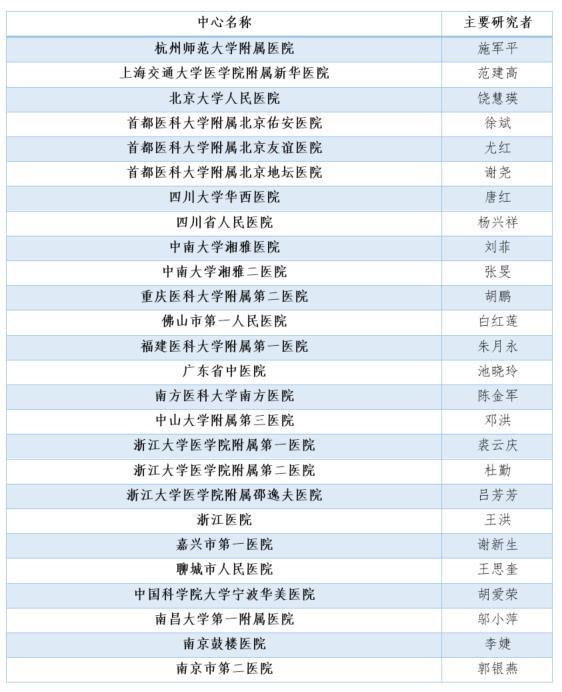
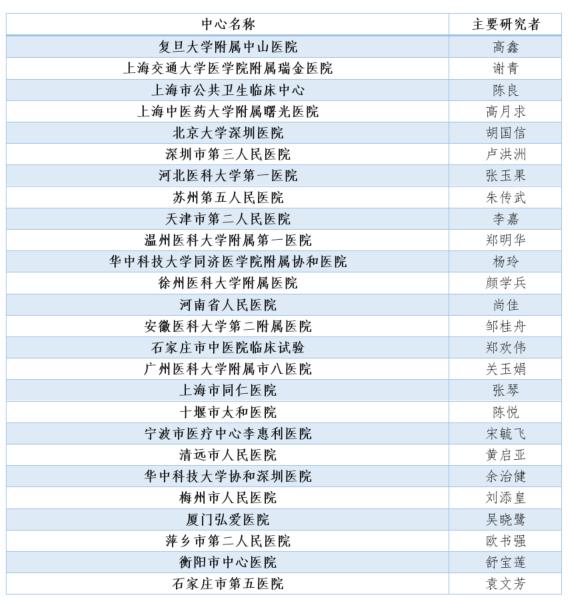
本文作者可以追加内容哦 !

