继降糖、减重之后,又一几乎“无药可救”的代谢病迎来首款新药获批。
近年来,患脂肪肝这一“富贵病”的人群愈发广泛,四个成年人中可能就有一个受脂肪肝困扰。其中,发展成为非酒精性脂肪肝炎(NASH,后更名为代谢相关脂肪肝炎,缩写为MASH)的患者,时常伴随着肝纤维化,若得不到有效干预,可能发展成为肝硬化、肝脏肿瘤等严重疾病。
然而,如此常见的疾病,既往FDA却未批准一款药物用于非酒精性脂肪肝。
病人多、药少,MASH这一新药开发的蓝海,吸引了礼来$礼来(NYSE|LLY)$、诺和诺德$诺和诺德(NYSE|NVO)$、阿斯利康$阿斯利康(US ADR)(NASDAQ|AZN)$、默沙东等跨国巨头入局,但这个“研发黑洞”既往已有不下20条管线研发失败。直到3月15日凌晨(北京时间),FDA批准了生物医药公司Madrigal开发的口服小分子药物Resmetirom,成为全球首款可用于治疗有肝纤维化的成人MASH患者。
Resmetirom的获批在业内引发热烈反响:“划时代”、“里程碑”、“相当于20年前的拉米夫定(畅销药)治疗慢性乙肝” 、“意义堪比PD-1”等评价不绝于耳。这款first-in-class药物三期临床数据显示:超过80%的患者达到肝纤维化逆转或无进展,有望成为MASH的基础标准疗法。
据介绍,Madrigal为该创新药的定价为每年47400美元(折合人民币约33.7万元),目前约有31.5万名MASH患者且出现二三期肝纤维化的美国患者正在接受治疗。根据弗若斯特沙利文报告,2020年全球和中国的MASH患者人数分别为3.5亿人、3870万人,存在巨大的临床缺口。
如今,司美格鲁肽、替尔泊肽等减肥神药,被认为是治疗NASH的潜力选手;特别是二期临床的表现优异,强化着“GLP-1颠覆MASH市场”的预期。不过司美格鲁肽治疗NASH的三期临床试验预计2029年完成,礼来、BI上月刚刚公布二期临床数据,距离获批仍需几年时间。因此,抓住一枝独秀的窗口期,快速实现商业转化,正是Madrigal的当务之急。
Madrigal也早早做好了商业化的准备。早在2023年9月Madrigal向FDA提交新药上市申请时,便邀请了履历丰富、曾在赛诺菲领导百亿美元级单抗药品商业化的Bill Sibold作为新任CEO,并在一年时间内自建了商业化团队,Resmetirom在4月即将开始销售。
根据Evaluate 预计,到 2028 年Madrigal 的药物销售额将达到21亿美元,成就新的十亿美元“重磅炸弹”。
攻破NSHA研发黑洞,R药潜力早现
代谢相关性脂肪肝炎,顾名思义,这类脂肪肝病与高血压、血脂异常、2型糖尿病、胰岛素抵抗等代谢疾病息息相关,受上次适应症困扰的患者需警惕发展成MASH的可能性。此前英国权威期刊GUT荟萃分析指出:中国2型糖尿病患者中,MASH的发病率达到52.56%。
这样一种困扰人类的常见病,为什么新药开发如此困难,以致于研发40年才有一款新药获FDA批准?
首先,因为MASH是一种致病机制复杂的慢性代谢病,受多种风险因素、细胞类型和组织器官平行作用而致病,肝部又是代谢中枢,靶向其中一个通路或靶点或不足以产生疗效。同时,实验动物模型也难以完全模拟人类NASH病理特点,给新药研发增加了难度。
再者,FDA对脂肪肝炎缓解的临床终点认定非常严格,三期临床需要通过肝穿刺活组织进行病理学评价,以判断是否MASH缓解、或肝纤维化改善;“肝穿刺”(存在出血风险)也增加了临床试验受试者的招募难度。
新药开发难,老药新用又何如?事实上,大家耳熟能详、用于代谢疾病的药物,如二甲双胍、熊去氧胆酸、他汀类药物和水飞蓟素在MASH患者中都未发现有显著的肝组织学获益,因此不被推荐用于治疗MASH。
本次获FDA批准的Resmetirom也经历了漫长的开发过程,自2002年前后就启动临床前的靶点和分子研究,到2011年开始临床一期试验,再到2022年公布临床三期试验的积极效果,仅临床试验就历时11年之久。
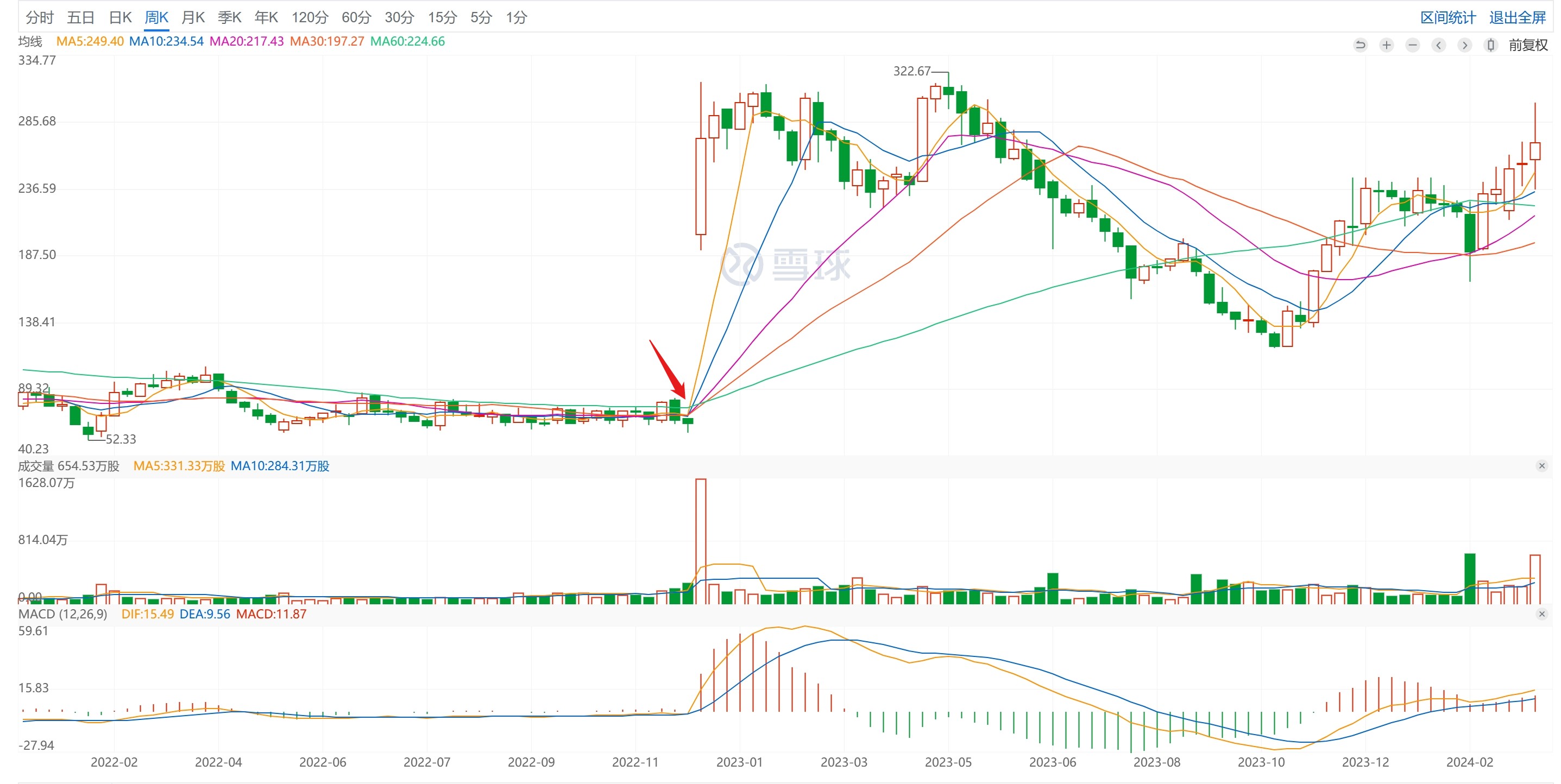
不过,市场也给予了成功坚守者以回报,2022年12月Resmetirom临床数据公布次日,Madrigal股价暴涨268%,市值超过40亿美元;利好消息甚至拉动了国内同靶点开发药企歌礼药业股价也暴涨50%。而R药获批后,3月16日收盘这一biotech市值已达到53.8亿美元。
Resmetirom针对MASH的三期临床,招募了1000多例患者。数据表明:50%的患者达到NASH缓解或纤维化改善,超过70%的患者肝脏脂肪含量下降超过30%,超过80%的患者达到纤维化逆转或者无进展。
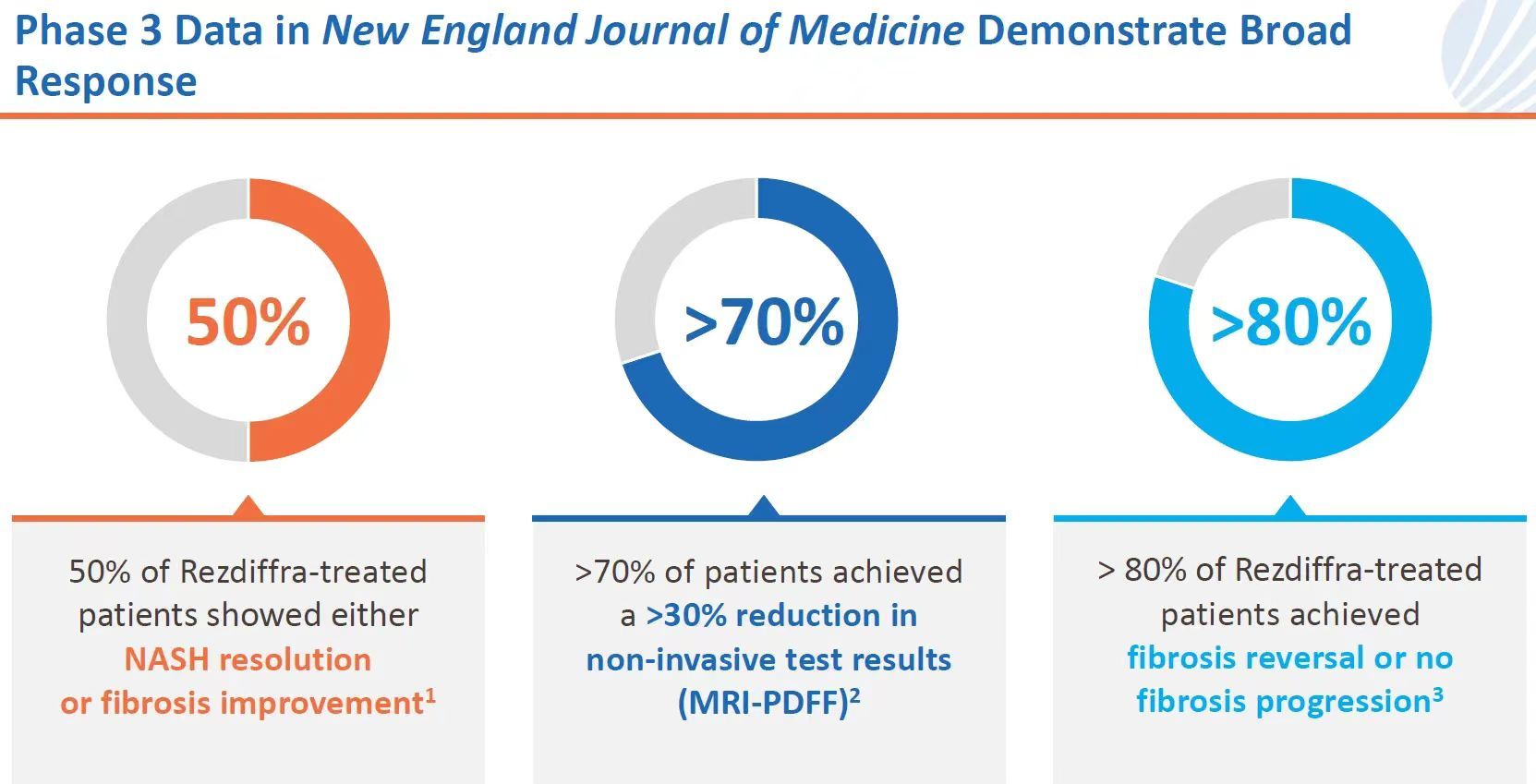
特别在“肝纤维化改善且MASH不恶化”这一主要终点的数据实现上,Resmetirom的表现也超出预期。毕竟,在国内有一些保肝药物能够治疗肝脏炎症,但并不能改善肝脏脂肪的沉积和肝纤维化。可以说,这款“fisrt-in-class”药物的临床和商业潜力,早在两年前数据公布时,已被业内广泛关注。
多方分析人士对这款MASH靶向特效药的销售额给出乐观预判:Evercore ISI分析师估计,到2030年,Rezdiffra的全球销售额可能达到约26亿美元,峰值时可能达到55亿美元。与前述Evaluate的“2028年销售额达21亿美元”的预估数据也比较接近。
司美格鲁肽等“踢馆者”,进展如何
MASH这一百亿美元蓝海,尽管既往少有新药选手成功“撞线”,但前仆后继者不计其数。据方正证券统计,全球有超过500个MASH新药项目在研,其中处于临床试验开发阶段的药物管线超过200个。
其中,因减肥疗效而出圈的“代谢神药”司美格鲁肽、替尔泊肽等GLP-1药物,被认为是有可能改写MASH市场的“黑马”。
如前所述,MASH的发病进展与2型糖尿病、肥胖等息息相关,在以往没有特效药的情况下,通过饮食和运动锻炼管理体重,是干预脂肪性肝炎的基石。研究表明,减重10%以上者脂肪性肝炎改善率高达90%,这也意味着,随着司美格鲁肽等药物的推广,肥胖超重人群的数量可能会得到有效控制,MASH患病人群增长有可能也被抑制。
除此之外,司美格鲁肽、替尔泊肽及默沙东的在研药物MK-6024等GLP-1类药物的临床试验也正在开发过程中。
其中,已揽金百亿美元的司美格鲁肽,针对MASH的临床试验已经进展到三期。此前已揭盲的二期临床数据显示:接受高剂量0.4mg治疗的患者,58.9%患者的MASH消除且肝纤维化没有进展,远高于安慰剂组。不过,在肝纤维化分期的改善方面,司美格鲁肽与安慰剂组差异不显著。据了解,其三期临床试验正在开展中,预计2029年完成。
另一款GLP-1赛道的重量级选手,来自礼来的替尔泊肽,在MASH治疗的临床实验中,展现出更强效果:接受高剂量替尔泊肽治疗的患者中,73.9%达到MASH消除且肝纤维化没有进展;且超过80%的患者的肝脏脂肪变性减少率达到70%或更高。
替尔泊肽MASH试验数据公布后,礼来股价上涨,同时其它从事MASH药物研发的企业股价应声下跌。
除了GLP-1的单一药物治疗,该领域另一实力派选手Akero Therapeutics研究了在研药物EFX(Efruxifermin)与GLP-1药物的联用,发现在减缓脂肪肝变性、降低肝损伤或肝纤维化、及更好的血糖控制上,联用效果优于司美格鲁肽单药。随着相关药物的临床开发及审评上市,多药联用治疗MASH或也是未来重要方向。
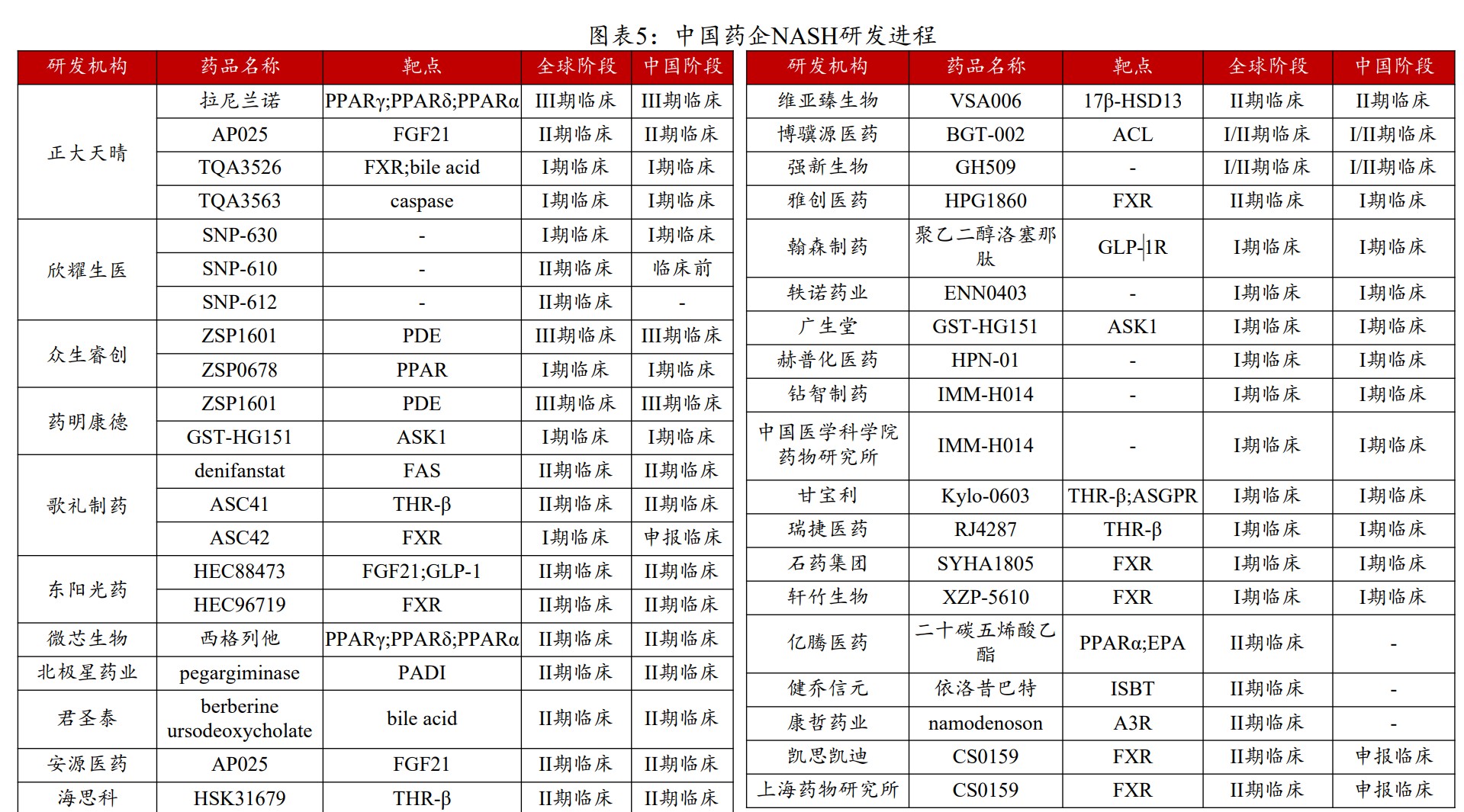
现阶段,国内布局MASH新药研发的企业有30多家,其中进入临床阶段的管线超过20条,其中,众生瑞创和药明康德联合开发的新药、正大天晴的在研管线已经推进到临床三期;东阳光药、歌礼制药处于临床二期。另外,派格生物、先为达生物等GLP-1研发企业也已涉足MASH赛道。
本文作者可以追加内容哦 !

