康宁杰瑞KN046治疗晚期鳞状sqNSCLC的临床III期临床,OS暂未达到统计学显著性差异未能成功揭盲,导致公司股价下挫超60%。KN046治疗NSCLC的III期临床一波三折,数据问题仍旧悬而未决,在KN046的期待落空后,市场对其兴趣减淡。随着ADC药物的热潮席卷全球,HER2双表位ADCKN003得到了更多关注,那么康宁杰瑞能够凭KN003打一场漂亮的翻身仗呢?
1.KN003设计与优化思路
2. 双表位的设计或能使更多的患者收益
3. HER2 ADC在增效减毒思路下寻找更完美的平衡
4. DXd专利问题并非核心KN003需要更多的临床证据
1KN003设计与优化思路
抗体部分的设计。

KN046抗体引入了KiH突变技术和自主研发电荷网络的异源二聚体制备技术,可以有效的防止Knob重链配对,并最大程度减少同源二聚体的形成,提高双抗体产率。
偶联方式。
Payload。根据康宁杰瑞专利中披露的双抗ADC示意图,payload基本沿用了DS8201基础结构,即GGFG linker+DXd毒素,linker部分的PEG4链提升ADC亲水性。

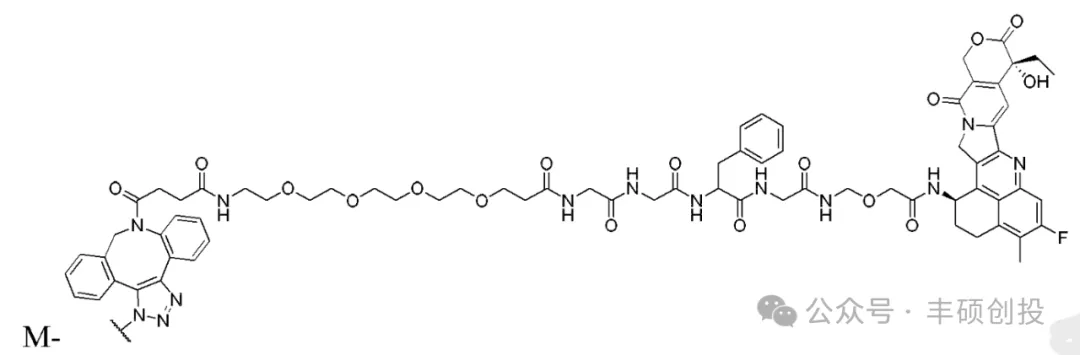
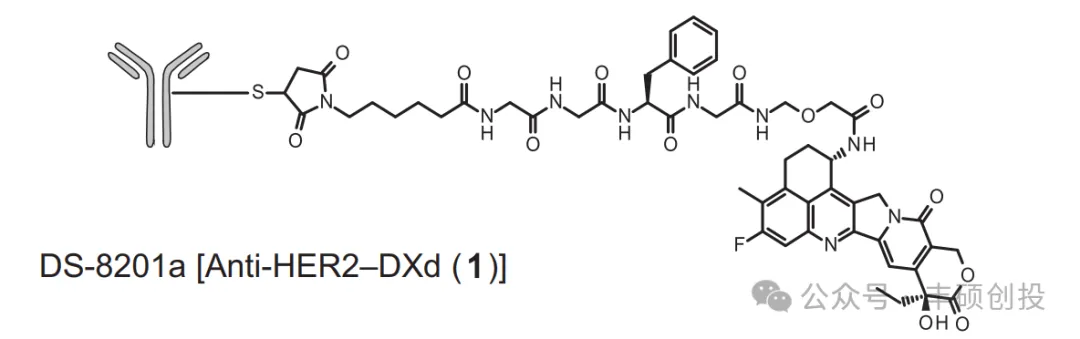
2、双表位的设计或能使更多的患者收益
HER2低表达和曲妥珠耐药人群是HER2 ADC的重要市场机会。以曲妥珠单抗为代表的HER2靶向药物为乳腺癌患者带来显著的临床获益,Her2高表达仅占整体的15%,而Her2低表达乳腺癌患者约占45-55%,传统的Her2单抗疗法在低表达人群中的临床获益欠佳。此外,临床上约14%-31%的早期乳腺癌和几乎全部晚期乳腺癌会对曲妥珠单抗产生原发性或继发性耐药。除此之外Her2疗法耐药机制产生的原因复杂多样,包括HER家族突变使得下游信号通路激活、HER2和HER3突变、HER2表位丢失或掩蔽和代偿通路激活等等。
以曲妥珠抗体为基础的DS-8201在HER2低表达中临床获益率存在提升空间。DESTINY-Breast04研究结果显示,DS-8201在HER低表达患者(HR-\HR+)中临床获益率为62.5%、71.2%,仍存在30%~40%患者无法临床获益。
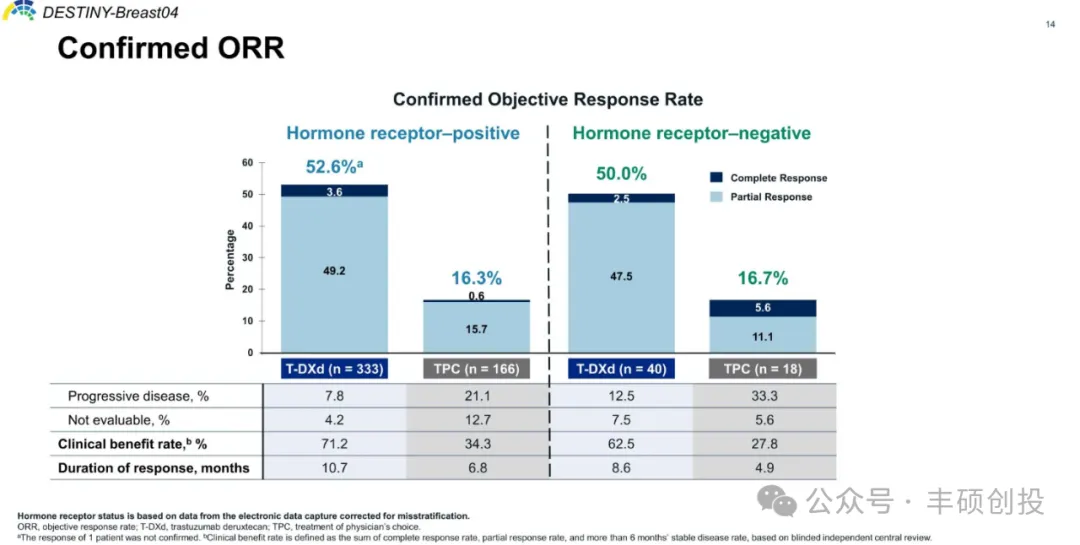
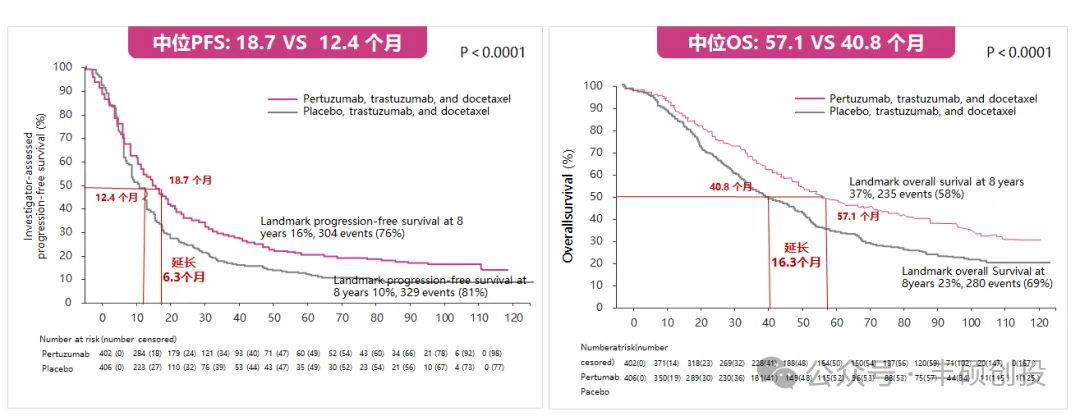
双表位设计能提高ADC内吞,增强细胞毒性与旁杀效应。双表位抗体设计够促进细胞表面HER2受体的聚集,提高受体内化的效率增加ADC药物的内吞,为ADC的细胞毒性或旁观者效应提供更充分的条件。临床前研究中,MEDI4276的双表位抗体介导的HER2受体内吞速率作用明显优于单抗,甚至远超二者联用后的内吞效率。而Zanidatamab双抗不对称设计,能够与细胞表面HER2形成反式结合,类似于“手拉手”的效果将多个HER2连接到一起,并引起HER2受体的聚集在细胞表面聚集(两种单抗联用无此效果),提高受体内吞增强细胞毒性。
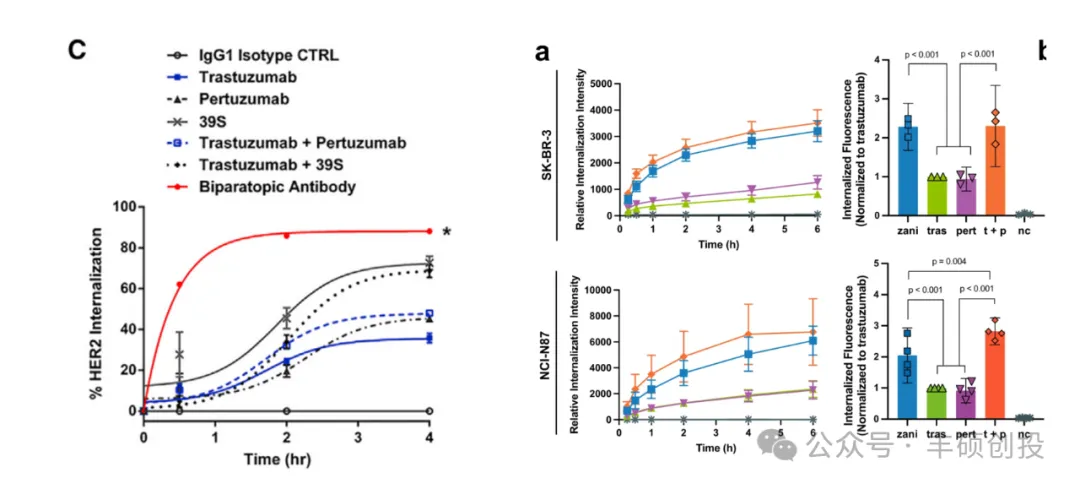
3、HER2 ADC在增效减毒思路下寻找更完美的平衡
ADC是复杂结构药物形式,疗效和安全性间存在微妙的系统性平衡。ZW49和MEDI4276的前车之鉴,已证明HER2 双表位ADC的开发并不简单。即使HER2双表位的设计有诸多好处,但仍旧需要与linker、Dar值、payload等部件形成系统性的平衡,ADC的改造往往牵一发而动全身,细微的改动也可能导致临床结果背离设计的初衷。
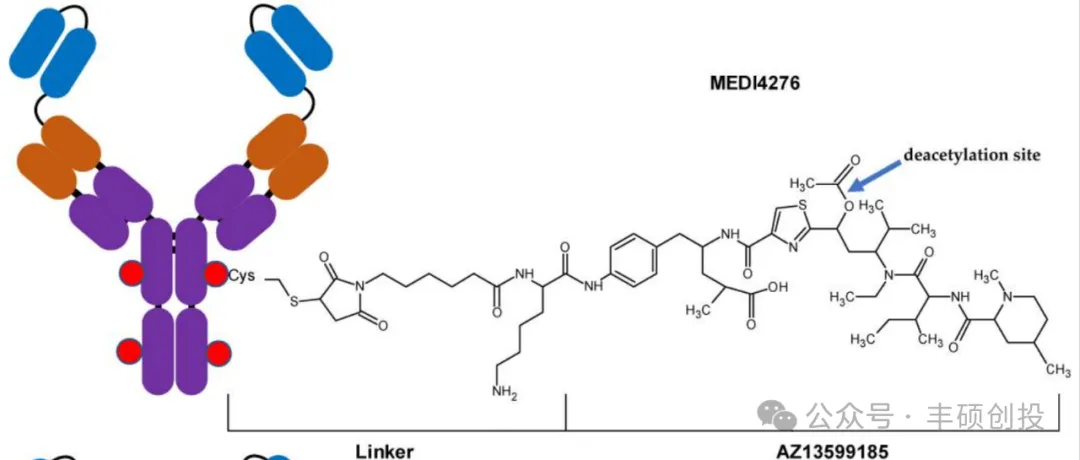
MEDI4276为四价双抗通过可裂解肽linker偶联微管蛋白抑制剂Tubulysins类似物(DAR=4)。在用于治疗HER2阳性晚期乳腺癌和胃癌患者的I期临床研究中,尽管MEDI4276对曲妥珠单抗、帕妥珠单抗、T-DM1治疗失败的乳腺癌患者展示出临床治疗潜力(具有T-DM1的非交叉耐药特性)。但MEDI4276治疗中出现了显着的肝毒性、胃肠道毒性和周围神经病变,并在剂量超过0.5 mg/kg(Q3W,下同)后,AE发生率和严重程度有增加的趋势。MEDI4276最大耐受剂量(MTD)为0.75 mg/kg、0.9mg/kg,MTD下75.0%的患者经历≥1次严重和/或≥3 级AE。结合临床药代动力学数据,由于药物耐受性差MTD太低,导致MEDI4276给药剂量尚未达到组织和循环HER2饱和剂量(3-5mg/kg),无法实现最佳的临床疗效。
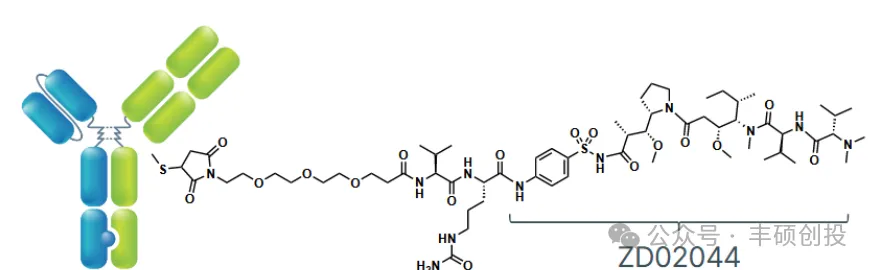
ZW-49为二价HER2双抗通过可酶切连接子偶联Auristatin衍生物(DAR=2)。在I期临床研究中,ZW-49在HER+晚期实体瘤患者(既往治疗中位数=3)中具有良好的安全性,大部分AE为1级或2级包括角膜炎、脱发、腹泻,≥3级TRAE和TRSAE仅有12%、4%。ZW-49最大给药剂量为3mg/kg Q3W未达到MTD,推荐剂量为2.5mg/kg Q3W。但ZW-49疗效却不及预期,ZW-49在8例接受晚期乳腺癌患者中ORR仅有13%,DS-8201在相似患者人群中ORR为60.3%(DESTINY-Breast01研究,既往治疗中位数=5)。
从MEDI4276和ZW49看来,HER2 ADC并未能通过引入双表位抗体就能实现临床收益的提高,还需要综合考虑linker的稳定性、DAR值的控制、毒素小分子等因素。MEDI4276、ZW49都期望通过引入双表位抗体提升ADC活性与响应率,但却在临床试验中出现相反的结果。对比T-DM1设计,ZW49的毒素分子为Auristatin衍生物并降低DAR值,而MEDI4276选择Tubulysins衍生物(IC50与Auristatin相近)且DAR值稍有提升,可能是导致MEDI4276毒性过强,而ZW49疗效不足的问题。

4、DXd专利问题并非核心KN003需要更多的临床证据
安全性方面,治疗相关不良事件(TRAEs)发生27例(84.4%),4例患者(12.5%)发生3级TRAE,1例患者(3.1%)发生2级间质性肺炎(7.3mg/kg组)。发生率超过10%的所有级别常见TRAE为:腹泻(62.5%)、恶心(53.1%)、疲乏(21.9%)、呕吐(21.9%)、食欲减退(18.8%)、腹痛(12.5%)、困倦(12.5%)和脱发(12.5%)。血液学毒性发生率极低。无TRAE导致的死亡或终止治疗。所有患者均已完成剂量限制性毒性(DLT)观察期,未发生DLT事件,研究未达到最大耐受剂量(MTD)。这样的结果相对于DS-8201将近50%≥3级的不良反应发生率来说无疑是优秀的。与之对应的是2020年ASCO会议上的KN026安全性数据,在KN026剂量达到20mpk的时候,才出现了KN003发生率相类似的3级或更高水准的TRAE(7.1%)。根据I期临床个位数患者的有效性评估结果KN003临床疗效如何尚不能对确切的定论。
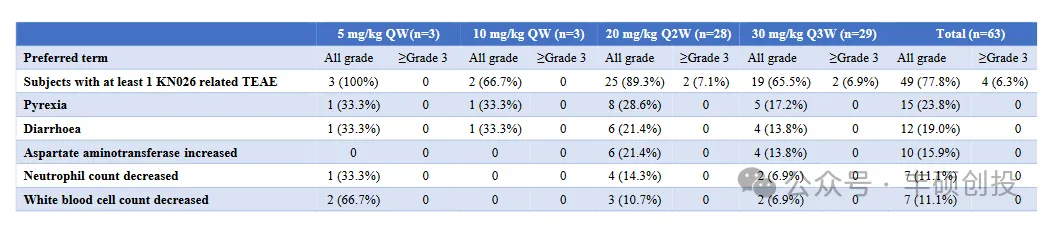
5、总结
DS-8201已在Her2低表达乳腺癌的患者中证明了其难以超越的优势,后来的HER2 ADC玩家基本在DS-8201设计框架上寻找更完美的疗效和安全性平衡。康宁杰瑞KN003希望在HER2双表位的基础上,优化linker的稳定性、适当降低DAR值来获得更好的临床收益,但其设定仍旧需要更多的临床数据证明。从另一角度思考,在DS-8201的框架上进行优化,产品力是否真的能获得突破性的提高呢?即使产品最后能以疗效优势赢得和DS-8201的对决,恒瑞、荣昌、浙江医药等玩家早就为商业化上的激烈竞争埋下伏笔,康宁杰瑞将面临着的艰难商业化挑战。
声明:以上内容仅供参考,不构成投资建议。
本文作者可以追加内容哦 !

