云顶新耀(HKEX 1952.HK)合作伙伴 Calliditas Therapeutics AB(纳斯达克股票代码:CALT,纳斯达克斯德哥尔摩股票代码:CALTX)(以下简称“Calliditas”),在近日举行的第61届欧洲肾脏协会大会(ERA 2024)上,公布了耐赋康(布地奈德肠溶胶囊,NEFECON)最新的积极研究结果,数据表明耐赋康治疗9个月带来的估算肾小球滤过率(eGFR)获益显著优于sparsentan(双效内皮素-血管紧张素受体拮抗剂)持续治疗2年。
云顶新耀首席执行官罗永庆表示:“耐赋康在第61届欧洲肾脏协会大会上展现的积极结果有力证明了耐赋康在保护肾功能方面更具优势,可以为IgA肾病患者带来更显著的获益。中国目前有约500万的IgA肾病患者,每年新增确诊患者超过10万人,约50%具有高进展风险的IgA肾病患者在10-20年内会进展为终末期肾病,因此需要用更积极的治疗去干预,尽早启动对因治疗,控制疾病进展风险。耐赋康作为全球首个对因治疗IgA肾病的药物,目前已经正式在中国大陆上市,未来,我们将继续推动耐赋康的可及性,将这款创新药物带给更多患者,满足迫切的临床需求。“
本次Calliditas公布的研究旨在通过MAIC(匹配调整间接比较)方法比较耐赋康与sparsentan对IgA肾病患者肾功能恶化的影响。eGFR是衡量肾功能的一项指标,被公认为是评估肾功能恶化的临床试验的替代终点。
该研究根据NefIgArd研究的患者特征从PROTECT研究选择匹配人群,使用重复测量混合模型(MMRM)方法分析eGFR的绝对变化,包括基线、3、6、9、12、18和24个月数据、基线eGFR、基线eGFR-时间交互作用、治疗和治疗-时间交互作用。采用MAIC方法评估耐赋康和sparsentan对9、12和24个月时绝对eGFR变化的影响。
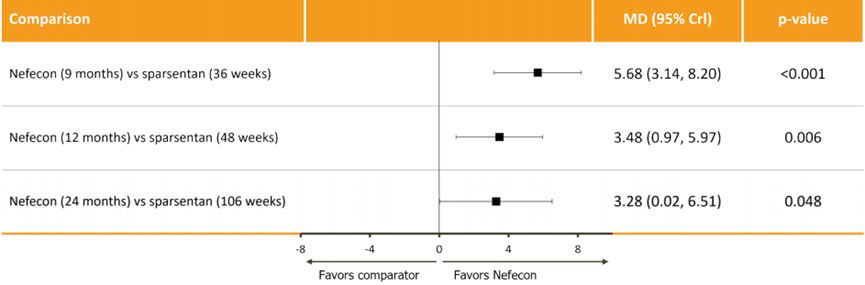
研究结果显示,在9、12和24个月时,耐赋康对eGFR的有利影响均优于sparsentan,且具有统计学和临床显著意义。与sparsentan 400 mg/d连续治疗组比较,在9、12、24个月时,耐赋康组的eGFR改善显著优于Sparsentan(图1)。IgA肾病患者接受耐赋康16 mg/d治疗9个月与sparsentan 400 mg/d连续治疗2年相比,eGFR获益更大,且在治疗开始后9个月就观察到显著差异,并维持长达2年。需要强调的是,在NefIgArd试验中,患者治疗9个月后就停用耐赋康,后续仅为最佳支持治疗,这也是在12和24个月时其与sparsentan eGFR差异缩小的原因。
作为全球首个且唯一获得美国食品药品监督管理局完全批准的对因治疗IgA肾病药物,耐赋康首张处方于今年5月14日在中国大陆成功落地,正式惠及中国大陆的患者。为了帮助更多适用于耐赋康治疗的IgA肾病患者减轻经济负担,接受可持续、规范地治疗,慈善基金会已启动了“护肾赋康援助项目”,为中国大陆地区公民在中国大陆自行使用耐赋康的成人患者提供部分药品援助,帮助患者提高生活质量,延长生命。
耐赋康于2023年11月获得中国国家药品监督管理局的新药上市申请批准,用于治疗具有进展风险的原发性IgA肾病成人患者。此外,耐赋康也已在中国澳门、中国香港和新加坡获批,并于2023年底在中国台湾和韩国分别提交了新药上市许可申请并成功获得受理。
关于耐赋康(NEFECON)
耐赋康(NEFECON)是布地奈德肠溶胶囊,作为全球首个对因治疗IgA肾病的药物,是靶向肠道黏膜B细胞的免疫调节剂,能减少50%肾功能下降2,在中国人群中能延缓肾功能衰退达66%3,预计将疾病进展至透析或肾移植的时间延缓了12.8年4。同时布地奈德首过代谢程度达90%5,具有良好的安全性。耐赋康专为IgA肾病患者研制,每颗胶囊含布地奈德4mg,通过特殊的制剂工艺,将布地奈德靶向释放于回肠末端的黏膜B细胞(包括派尔集合淋巴结),胶囊溶解后,三层包衣微丸持续稳定释放布地奈德,高浓度覆盖整个靶区域,从而减少诱发IgA肾病的半乳糖缺陷的IgA1抗体(Gd-IgA1)产生,进而干预发病机制上游阶段,达到治疗IgA肾病的作用。
2019年6月,云顶新耀与Calliditas签订独家授权许可协议,获得在大中华地区和新加坡开发以及商业化耐赋康的权利。该协议于2022年3月扩展,将韩国纳入云顶新耀的授权许可范围。
关于云顶新耀
云顶新耀是一家专注于创新药和疫苗研发、临床开发、制造和商业化的生物制药公司,致力于满足亚洲市场尚未满足的医疗需求。云顶新耀的管理团队在中国及全球领先制药企业从事过高质量研发、临床开发、药政事务、化学制造与控制(CMC)、业务发展和商业化运营,拥有深厚的专长和丰富的经验。云顶新耀已打造多款疾病首创或者同类最佳的药物组合,公司的治疗领域包括肾科疾病、感染性和传染性疾病、自身免疫性疾病。有关更多信息,请访问公司网站:www.everestmedicines.com。
前瞻性声明
本新闻稿所发布的信息中可能会包含某些前瞻性表述,乃基于本公司或管理层在做出表述时对公司业务运营情况及财务状况的现有看法、相信、和现有预期,可能会使用“将”、“预期”、“预测”、“期望”、“打算”、“计划”、“相信”、“预估”、“确信”及其他类似词语进行表述。这些前瞻性表述并非对未来业绩的保证,会受到风险、不确定性及其他因素的影响,有些乃超出本公司的控制范围,难以预计。因此,受我们的业务、竞争环境、政治、经济、法律和社会情况的未来变化及发展等各种因素及假设的影响,实际结果可能会与前瞻性表述所含资料有较大差别。本公司及各附属公司、各位董事、管理人员、顾问及代理未曾且概不承担更新该稿件所载前瞻性表述以反映在本新闻稿发布日后最新信息、未来项目或情形
的任何义务,除非法律要求。
参考文献:
1. Reich H,et al. #2459-Matching-adjusted indirect comparison of eGFR in patients with immunoglobulin A nephropathy treated with Nefecon (TRF budesonide) or sparsentan. Presented at ERA 2024.
2. Lafayette R, et al. Lancet. 2023 Sep 9;402(10405):859-870
3. 2023ASN. Oral presentation
4. Jonathan Barratt, et al. 2023 ASN. Poster no. SA-PO886.
5. Edsbcker S, et al. Aliment Pharmacol Ther. 1999 Feb;13(2):219-24.
本文作者可以追加内容哦 !

