创新医疗器械,始终是医疗科技革新的核心焦点,其发展一直是医疗行业不变的热点话题。
近年,国内众多具有领先优势的Best-in-class乃至开创性的First-in-class医疗器械项目正在不断涌现。与此同时,国内医疗器械企业在研发周期、项目规模以及技术创新等方面正逐步缩小与国际同行的差距,并开始在全球舞台上崭露头角。
健世科技携自主创新研发的第二代经导管三尖瓣置换系统LuX-Valve Plus在2024美国纽约瓣膜会(New York Valves 2024)上精彩亮相。来自美国心血管研究基金会(Cardiovascular Research Foundation, New York, U.S.)的Juan F. Granada教授正式发布了LuX-Valve Plus TRAVEL II研究的6个月期临床数据。显著的安全性和有效性,以及广泛的适用性和兼容性,使LuX-Valve Plus广受业内专业人士的认可,或将为复杂解剖结构的重度三尖瓣反流患者带来一个全新的治疗方式。
1、创新性再升级,彰显临床应用价值
简单来说,LuX-Valve系列产品以其全球创新的"室间隔锚定"和非径向支撑力设计理念,为三尖瓣反流疾病治疗树立了新的标杆。而LuX-Valve Plus在这一基础上,通过全面升级的经血管输送系统,实现了更为先进的经颈静脉入路方法。
这一创新不仅确保了瓣膜植入过程中的稳定性和安全性,更显著降低了手术风险和患者承受的创伤,足以展现出中国经导管三尖瓣介入置换瓣膜产品和治疗技术的优势和在全球范围内的领先性。
从本次健世科技公布的研究数据来看,LuX-Valve Plus不仅在疗效上取得了令人鼓舞的成果,而且在安全性上也显示出了较低的并发症风险,为患者提供了一个既有效又安全的治疗选择。
在有效性上,绝大多数患者的反流情况得到了明显改善,心功能等级和生活质量方面也展现出显著提升。
首先,100%的患者和97.62%的患者分别在30天时和6个月期时显示无中度及以上反流。其次,在心脏功能方面,按美国纽约心脏协会(NYHA)的标准,80.43%的患者在30天时从术前III/IV级提升到了术后I/II级,并在6个月期时有91.86%的患者提升到了术后I/II级。最后,在生活质量上,依据患者堪萨斯城心肌病变问卷(KCCQ)的评分,在30天时平均提高了15分,6个月时平均提高了20分。
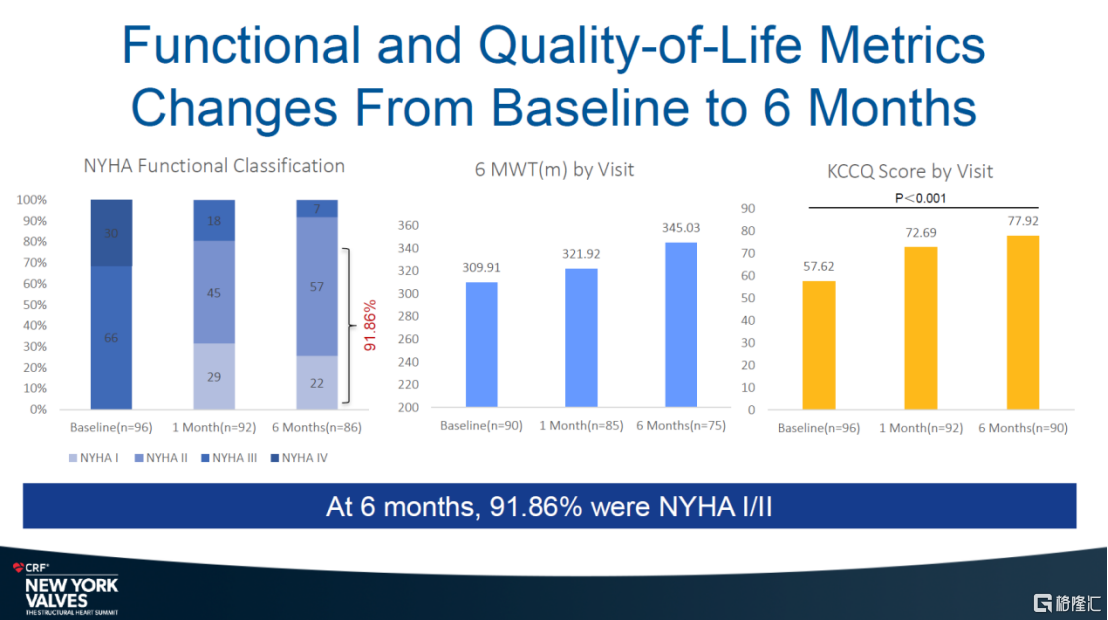
在安全性上,LuX-Valve Plus术后发生严重并发症的概率和全因死亡率都维持在较低水平。
一方面,6个月期的复合事件发生率为8.33%,且诸如心梗、卒中、使用体外膜肺氧合或主动脉内球囊反搏、急性肝功能衰竭、长期机械通气、需要外科干预的心血管损伤、危及生命的大出血事件发生率均为0。另一方面,全因死亡率仅为2.08%,急性肾脏衰竭、重度瓣周漏和中转外科三尖瓣置换或成形术发生率分别为1.04%、2.08%和3.13%,且新发III度房室传导阻滞需植入永久心脏起搏器的发生率仅1.04%。

LuX-Valve Plus作为国内在研经导管三尖瓣置换产品进展领先的产品,这组数据的优异表现不仅为其后续的全球商业化推进提供了坚实的数据支撑,而且对健世科技以及整个三尖瓣介入市场具有重大的里程碑意义。
2、临床应用成果引众多专家瞩目,凸显全球影响力
与此同时,多位心血管领域的专家学者也都对LuX-Valve Plus临床价值给予了高度认可,标志着其在全球范围内的认可度和影响力正日益扩大。
例如,来自德国慕尼黑路德维希·马克西米利安大学医院的Jrg Hausleiter教授此前已在今年5月份的欧洲介入心脏病学大会(EuroPCR 2024)上分享了LuX-Valve Plus在全球多中心的同情救治经验的临床数据;并在此次美国纽约瓣膜会上,再次指出了LuX-Valve Plus的广泛适用性,特别是对于那些不适合传统T-TEER术式的患者,如瓣口接合缺陷较大或超大瓣环患者,以及超声影像质量不佳的情况。LuX-Valve Plus不仅扩大了治疗选择,还为超大解剖结构的患者提供了新的希望,并展示了出色的早期治疗效果。目前,该产品以获得CE认证为目标的注册临床试验正在欧洲进行。
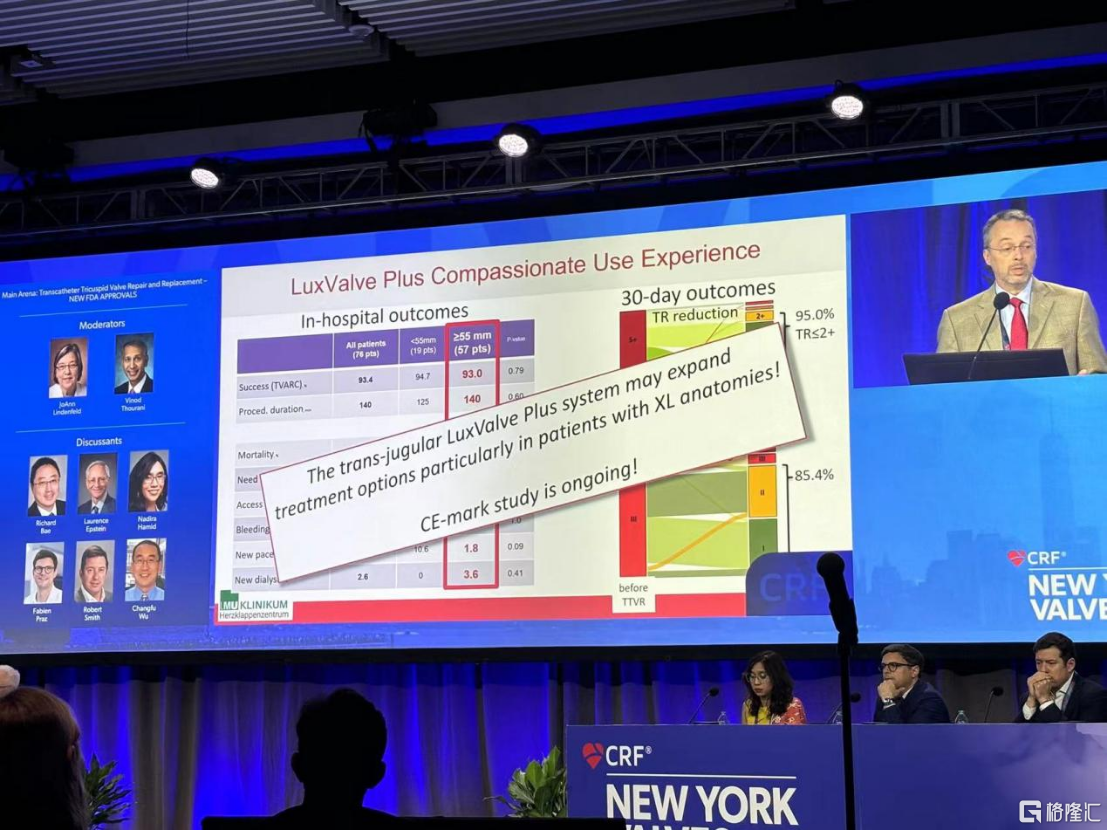
来自法国波尔多大学医院的Thomas Modine教授指出,LuX-Valve Plus为三尖瓣反流的治疗提供了创新的解决方案。面对大瓣环、起搏器或心脏除颤器ICD导线的影响等临床难题,LuX-Valve Plus都能提供有效的应对策略。Modine教授还提到,根据TRAVEL II研究的6个月期随访结果,LuX-Valve Plus不仅缩短了器械操作时间,显现出较低的复合事件发生率,还显著改善了患者的心功能和生活质量,并且能够与术前已存在的起搏器导线兼容。

来自中国香港玛丽医院的Simon Lam教授则展示了LuX-Valve Plus应用的一个复杂案例。一位高龄男性患者在两年前接受了二尖瓣和三尖瓣TEER术式,但后复发三尖瓣反流。 Lam教授成功地为患者进行了二尖瓣TEER术式和用LuX-Valve Plus行三尖瓣TTVR术式,且未取出先前植入的三尖瓣修复夹。这一案例不仅体现了LuX-Valve Plus可以与二尖瓣术式并行,更可以兼容三尖瓣原位的其他修复夹产品,并展现了其在复杂情况下应用的安全性和有效性。
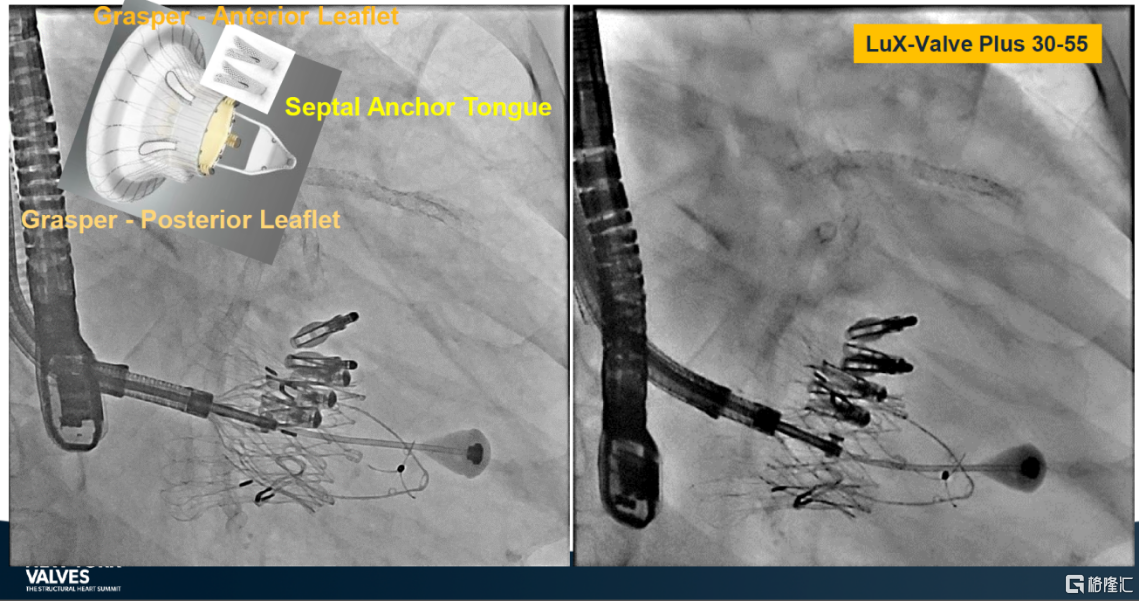
最后,来自美国纽约蒙特法沃医疗中心的Azeem Latib教授在TTVR研究分享中对LuX-Valve Plus给予了高度评价。他指出,TTVR在消除三尖瓣反流、改善症状和生活质量方面表现出色,能够成为一线的治疗选择。Latib教授还提到,一些TTVR器械在临床试验中出现了较高的严重出血率和起搏器植入率,但LuX-Valve Plus却保持了较低的起搏器植入率。他总结道,合适的患者和器械选择,以及较短的学习曲线,能够显著降低并发症的发生率。
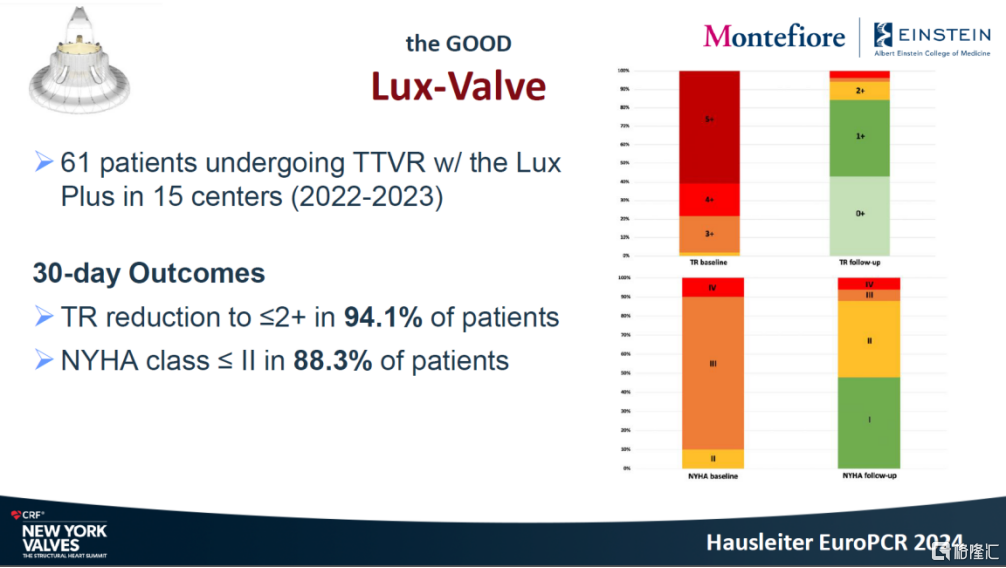
通过这些专家的分享和研究数据,我们可以看到LuX-Valve Plus不仅在技术上实现了创新,更初步验证了其在实际应用中的有效性和安全性,预计将为患者带来了新的治疗方式。
3、需求驱动,全球百亿美元市场规模下的一大业绩增长推动引擎
那么,作为投资者,又应当如何理解?
直观看到一组数字,Frost&Sullivan预计2023年至2030年期间,全球三尖瓣介入器械市场规模将从0.32亿美元增长至112.80亿美元,CAGR达131.14%,正迎来爆炸式增长,凸显出全球心血管疾病治疗领域的巨大潜力和市场需求。
特别是在中国市场,随着人口老龄化的加剧,中度至重度三尖瓣反流患者的数量预计将在2030年增至1060万人。这一人口结构的变化,预示着对微创、安全、有效的治疗方案的需求将持续增长。Frost&Sullivan预计,中国的经导管三尖瓣介入治疗(TTVI)市场将从2023年的8560万元增至2030年的203亿元人民币,年复合增长率为118.29%。
面对这一巨大的市场潜力,健世科技的LuX-Valve Plus展现出了巨大的市场前景。
目前,全球仅有爱德华的EVOQUE经导管三尖瓣置换产品获批上市,健世科技的LuX-Valve Plus正在欧洲开展注册临床,在美国也正式开启了IDE的准备工作,在国内预计近期递交注册,有望成为全球首批商业化的经导管三尖瓣置换产品之一,填补市场空白。
中泰证券指出,2023年爱德华经导管二尖瓣和三尖瓣治疗(TMTT)板块营收达约1.98亿美元,同比增速高达67%。而伴随着EVOQUE在欧洲、美国市场的陆续上市,预计2024年爱德华TMTT业务销售额有望超过此前2.8亿美元至3.2亿美元的指引。
通过这一预测不难判断,若LuX-Valve Plus能够顺利商业化,其凭借在国内的先发优势,以及全球众多未被满足临床需求的背景下,有望迅速抢占市场份额,为健世科技带来显著的业绩增长。
4、小结
健世科技此次携LuX-Valve Plus在2024美国纽约瓣膜会上的亮相,一方面6个月期的随访结果初步验证了产品的安全性和有效性,不仅能预期为全球患者提供新的治疗方式,也为公司商业化能力奠定坚实的基础;另一方面也展现出LuX-Valve Plus在推动医疗技术创新、满足市场需求、激发市场活力以及增强中国在全球医疗器械行业中的竞争力方面的重要作用。
相信随着LuX-Valve Plus顺利推进上市,也将助力健世科技内在价值不断释放,估值水平获得进一步提升。$健世科技-B(HK|09877)$
本文作者可以追加内容哦 !

