近日,海南普利制药股份有限公司旗下的全资子公司浙江普利药业有限公司,收到FDA签发的布立西坦片的暂时性批准。
这是普利制药今年收到的第11张美国ANDA,标志着待UCB公司持有的布立西坦专利US6911461和US 10729653分别将于2026-02-21和2030-04-09到期失效后,即可转为正式批准,届时可具备在美国销售布立西坦片的资格。

普利制药的布立西坦注射液已于2024年3月获得FDA签发的暂时性批准,布立西坦口服液已于2024年8月中旬获得FDA签发的暂时性批准,布立西坦片的顺利获批标志着普利制药在抗癫痫领域内多年来的持续深耕终结硕果。口服固体剂型+口服液体剂型+注射剂,三种剂型实现全方位发力。
癫痫是一组由于脑部神经元异常过度放电引起的反复、发作性和短暂性的中枢神经系统功能失常的慢性脑部疾病。目前,癫痫已经成为中国神经系统第二大疾病,全球超过7000万人受其影响。每年每10万人口为28至70例发病率,癫痫的终生患病率约为3-5%。癫痫发作给患者、家庭、乃至整个社会带来沉重的疾病负担。
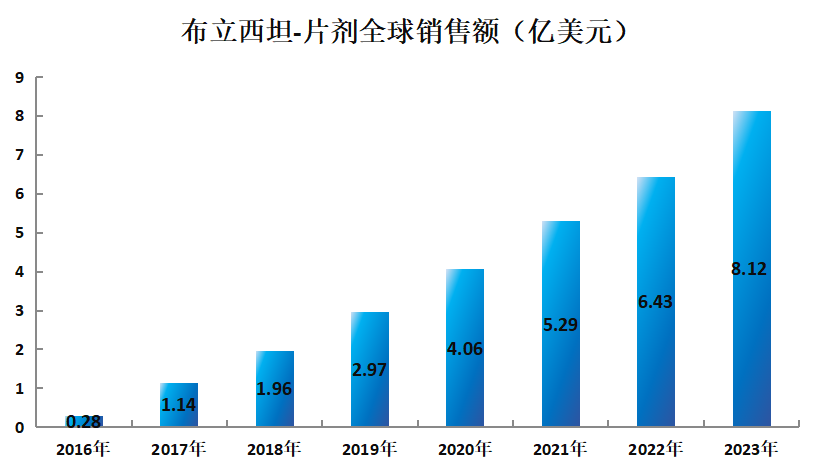
据IQVIA数据,布立西坦片剂近三年增长趋势如下:2021年全球销售额约5.3亿美元,其中美国市场销售额约3.4亿美元,占比65%;2022年全球销售额达到约6.4亿美元,其中美国市场销售额约4.3亿美元,占比66%;2023年全球销售额达到约8.1亿美元,其中美国市场销售额约5.3亿美元,占比66%,美国为布立西坦片剂全球第一大市场,布立西坦的市场潜力巨大。
抗癫痫发作药物(ASMs)是癫痫治疗最重要、最基本的措施,也是大部分癫痫患者的首选治疗方式。过去的几十余年里,随着科学研究的不断深入,陆续出现了不少ASMs,为癫痫患者带来福音,然而,癫痫治疗依然存在未满足的需求,三分之一的癫痫患者尽管接受了ASMs治疗,仍会出现无法控制的癫痫发作;许多癫痫患者深受ASMs不良反应的困扰,治疗依从性差,甚至终止治疗,导致死亡风险增加。因此,亟需更安全有效、且耐受性好的创新药物出现,以加强对癫痫发作的控制,减少副作用,改善患者整体生活质量。
本文作者可以追加内容哦 !

