
8月28日,据CDE官网最新公示,$阿斯利康(US ADR)(NASDAQ|AZN)$申报的acalabrutinib Maleate片(通用名:阿可替尼胶囊)上市申请已获得受理。据公司官网消息,推测此次阿可替尼申报上市的新适应症可能是一线治疗慢性淋巴细胞白血病(CLL)。

据药融云数据库显示,阿可替尼是新一代高选择性原研BTK抑制剂,通过与BTK共价结合抑制其活性。在B细胞中,BTK信号导致B细胞增殖、转运、趋化和粘附所需的途径激活。
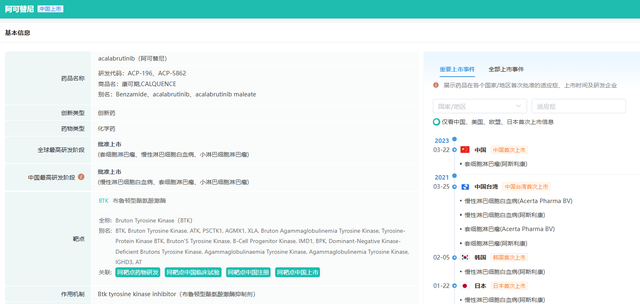
在中国,阿可替尼于2023年3月首次获批上市,用于治疗既往至少接受过一种治疗的成人套细胞淋巴瘤(MCL)患者;同年9月,其治疗领域进一步拓展,获批作为单药治疗既往至少接受过一种疗法的成人慢性淋巴细胞白血病(CLL)及小淋巴细胞淋巴瘤(SLL)患者。
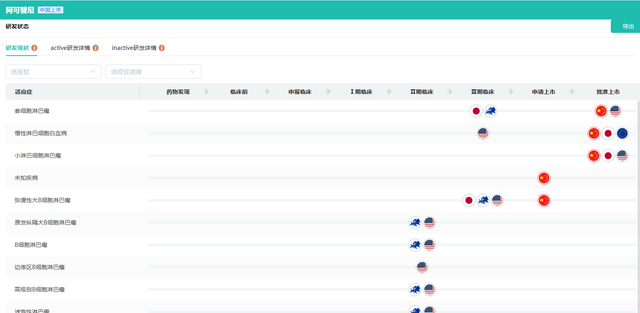
今年4月,$阿斯利康(UK)(LSE|AZN)$欣然宣布,在其主导的中国3期ChangE临床试验中,阿可替尼针对未治疗的慢性淋巴细胞白血病(CLL)患者展现出了显著的统计学与临床意义优势,特别是在无进展生存期方面。这项开创性的随机、多中心、开放标签3期临床试验,不仅由中国引领,还汇聚了66%来自中国(含中国台湾地区)的患者参与。该试验旨在评估阿可替尼与苯丁酸氮芥联合利妥昔单抗相比,对未经治疗的CLL患者的安全性和有效性。
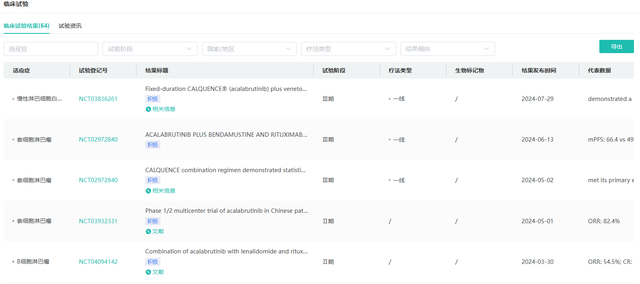
ChangE试验的核心成果显示,阿可替尼在全部预设亚组中均实现了与苯丁酸氮芥联合利妥昔单抗相比,统计学上显著且临床显著的无进展生存期(PFS)延长。此外,试验数据还透露出,相较于对照组,阿可替尼在总体生存期(OS)方面亦展现出积极的改善趋势,为CLL患者带来了新的治疗希望与选择。
参考来源:
[1] CDE官网
[2] 药融云数据库
<END>
本文作者可以追加内容哦 !

