一、国家药品审评中心DNA,去重后排名11!
9月还有16个工作日
先观察排名第1的3月2日进中心,
再观察排名第2和第3的3月13日进中心,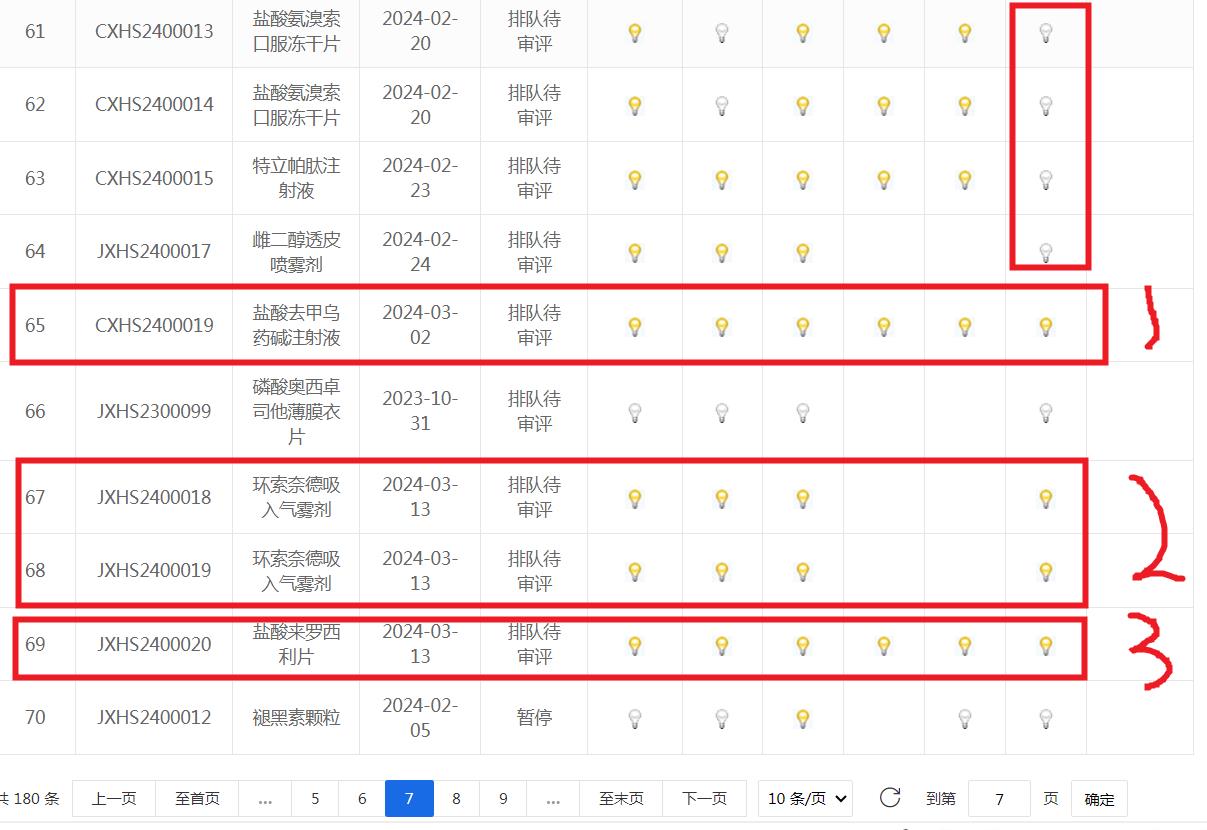
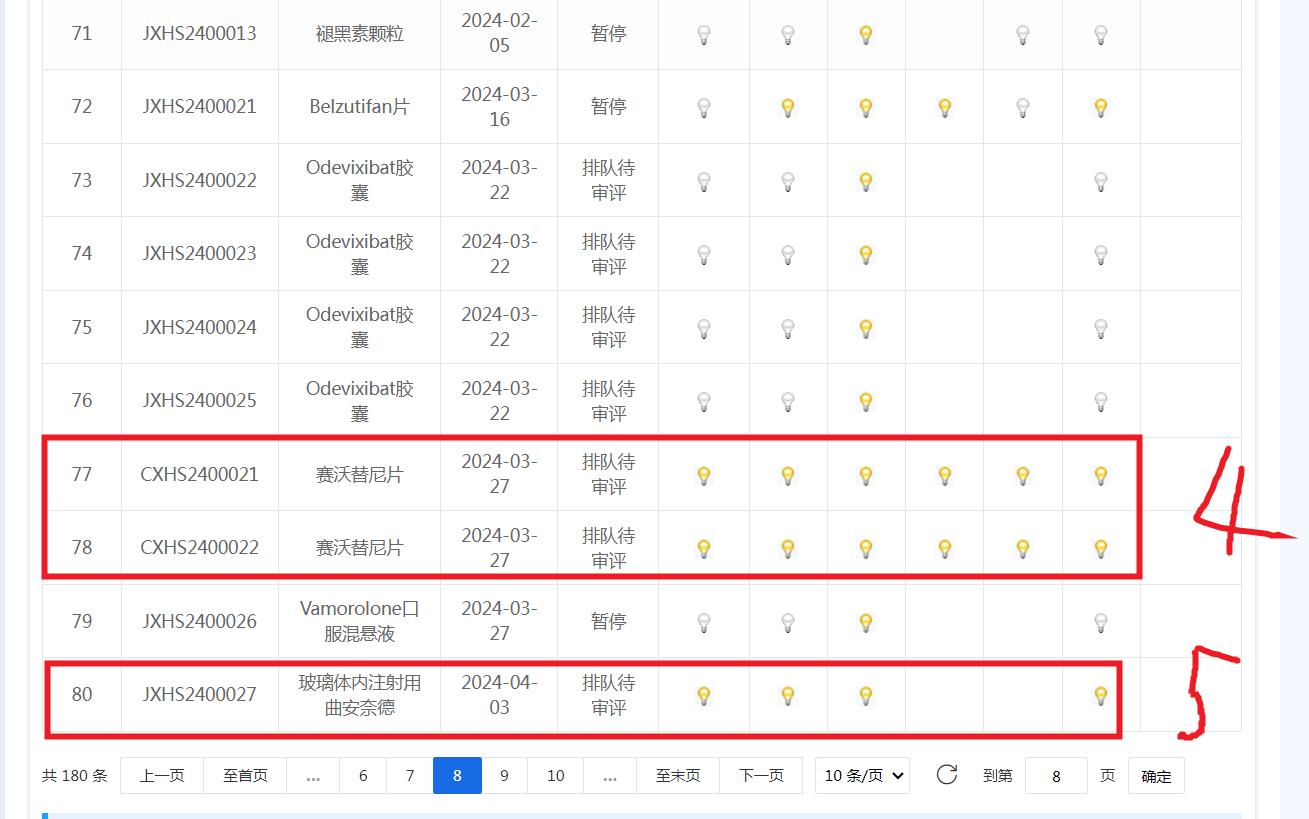
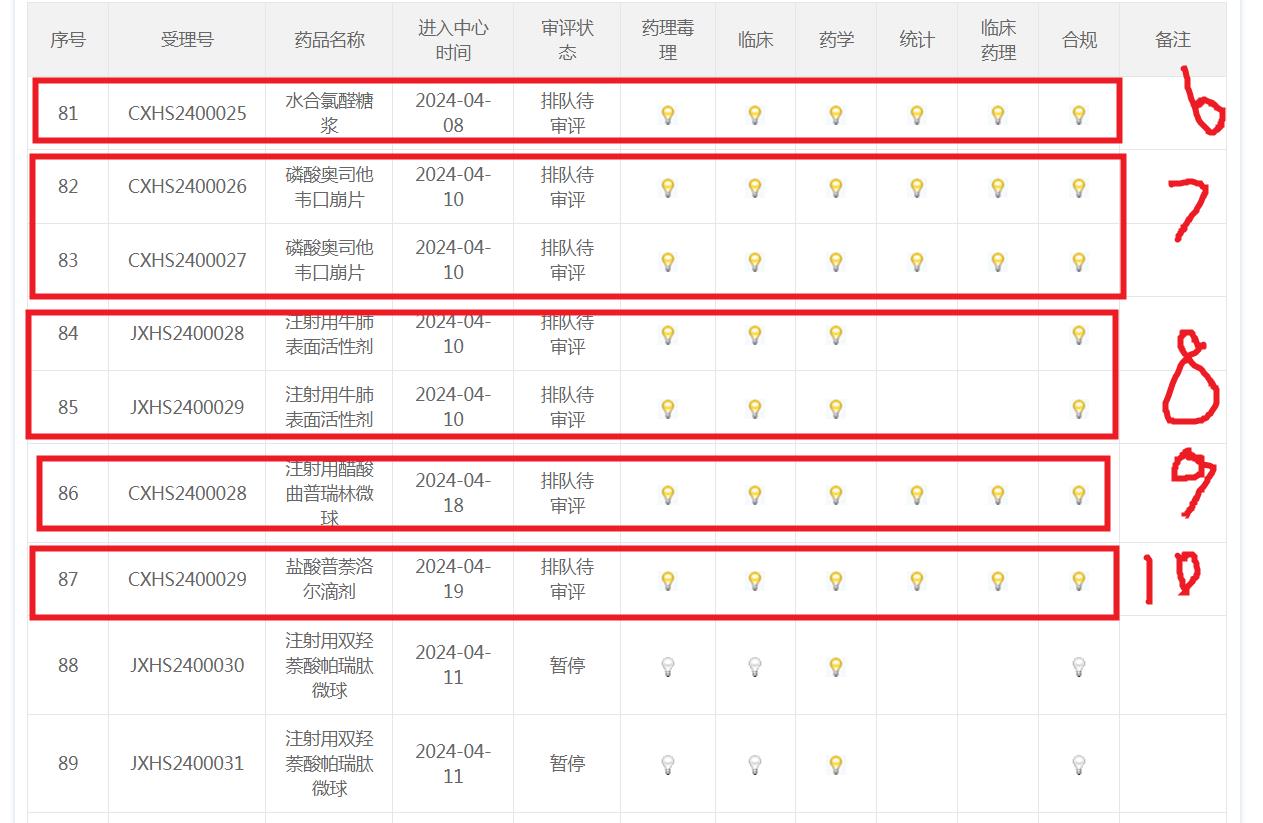
二、9月以来,审评加速
比如,2月7日进中心,非优先审评的玛仕度肽注射液(减重适应症),8月29日临床项灯先灭,而不是合规项灯先灭!
到了9月6日,只剩下药学灯未灭,只用了1周时间!
看来休假专家回来干活了!
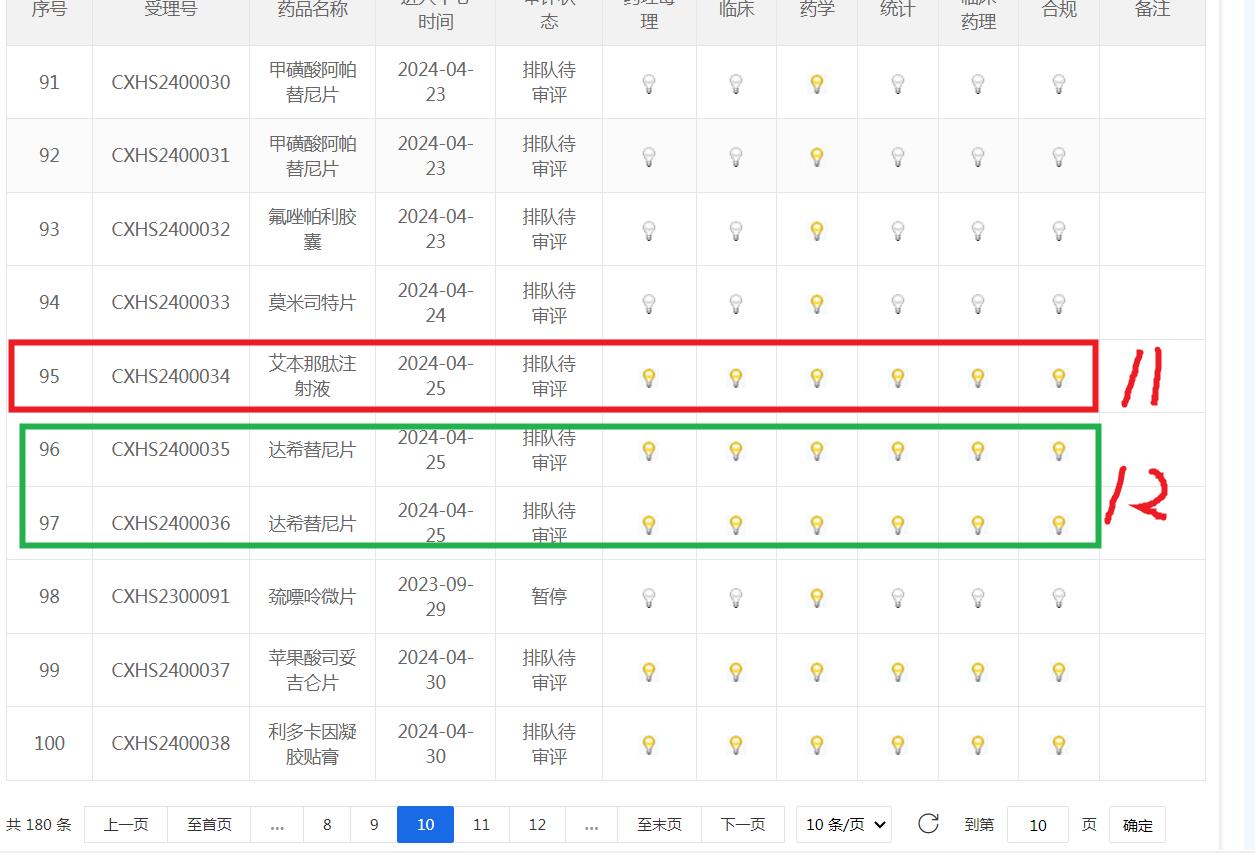
艾本那肽可能是临床项灯先灭,也可能是合规项灯先灭!
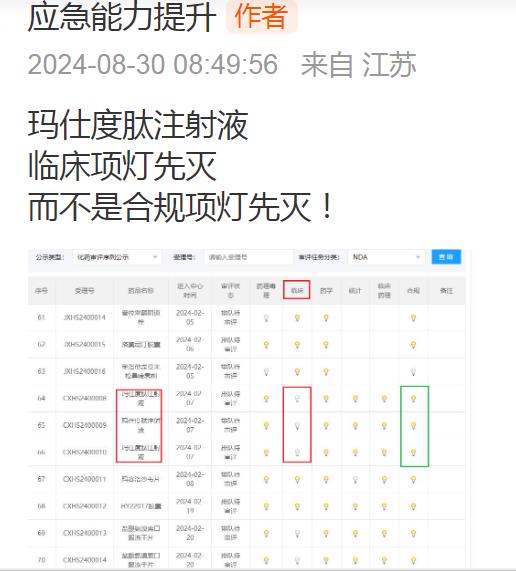
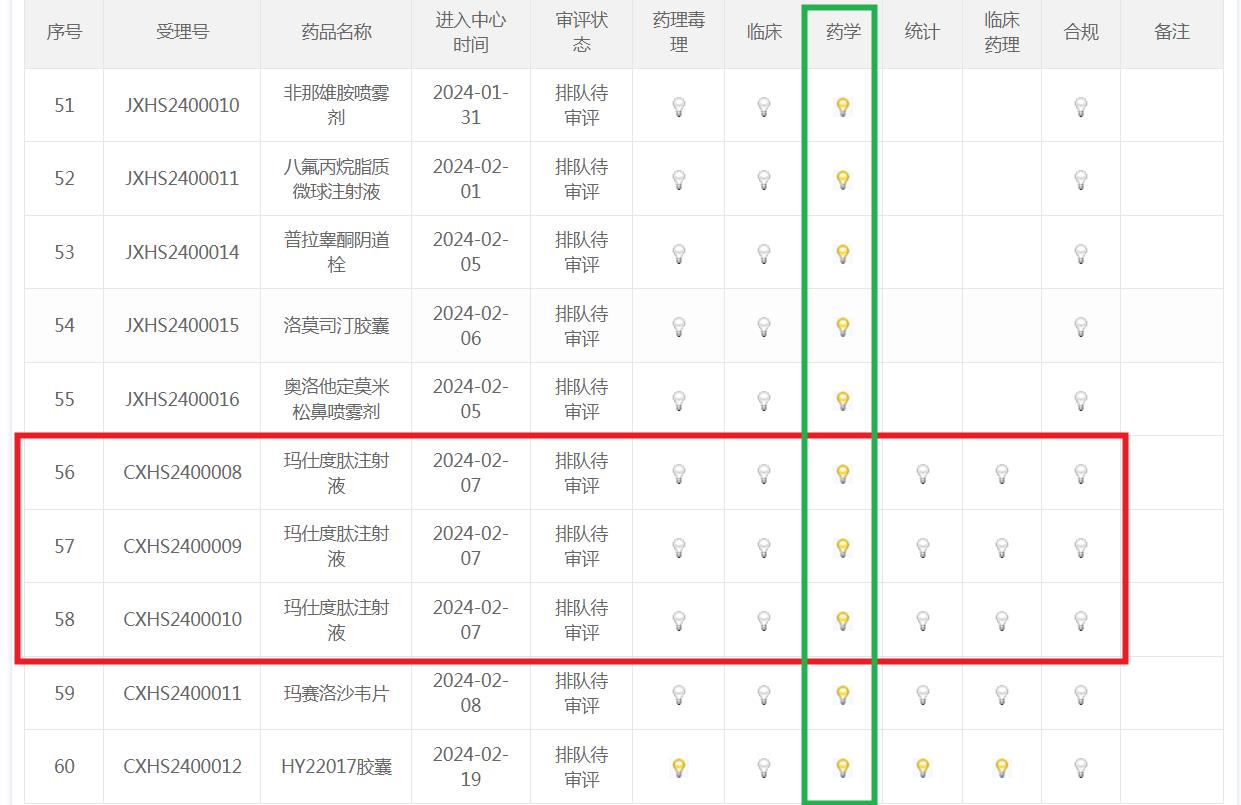
三、艾本那肽审批9月灭第1灯,比何时获批更重要
8月20日,艾本那肽原料药登记数据变更,至少可以理解为应药监审批部门的审批活动而进行的一次重要的艾本那肽原料药登记数据变更。
艾本那肽审批9月灭第1灯,会象玛仕度肽注射液一样,一周内5灯灭,只剩下药学灯未灭。
只要再观察玛仕度肽注射液的药学灯灭的时间间隔,就可大概知道何时获批!
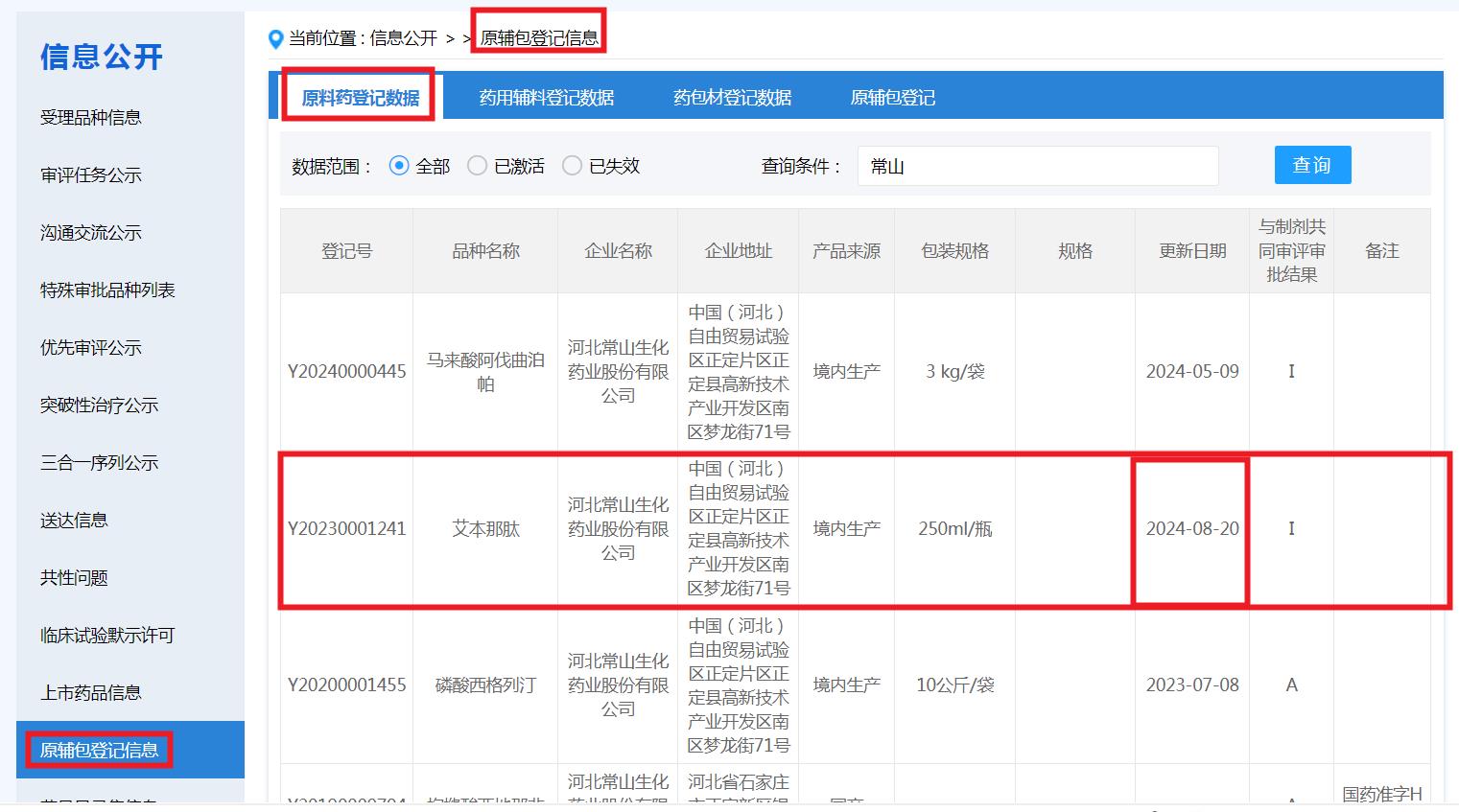
四、艾本那肽审批1灯未灭,不是药监审批部门的审批活动一动不动,只是审批活动不为外界所知,只是公司过于低调!
再以国家药品审评中心DNA,去重后排名NO1盐酸去甲乌药碱注射液为例:
CXHS2400019,盐酸去甲乌药碱注射液,2024-03-02进中心,6灯1灯未灭!
 但事实是:4月收到药审中心3个通知(注射液药学、临床、原料药药学),7月就通过了3项审评(注射液药学、临床、原料药药学)。
但事实是:4月收到药审中心3个通知(注射液药学、临床、原料药药学),7月就通过了3项审评(注射液药学、临床、原料药药学)。
但到9月7日,仍是1灯未灭!

五、艾本那肽审批最近的公司公告为半年报第11页表述
在积极推进后续的现场核查、GMP 符合性检查、药品注册检验。

六、看看9月5-6日,艾本那肽与CXHS2300091巯嘌呤微片进位与退位的次序,可断定艾本那肽已到窗口,在实质性审评
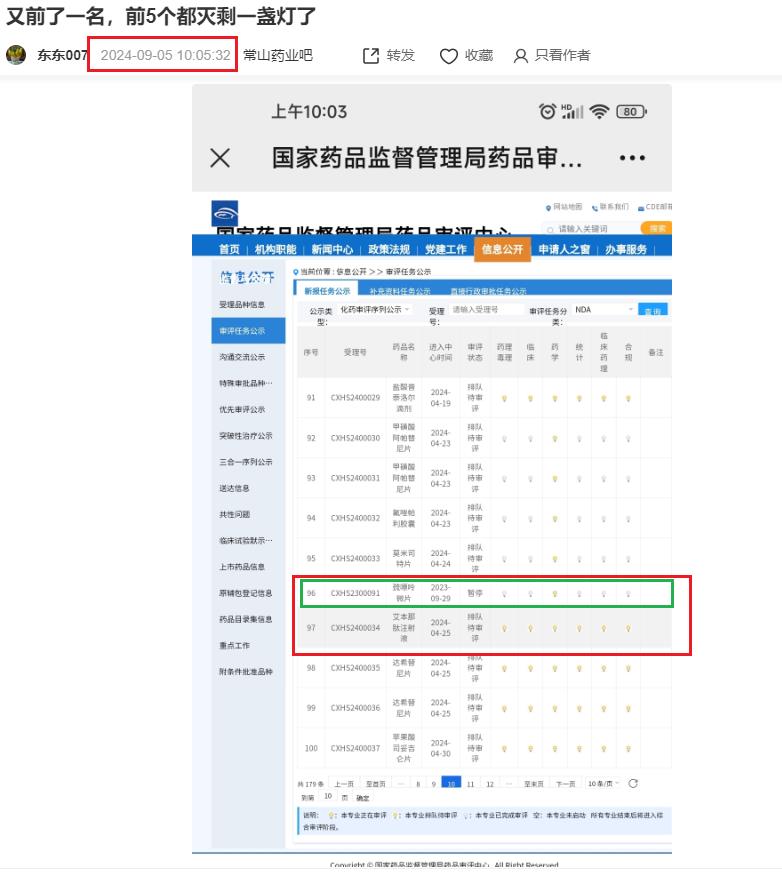
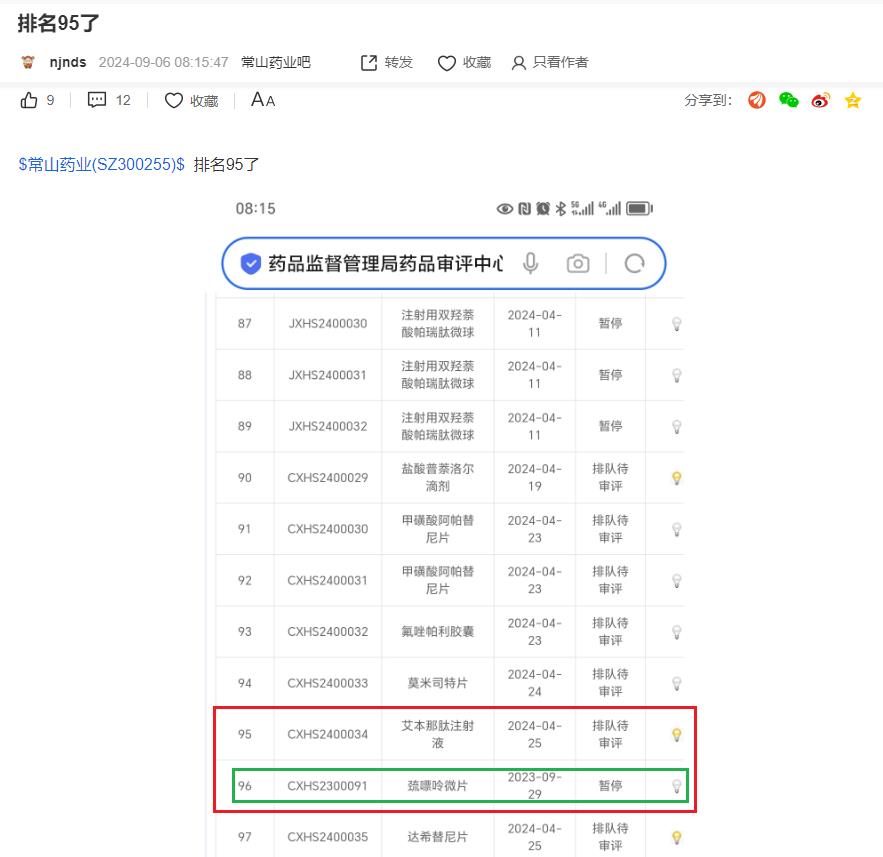
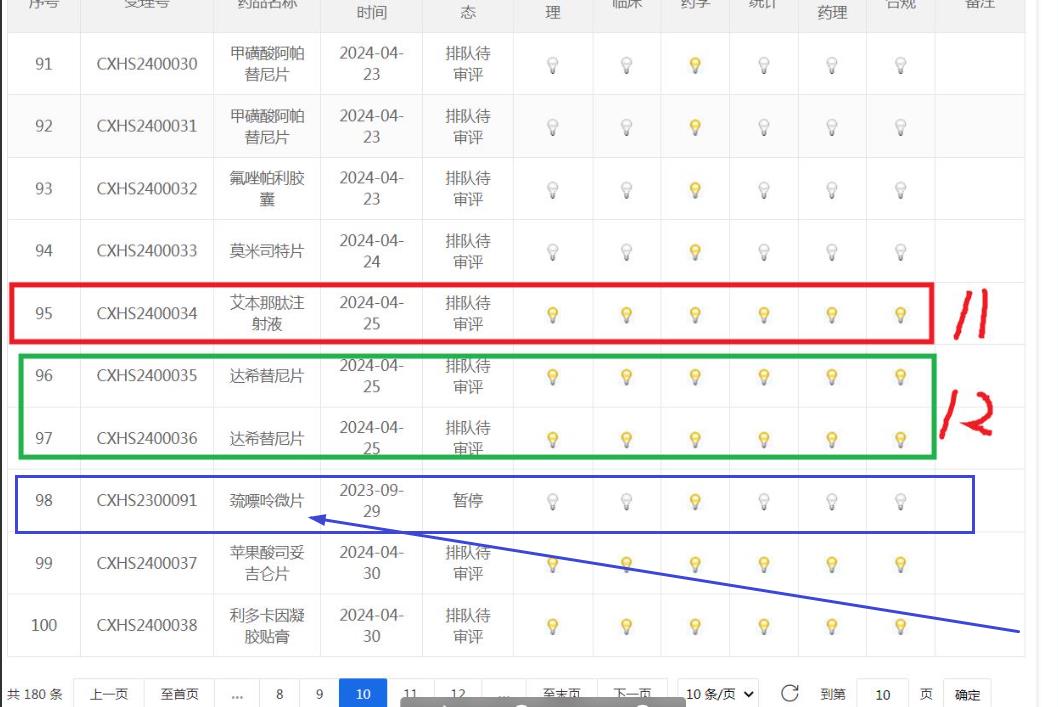
七、看看9月12日,CXHS2300091巯嘌呤微片再次退位到第13名后,再次强化断定艾本那肽已到窗口,在实质性审评
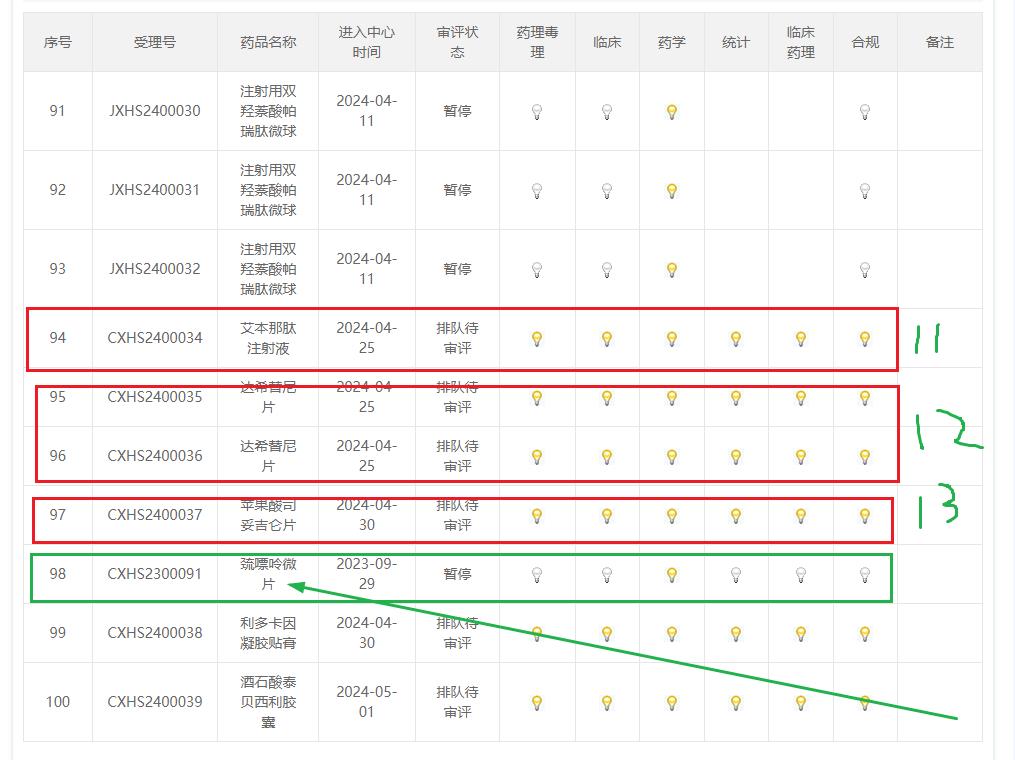
本文作者可以追加内容哦 !

