
临床阶段生物技术公司Nectero Medical近日宣布完成9600万美元的D轮融资。本轮融资由Norwest Venture Partners领投,波士顿科学公司(Boston Scientific Corporation)、BioStar Capital、Cadence Healthcare Ventures、Aphelion Capital和其他公司跟投。募集资金将用于加快执行 II/III 期(stAAAble)试验,并支持向美国食品药品管理局(FDA)提交 Nectero 血管内动脉瘤稳定治疗(Nectero EAST)系统的新药申请(NDA)。
Nectero EAST系统是一种研究型、一次性使用的血管内系统,可将五聚吡咯葡萄糖(PGG)局部注入动脉瘤壁,使其与弹性蛋白和胶原蛋白结合,从而增强主动脉血管壁的强度,并有可能减少进一步降解。整个过程不到一小时,不会留下永久性植入物。2024 年 1 月,Nectero Medical 启动了一项 II/III 期临床试验(stAAAble),研究 Nectero EAST 系统对最大直径为 3.5 - 5.0 厘米的肾下腹主动脉瘤(AAA)患者的安全性和有效性。
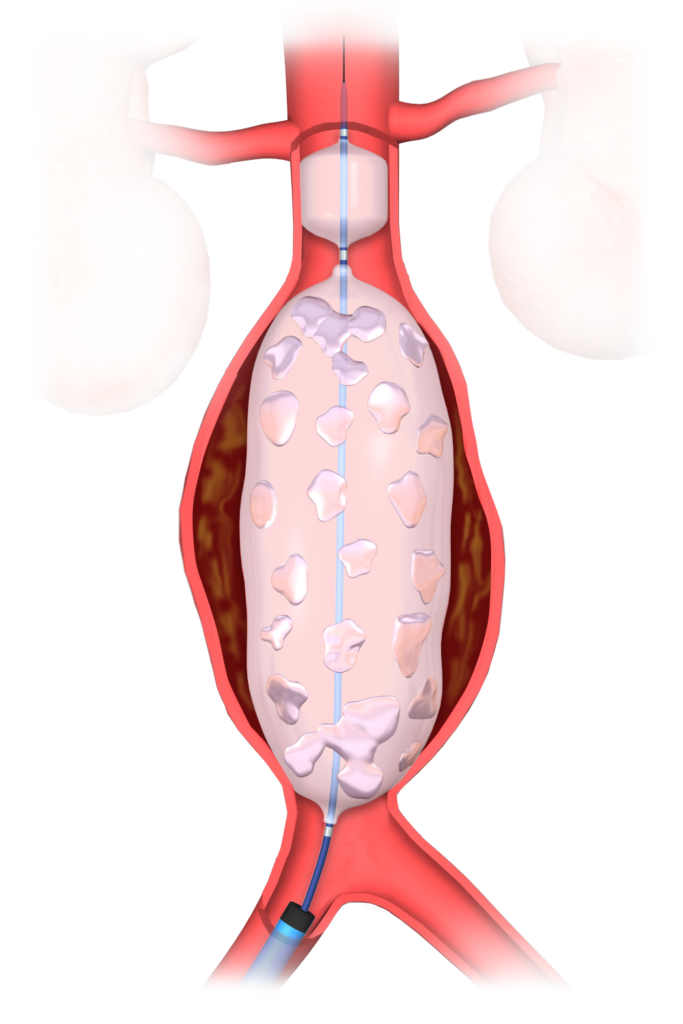
关于Nectero EAST系统
Nectero EAST系统是一种一次性使用的血管内系统,用于治疗肾下腹主动脉瘤(AAA)。据估计,超过 100 万美国人确诊患有 AAA,每年约有 6 万人接受治疗;美国每年约有 1 万人死于 AAA 并发症。现有的治疗方法主要针对直径大于 5.0/5.5 厘米(女性/男性)的 AAA、有症状的患者或迅速扩张的动脉瘤。较小的 AAA 传统上采用连续超声或 CT 监测,每年的破裂风险为 0.5-5%。
Nectero EAST 系统由双球囊输送导管和含有五聚吡咯葡萄糖 (PGG) 的稳定剂混合物组成。该系统将 PGG 运送到动脉瘤壁局部,使其与弹性蛋白和胶原蛋白结合,从而增强主动脉血管壁的强度,降低进一步退化的风险。对于受过血管内技术培训的血管外科医生来说,这种手术不需要任何专用工具,只需不到一个小时就能完成,不会留下永久性植入物,也不会排除今后的任何干预措施。公司的首次人体("FIH")研究的早期临床结果最近发表在《血管外科杂志》(Journal of Vascular Surgery)上。2023 年,Nectero EAST 系统被授予 "快速通道 "和 "突破性疗法 "称号,用于治疗最大直径为 3.5 - 5.0 厘米的肾下动脉瘤患者。Nectero EAST 系统治疗肾下动脉瘤患者的安全性和有效性正在 Nectero EAST 系统治疗中小型腹主动脉瘤 (AAA) StaBiLization 项目中进行研究: 疗效评估 (stAAAble) 临床试验。如果成功,Nectero EAST 系统将为较小的 AAA 患者提供除监测外的首个获批治疗方案。
本文作者可以追加内容哦 !

