| 1398人浏览 | 2024-09-11 07:49 |
近日,复星医药自主研发的治疗ALK 阳性非小细胞肺癌(NSCLC)的创新药复瑞替尼(Foritinib,SAF-189s)III期研究期中分析结果于2024年世界肺癌大会(WCLC)期间重磅发布。
由上海同济大学附属东方医院周彩存教授牵头开展的复瑞替尼III期REMARK研究荣幸入选此次大会的最新突破性摘要(LBA,编号:OA09.03),并由主要研究者上海同济大学附属东方医院稳教授口头汇报了其治疗ALK 阳性非小细胞肺癌(NSCLC)患者的主要期中分析结果1,再次表明复瑞替尼是极具前景的治疗非小细胞肺癌的创新药物。
肺癌位居全球及中国癌症的发生率和死亡率首位2-3。2022年,中国肺癌新发患者高达约106万,肺癌死亡人数亦超过73万3。肺癌患者中约80%-85%为非小细胞肺癌,而我国NSCLC患者中约5.6%呈现间变性淋巴瘤激酶(ALK)基因突变4-5。目前多项研究表明了二代或三代ALK抑制剂的疗效,ALK阳性患者治疗进入“慢病化”管理模式。但耐药、疾病复发和中枢神经系统进展、以及各种安全性等问题仍然存在。因此,临床上亟需一款兼顾安全性和疗效的可及性药物。复瑞替尼(Foritinib)是一种在研的高效、具有CNS高渗透性的ALK/ROS1抑制剂,且具有非常好的安全性6。
研究方法
REMARK研究是一项开放标签、随机、III期临床研究,纳入了既往未经治疗的ALK阳性晚期NSCLC患者。患者根据基线ECOG评分(0/1 vs 2)和是否发生CNS转移进行分层分析,并按1:1比例随机分为接受复瑞替尼治疗(160 mg,每日一次)或克唑替尼治疗(250 mg,每日两次)。研究主要终点为由独立评审委员会(IRC)评估的无进展生存期(PFS),次要终点包括由研究者(INV)评估的PFS和客观应答率(ORR);由IRC和INV评估的应答时间(TTR)和应答持续时间(DOR);由IRC评估的颅内 ORR(C-ORR)、颅内TTR(C-TTR)、颅内DOR(C-DOR)和所有受试者至CNS进展时间(CNS-TTP);以及总生存期(OS)和安全性(图1)。
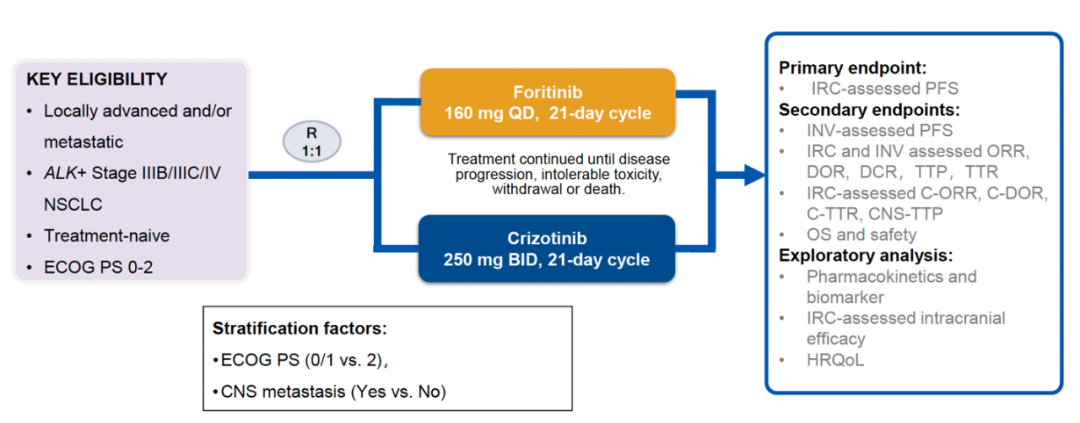
图1. 研究设计
研究结果
从2020年12月至2022年3月,该研究共招募275例患者,其中139例接受复瑞替尼治疗,136接受克唑替尼治疗(图2)。截至2024年3月,中位随访时间为16.7个月
本文作者可以追加内容哦 !

