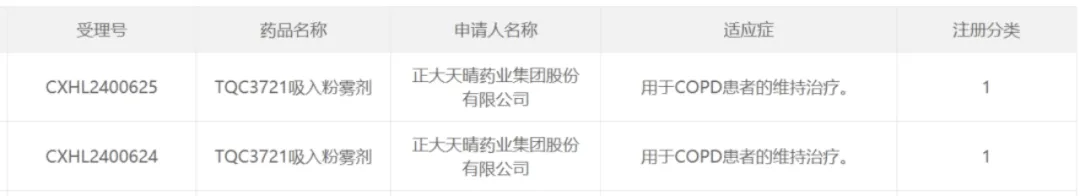
9月9日,中国国家药监局药品审评中心(CDE)官网公示,中国生物制药研发的1类新药TQC3721吸入粉雾剂获批临床,拟开发用于慢性阻塞性肺疾病(COPD)的维持治疗。TQC3721是中国研发进度最快的国产PDE3/4双重抑制剂。目前,吸入混悬液剂型正在中国开展治疗中重度COPD的II期临床研究,本次为吸入粉雾剂剂型首次在中国获批临床。
慢性呼吸系统疾病是全球第三大致死原因,2019年导致近400万人死亡[1]。慢性阻塞性肺疾病是一种进行性疾病,可引起肺部气流阻塞,导致呼吸困难。即使是单次急性加重也可能带来肺功能下降率的显著增加、生活质量的显著恶化,并可显著降低预期寿命,增加死亡风险。改善肺功能,减少急性加重和管理日常症状是此疾病管理中的重要治疗目标。
TQC3721是一款PDE3/4双重抑制剂,PDE3主要作用于支气管平滑肌,PDE4主要在各种炎症细胞中表达,抑制它可减轻炎症反应。TQC3721通过双靶点抑制,并在一个化合物中同时实现支气管扩张和抗炎的双重活性[2]。目前,TQC3721已开发吸入混悬液、吸入粉雾剂两种剂型。
TQC3721临床开发的第一种剂型为吸入混悬液,2项研究同时入选呼吸领域国际学术盛会。吸入混悬液给药途径稳定,对手口协调较差的老年患者更加便捷。在9月11日刚刚结束的欧洲呼吸学会国际大会(2024 ERS)上,TQC3721混悬液I期和II期临床研究摘要在线下和线上进行同步展示。多位研究者和海外潜在合作者对TQC3721获得的早期研究结果密切关注。

这两项研究评估了TQC3721吸入混悬液的安全性、耐受性、药代动力学特征和初步疗效,以及在中重度慢性阻塞性肺疾病患者中的有效性和安全性,其中一篇以最新重磅摘要(LBA)的形式入选。这些研究的开展,为公司后续临床开发奠定了坚实的基础。
本次TQC3721吸入粉雾剂获批临床,意味着产品研发迎来新的进展。吸入粉雾剂是一种药械结合的复杂剂型,开发难度较大。新剂型获批临床,有助于进一步满足COPD临床治疗的未尽需求。
呼吸领域是中国生物制药四大核心治疗领域之一,目前有8款创新候选药物处于临床及以上研发阶段。除TQC3721外,还包括TDI01(ROCK2抑制剂)、TQC2731(TSLP单抗)、TCR1672(P2X3受体拮抗剂)、TQH2722(IL-4R单抗)、TQC3927(MABA)等。ERS是世界上最大的呼吸医学专业学术会议,这是公司1类创新药研究数据首登该项国际大会,标志着中国生物制药在呼吸领域的研发创新取得重大进展。
参考文献:
[1] Global burden of chronic respiratory diseases and risk factors, 1990–2019: an update from the Global Burden of Disease Study 2019. eClinical Medicine 2023;59: 101936.
[2] Clmence Martin, Pierre-Rgis Burgel, Nicolas Roche ,Inhaled Dual Phosphodiesterase 3/4 Inhibitors for the Treatment of Patients with COPD: A Short Review,Int J Chron Obstruct Pulmon Dis. 2021; 16: 2363–2373.
声明:
1. 本新闻稿旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参阅,非广告用途。
2. 本公司不对任何药品和/或适应症作推荐。
3. 本新闻稿中涉及的信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医生或其他医疗卫生专业人士的意见或指导。
前瞻性声明:本新闻稿中包含若干前瞻性陈述,包括有关【TQC3721】的临床开发计划、临床获益与优势的预期、商业化展望、患者临床获益可能性,以及潜在商业机会等声明。“预期”、“相信”、“继续”、“可能”、“估计”、“期望”、“有望”、“打算”、“计划”、“潜在”、“预测”、“预计”、“应该”、“将”、“拟”、“会”和类似表达旨在识别前瞻性陈述,但并非所有前瞻性陈述都包含这些识别词。这些前瞻性陈述为公司基于当前所掌握的数据和信息所做的预测或期望,可能因受到政策、研发、市场及监管等不确定因素或风险的影响,而导致实际结果与前瞻性陈述有重大差异。请现有或潜在的投资者审慎考虑可能存在的风险,并不可完全依赖本新闻稿中的前瞻性陈述,该等陈述包含信息仅及于本新闻稿发布当日。除非法律要求,本公司无义务因新信息、未来事件或其他情况而对本新闻稿中任何前瞻性陈述进行更新或修改。
本文作者可以追加内容哦 !

