
9月13日,复星医药宣布,控股子公司复星医药产业拟现金出资2700万美元(约2亿元人民币)受让Kite Pharma持有的复星凯特50%的股权。本次转让完成后,复星医药将持有复星凯特100%的股权,并拟作为单一股东现金出资1000万美元或等值人民币对复星凯特进行增资。
于《股权转让协议》签订同日,复星凯特获得Kite Pharma许可于中国内地、香港和澳门(许可区域)及癌症治疗领域(许可领域)内独家开发、生产及商业化奕凯达及Brexu-cel(在研项目FKC889)的权利。
未来,复星医药与Kite Pharma将继续通过许可合作的模式保持长期战略合作伙伴关系。
与此同时,复星医药全资子公司复星凯特拟更名为复星凯瑞,并将作为复星医药细胞治疗技术的核心平台,持续聚焦肿瘤免疫治疗领域,推动CAR-T细胞治疗产品惠及更多患者,满足未被满足的临床需求。
复星医药执行总裁、复星凯特董事长张文杰表示:“未来,复星凯瑞将继续坚持以未满足的临床需求为中心,竭力推动CAR-T细胞治疗产品可及可愈、惠及更多患者,并积极探索与政府、行业各方合作的新模式,打造CAR-T生态圈,持续引领产业发展及升级。”
有趣的是,张文杰此前担任复宏汉霖首席执行官,复宏汉霖首度扭亏为盈后,2023年7月,复星医药聘任张文杰为公司执行总裁。
2024年4月公开信息显示,张文杰担任复星医药执行总裁、创新药事业部联席首席执行官,复宏汉霖执行董事、董事会主席,以及合营公司复星凯特董事长。
如今继复宏汉霖之后,复星系再填一家全资子公司复星凯特。
2024年6月,复星医药、复宏汉霖联合发布公告:由复星新药以吸收合并方式对复宏汉霖私有化。
01、中国第一款CAR-T疗法会第一个进国家医保吗?
复星医药在细胞基因疗法领域的前瞻性布局,似乎一直显得十分迅速。
2017年,全球首个CAR-T疗法在美国获批上市,意味着血液癌不再是无法治愈的绝症。
同年,复星凯特成立,这是复星医药与美国Kite Pharma(隶属于吉利德科学公司)的合资企业。
成立当年,复星凯特便从美国Kite Pharma引进了全球首款获批治疗特定非霍奇金淋巴瘤的CAR-T细胞药物Yescarta(FKC876),并迅速获批在中国开展注册临床试验。
2021年6月22日,复星凯特的阿基仑赛注射液Yescarta(商品名:奕凯达)在华获批,成为中国首个获批上市的CAR-T细胞治疗产品,用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者。
2023年6月,奕凯达新适应症获批,用于治疗一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤,也是当时国内唯一治疗该适应症的CAR-T疗法。
目前,奕凯达的第三项适应症的临床试验申请已在中国境内获批,目标人群为复发/难治性惰性非霍奇金淋巴瘤(r/r iNHL,包括滤泡性淋巴瘤和边缘区淋巴瘤)的成人患者。目前该项适应症于中国境内处于桥接临床试验阶段。
在推进产品临床试验的同时,复星也为其细胞基因疗法布局了从研发到生产的全价值链。
2019年1月,复星凯特1万平方米的CAR-T产业化生产基地在张江创新药产业基地启用。同年,其近2000平米的细胞治疗研发中心在上海揭牌。
细胞基因疗法虽然展现出惊人的疗效,但其价格也不断突破行业记录,也让普通患者闻之却步。目前在中国市场上,这类产品的价格普遍高达百万元人民币每针(且未进医保)。
鉴于此,自从奕凯达获批上市以来,复星凯特积极与商业保险公司合作,并推动定制化的城市保险计划。迄今为止,已在28个省区市建立了170多家奕凯达高标准治疗中心,并成功将奕凯达纳入超过110个城市的惠民保险项目以及超过80个商业健康保险计划,从而使细胞治疗这一创新疗法能够造福更多患者。
此外,复星凯特也是首个宣布其CAR-T疗法按疗效付费的企业。
今年1月,复星凯特宣布对使用CAR-T疗法治疗的患者采取按疗效付费的模式,患者购药并回输后3个月后进行疗效评估,如未能达到完全缓解(CR),患者可获得最高60万元返还。
即使如此,在中国实现药品放量的最大途径仍然是进医保。
根据最近公布的“2024年医保目录调整初审名单”,包括阿基仑赛注射液在内的四款中国CAR-T疗法已经成功入围。回顾四年前,奕凯达已率先通过了国家医保的初步形式审查,但最终未能参与谈判,这一事件曾引起广泛热议。
对于即将进行的医保谈判,复星医药的董事长吴以芳此前表示,他坚信这些产品应当被纳入医保,因为它们确实为患者带来了显著的价值。
而复星医药此次全资控股的举措,不禁让人揣测其是否旨在全力推动这些疗法进入医保范围。
02、政策利好,占据先机?
近年来,生命科学领域的竞争已上升到国家高度,比如此前:美国发布“生物技术和制造目标”时间表,“重塑”全球生物创新规则。
而近日,中国发布的一系列政策也利好众多细胞基因疗法企业、机构,甚至包括外资。
9月8日,商务部、国家卫生健康委、国家药监局三部门发布《关于在医疗领域开展扩大开放试点工作的通知》。
在中国(北京)自由贸易试验区、中国(上海)自由贸易试验区、中国(广东)自由贸易试验区、海南自由贸易港允许外商投资企业从事人体干细胞、基因诊断与治疗技术开发和技术应用,以用于产品注册上市和生产
9月11日,上海市发布2024年度“科技创新行动计划”细胞与基因治疗专项项目申报指南。
项目网上填报起始时间为2024年9月20日9:00,截止时间(含申报单位网上审核提交)为2024年10月15日16:30。
执行期限:2024年12月1日至2027年11月30日。
申报要求之一是,项目申报单位应当是注册在本市的法人或非法人组织,具有组织项目实施的相应能力。
03、最强对手来势汹汹复星需全力以赴
2023年,阿基仑赛注射液Yescarta全球销售额14.98亿美元,是全球最畅销的CAR-T疗法。
复星医药财报提到2023上半年阿基仑赛注射液在中国卖出了1亿元以上。
2023全年累计惠及超过600位中国淋巴瘤患者。
截至目前,中国已有六款CAR-T疗法获批。
除了阿基仑赛注射液,还有:药明巨诺的瑞基奥仑赛注射液(2024上半年销售额8680万元,同比下降1%)、驯鹿生物/信达的伊基奥仑赛注射液、合源生物的纳基奥仑赛注射液、科济药业的泽沃基奥仑赛注射液,以及8月27日刚刚获批的传奇生物的西达基奥仑赛注射液。
因数据披露不完整,目前尚无法确定哪种CAR-T疗法在中国市场销量最佳。但是传奇生物的西达基奥仑赛注射液无疑将是复星的最强竞争对手。
2024上半年,西达基奥仑赛销售额3.43亿美元(约24.4亿元),+81.5%,主要由美国市场贡献;传奇生物合作伙伴强生预测今年西达基奥仑赛销售额有望成为第二款中国“10亿美元分子”。
此外,复星凯特的盈利之路依然任重而道远。
据复星医药公告,2023年复星凯特实现了2.4亿元的营收,但净亏损达到了3.5亿元。
此次控股事件,也不禁让人联想到复星医药之前的一项创新药资产——复宏汉霖。在复星医药集团的支持下,复宏汉霖成功跻身于首批实现扭亏为盈的创新药企之列。
2023年,复宏汉霖的净利润达到了5.46亿元,首次实现了全年盈利;相比之下,2022年其亏损额高达6.95亿元。而2024年6月,复星医药即宣布将通过吸收合并的方式对复宏汉霖进行私有化
在全球大健康企业纷纷追求精简和专注之际,复星医药似乎选择了一条独特的“大而全”道路。从复星医药目前的版图来看,主打一个包罗万象。
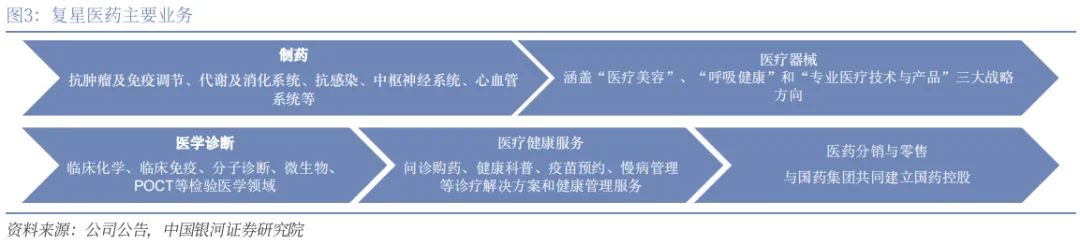
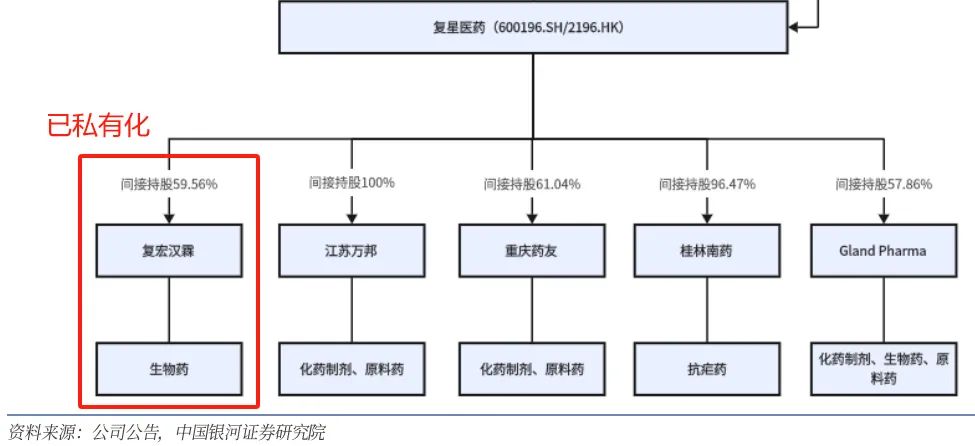
然而,越来越多的资产似乎并未对其业绩产生积极影响。
2024年上半年,复星医药营收204.63亿元,同比下降了4.36%(若不计新冠相关产品,营收实际同比增长5.31%)。此外,归母净利润12.25亿元,同比下降31.09%。
截至13日收盘,复星医药的股价下跌了0.76%,这表明市场可能只有在业绩出现上升时才会真正感到满意。
本文作者可以追加内容哦 !

