2024欧洲肿瘤内科学会(ESMO)年会于9月13-17日在西班牙巴塞罗那盛大召开。作为肿瘤领域最具权威的年度盛会之一,本届年会云集全球肿瘤大咖、汇聚领域最新进展。随着我国泌尿肿瘤领域相关研究的不断发展,越来越多的中国研究亮相国际舞台。其中,中国原研抗体偶联药物(ADC)维迪西妥单抗联合免疫治疗局部晚期或转移性尿路上皮癌(la/mUC)的两项研究——RC48-C014研究和RC48-G001研究Cohort C数据重磅公布(摘要号:1979P,1967MO),引发全球学者热烈讨论。值此契机,医脉通特邀北京大学肿瘤医院郭军教授和盛锡楠教授为我们解读这两项研究,并探讨相关结果对尿路上皮癌(UC)临床实践的影响以及未来的探索方向。
医脉通:维迪西妥单抗作为靶向HER2的ADC药物,在UC领域不断取得突破,您如何看待HER2在帮助筛选可能的获益最大化人群、制定精准治疗决策的价值?您如何评价维迪西妥单抗在HER2表达全人群的获益?

郭军教授
在本次ESMO大会上,我们报告了RC48-C014研究的更新数据,本项研究并未对患者进行HER2表达水平的筛选,HER2 IHC 0/1+/2+/3+的患者均被纳入了研究。令人欣喜的是,维迪西妥单抗联合免疫在HER2表达全人群(IHC 1+/2+/3+)中展现了一致的获益,甚至在HER2表达为0的患者中,维迪西妥单抗联合免疫依然能够达到33.3%的ORR,这一发现既出乎意料,又在情理之中,突显了维迪西妥单抗的治疗价值。

盛锡楠教授
HER2是人表皮生长因子受体(EGFR)家族中的一员,在多肿瘤的发生发展中发挥关键作用,是抗肿瘤治疗的重要靶点。UC是HER2表达排名第三的瘤种,过去我们研究了多种抗HER2的治疗方案如单克隆抗体和酪氨酸激酶抑制剂(TKI)等,但未能取得重大进展。直至近年来,以维迪西妥单抗为代表的靶向HER2的ADC问世,UC的抗HER2治疗才迎来重大突破。与此同时,我们也逐渐认识到HER2作为UC的重要生物标志物,在患者分层和指导精准治疗决策方面具有重要价值。随着临床研究的深入和数据的积累,我们应当把HER2表达的UC患者视作独立的人群来看待。我们甚至可以大胆推测,基于生物标志物的表达、生物学特性以及治疗手段的差异,未来我们很有可能将HER2有表达的UC患者作为独立的亚型来治疗。
既往临床研究显示,维迪西妥单抗在HER2低表达(IHC 1+)的人群中也达到了较高的客观缓解(ORR),随着HER2表达水平的升高,维迪西妥单抗的疗效也更佳。此次RC48-C014研究公布的最新数据显示,即使在HER2低表达(IHC 1+)的患者中, ORR仍能达到64.3%;值得注意的是,在HER2表达为0的患者中,ORR仍超过30%。究其原因,一方面UC的HER2表达存在较高的异质性,虽然部分患者当下的HER2表达检测结果为0,但实际上可能仍然存在确切的HER2表达;另一方面,从ADC药物的作用机制来看,细胞毒药物与靶向HER2的单克隆抗体进行了偶联,因此即便HER2低表达人群也能从维迪西妥单抗的治疗中获益。在临床实践中,需要根据HER2表达水平对患者进行分层以制定相应的治疗策略。对于HER2过表达的患者,应当将抗HER2 ADC药物作为首选;而对于HER2低表达的患者,抗HER2 ADC药物联合免疫治疗也许是更优的选择。靶向HER2的精准治疗是UC领域的重要研究方向,未来我们需要进一步开展更多的临床研究和基础转化研究,深入理解HER2在UC中的作用机制并优化患者筛选和分层治疗策略。
医脉通:本次ESMO大会公布了RC48-C014研究和RC48-G001研究Cohort C的更新结果,报告了迄今为止晚期UC一线治疗领域的最长OS和最高ORR数据,您如何评价维迪西妥单抗这一长期和短期疗效结果,以及将如何影响和改变中国的临床实践?

郭军教授
国内对于ADC联合免疫治疗晚期UC的研究几乎与国际同期迈进,早在三年前的ASCO年会上,我们就首次披露了RC48-C014研究的初步结果,本次ESMO大会上又更新了长期随访结果。近三年随访数据显示,维迪西妥单抗联合免疫治疗晚期UC的ORR达75%,中位OS达33.1个月,这是迄今为止晚期UC一线治疗领域报道的最高ORR和最长OS数据。在RC48-C014研究的基础上,我们又开展了首个大型III期随机对照临床试验RC48-C016研究,旨在评估维迪西妥单抗联合免疫对比化疗在晚期UC一线治疗中的疗效与安全性。目前该研究已经完成全部入组,正在随访中,初步结果令人欣喜。目前中国临床肿瘤学会尿路上皮癌(CSCO-UC)诊疗指南中,晚期一线治疗推荐仍以化疗为主,相信明年RC48-C016研究最终结果公布将为未来的UC抗HER2治疗策略提供坚实依据,维迪西妥单抗联合免疫必将改变我国UC领域治疗格局,成为晚期一线治疗的首选方案,进而深刻影响和改变中国临床实践。

盛锡楠教授
今年ESMO大会上,我们欣喜地见证了抗HER2 ADC治疗在UC领域取得的重大突破。自2016年我们在国内启动抗HER2 ADC治疗的研究以来,至今已有近8年的历程。在此期间,我们开展了大量的研究工作,其中包括两年前启动的维迪西妥单抗联合免疫治疗晚期UC的RC48-C014研究。从最终的生存随访数据来看,尽管研究入组的41例患者中有16例是二线患者,全人群的ORR仍然高达75%,一线患者的ORR更是高达79.2%,中位OS达33.1个月,这一结果优于去年ESMO大会上公布的EV-302研究数据。值得一提的是,这也是抗HER2 ADC联合免疫治疗在UC领域首次公布的长期随访数据,具有重要的里程碑意义。
维迪西妥单抗联合免疫的疗效在欧美人群中是否存在差异?今年ESMO大会上来自美国的M.Galsky教授报告了RC48-G001研究Cohort C的结果。该研究共纳入20例患者,评估了维迪西妥单抗联合免疫在既往未经治疗的HER2有表达(IHC 1+/2+/3+)的UC患者的疗效。结果显示,ORR同样达到了75%,其中完全缓解率(CR)高达35%。这一结果不仅证实了维迪西妥单抗在西方人群中的疗效,也进一步佐证了中国方案中国策略的合理性以及研究结果的可重复性。随着这一数据的公布,维迪西妥单抗联合免疫用于HER2有表达(IHC 1+/2+/3+)的UC患者的治疗策略将受到更多国际关注,有望推动更多相关临床研究的开展,增强国内同道对中国原研药物及临床研究水平的信心。
医脉通:ADC药物在UC中的应用突飞猛进,不断改变晚期UC整体治疗格局,随着国内更多ADC药物的可及,请结合您的临床经验谈谈如何帮助患者选择更强效、更安全、更适合的个体化治疗策略?

盛锡楠教授
ADC是近年来晚期UC药物治疗领域的研究热点,也是未来有望改变临床实践的重要方向。ADC药物在国内外UC诊疗指南的晚期一线和后线治疗推荐中均占据着重要地位,不仅如此,对于ADC的临床探索正逐步前移至新辅助、围术期等治疗阶段。多种ADC药物已在国内获批,针对新靶点的ADC药物也在持续研发中,取得了可喜的初步结果。但随着越来越多的ADC药物在国内可及,临床医生往往也面临着药物选择的困惑。对此,毫无疑问我们应首先基于临床研究数据来进行选择。从现有的临床数据来看,Trop2靶点的ADC药物相较其他靶点似乎处于疗效相对劣势的地位。其次,靶点分子的检测是ADC药物重要的选择因素,过去我们认为维恩妥尤单抗是一个无需进行靶点检测的药物,然而今年ESMO大会关于EV-302研究的分层数据显示,Nectin4低表达患者在疗效数据上还是略差于高表达患者。同时维迪西妥单抗的多项临床研究也证实了HER2表达越高,疗效越好。因此,靶点检测将成为ADC药物选择的重要考量因素,若患者Nectin4低表达而HER2高表达,那么毫无疑问应当首选抗HER2 ADC药物如维迪西妥单抗;若两者均为高表达,则需要综合考虑药物的可及性和经济性来做出选择。HER2检测已成为国内UC领域的常规医疗工作,随着更多需要进行靶点检测的ADC药物可及,不同的靶点都应考虑进行检测以支持制定治疗决策。综上,在未来ADC药物的选择中,临床研究数据、靶点的表达水平、药物的可及性和经济性将是核心的考量因素。
医脉通:ADC联合免疫治疗的新模式持续引领UC领域的研究发展,为治疗时机前移奠定了坚实的基础,结合我国临床实际需求,您认为维迪西妥单抗未来还有哪些值得期待的探索方向?

郭军教授
维迪西妥单抗是我国最早获批用于治疗UC的ADC药物,不仅在晚期治疗中展现出卓越的疗效,还在新辅助治疗领域表现出了显著的应用潜力。因此,未来除了晚期UC,我们还需要关注ADC药物在新辅助治疗阶段的研究探索和应用。
在今年6月的ASCO大会上,我们报道了维迪西妥单抗联合免疫用于新辅助治疗的RC48-C017研究数据,结果显示,联合方案治疗的患者病理部分缓解率(pPR)达74.2%,病理完全缓解率(pCR)达61.3%,这意味着近2/3的患者在治疗完成后的病理检查中未发现残留的肿瘤组织。这一结果引发了我们对未来治疗模式的深入思考。随着新辅助治疗的发展,手术在UC治疗中的地位可能会逐渐下降,甚至在未来,部分患者在接受新辅助治疗后,可能无需再进行手术转而成功实现保留膀胱,也能获得比现有的“先手术后辅助”这一治疗模式更好的效果。这不仅简化了治疗流程,还提升了治疗效果和患者生活质量,使患者获益最大化。期待未来UC领域能够涌现出更多有效的治疗手段和先进的治疗理念,造福更多患者。

盛锡楠教授
随着国内外对抗HER2 ADC药物研究的不断深入,我们发现仍有一些疑问亟待探索。首先,HER2表达在原发灶和转移灶之间、不同脏器之间可能存在差异,因此我们需要明确HER2表达的异质性,以便更准确地评估HER2表达水平,进而指导治疗决策。其次,在疗效探索方面,RC48-C017研究已经证实了维迪西妥单抗在新辅助治疗的获益,超过60%的患者达到了pCR,未来我们可以进一步探索其在保膀胱治疗中的应用价值。同时,ADC药物与免疫治疗的联合疗法已经展现出良好的效果,未来我们还可以验证多种ADC联合用药是否能够进一步提升疗效。此外,随着ADC药物种类的不断增加,如何合理地排兵布阵、序贯治疗也是一个重要的研究方向。随着以维迪西妥单抗为代表的ADC药物在UC治疗中的价值日益凸显,相关研究工作也在不断开展。未来的研究方向将更加多元化,必将进一步拓展和优化ADC的临床应用,从而惠及更多UC患者。
1979P :一项维迪西妥单抗(DV)联合特瑞普利单抗(T)用于不可切除的局部晚期或转移性尿路上皮癌(la/mUC)的Ib/II期研究的长期结果
研究背景
含铂化疗作为局部晚期或转移性尿路上皮癌(la/mUC)一线标准治疗方案的疗效不尽如人意,中位无进展生存期(PFS)和总生存期(OS)分别为6.3个月和16.1个月。维迪西妥单抗(一种靶向HER2的ADC药物)联合特瑞普利单抗(一种PD-1抑制剂)展现了高肿瘤缓解(ORR率73.2%)和长生存获益(中位PFS为9.2个月,2年OS率为63.2%),数据截至2022年11月18日,当时OS数据尚不成熟。本次报告包含OS和其他结局在内的更新结果,随访时间截至2024年3月1日。
研究方法
RC48-C014是一项研究者发起的评估维迪西妥单抗联合特瑞普利单抗治疗la/mUC的安全性和疗效的Ib/II期研究(NCT04264936)。
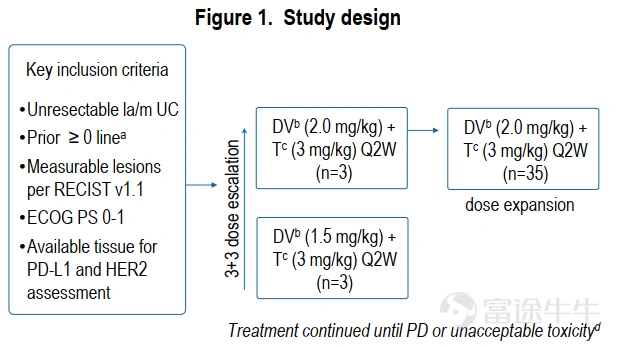
研究终点
主要终点:不良事件
次要终点:ORR,PFS,OS和药代动力学
本研究的数据截止日期:2024年3月1日
研究结果
研究共入组41例患者;中位年龄66岁(42-76),男性占比53.7%,ECOG评分为1的患者占比70.7%。17例(41.5%)患者肺转移,10例(24.4%)患者肝转移。
数据截至2024年3月1日,39例(95.1%)患者暂停治疗,主要因为疾病进展(61.0%)和不良事件(14.6%)。
抗肿瘤活性:
在至少完成一次基线后肿瘤评估的40例患者中,研究者根据RECIST v1.1标准评估的确认的ORR为75.0%(95% CI:58.8-87.3)。
中位缓解持续时间为8.6个月(95% CI:7.2-16.8)。
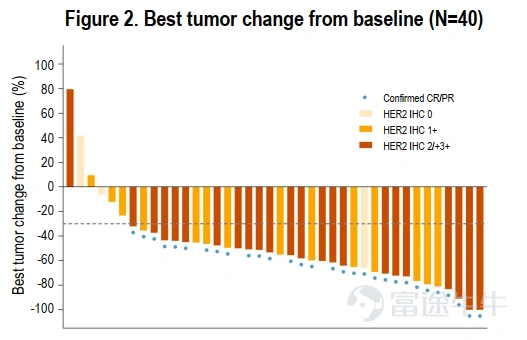
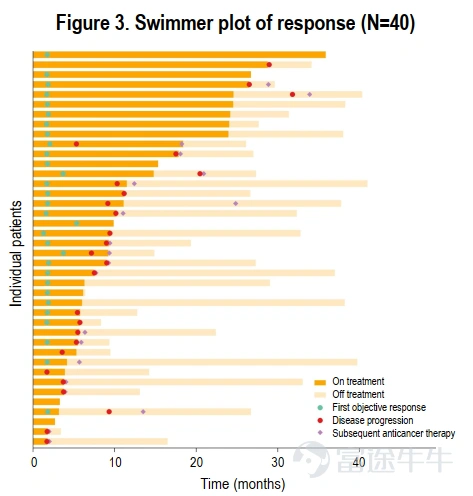
亚组分析:
无论先前的系统治疗的线数、HER2表达(IHC 1+/2+/3+)和PD-L1表达状态,ORR的亚组分析都展现了一致的获益。
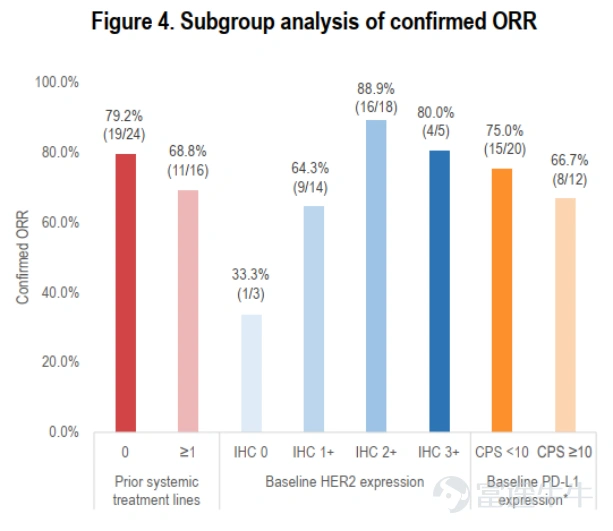
*8位没有PD-L1表达状态的患者,其cORR为87.5%
PFS
根据研究者的评估,所有患者的中位PFS为9.3个月(95% CI: 5.7-11.2)。
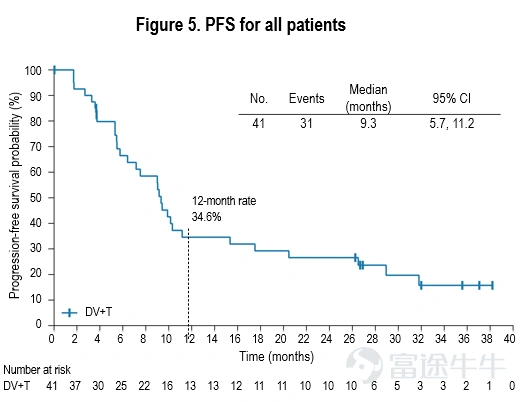
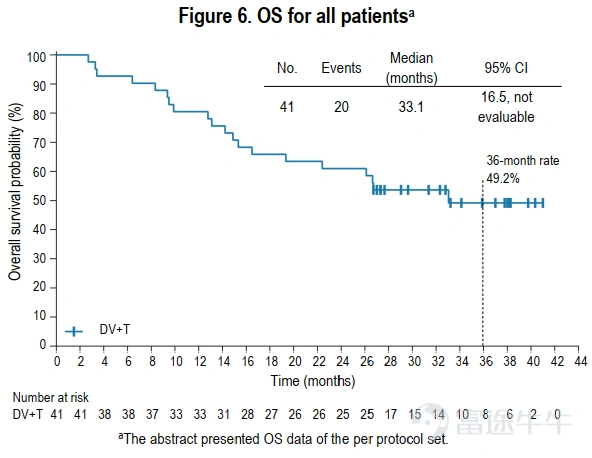
OS
中位随访时间33.2个月(95% CI:29.0-37.8),全人群的中位OS是33.1个月(95% CI:16.5-NE)。
安全性
安全性和之前报告的一致。
21例(51.2%)患者发生了≥3级的TRAE,最常见的不良事件是-谷氨酰转移酶升高(12.2%),乏力(9.8%),丙氨酸氨基转移酶升高(7.3%),高甘油三酯血症(7.3%),血糖升高(7.3%),肺炎(4.9%)、天门冬氨酸转氨酶升高(4.9%)、血肌酸磷酸激酶升高(4.9%)和中性粒细胞计数降低(4.9%)。
研究结论
长期随访结果证实了维迪西妥单抗联合特瑞普利单抗的高肿瘤缓解率、显著的OS获益和可控的安全性,支持维迪西妥单抗联合特瑞普利单抗作为一种有前景的方案治疗la/mUC患者。
1967MO:维迪西妥单抗联合帕博利珠单抗在未经治疗的HER2有表达的局部晚期或转移性尿路上皮癌中的初步疗效和安全性:RC48-G001研究Cohort C
研究背景
维迪西妥单抗改变了既往未经治疗的局部晚期或转移性尿路上皮癌(la/mUC)的治疗格局。研究表明约60%-80%的尿路上皮癌患者HER2有表达。维迪西妥单抗(DV,RC48-ADC)是一种研究中的抗体偶联药物,包含了完全人源化的靶向HER2的迪西妥单抗,通过蛋白酶可裂解连接子mc-vc与MMAE进行偶联。和其他基于迪西妥单抗的抗体偶联药物类似,维迪西妥单抗在靶向肿瘤细胞内释放MMAE后介导免疫原性细胞凋亡,为维迪西妥单抗与免疫检查点抑制剂的联合应用提供了理论依据。维迪西妥单抗还通过旁观者效应增强了抗肿瘤活性,其中维迪西妥单抗释放的细胞内的MMAE可以扩散并穿过细胞膜并在相邻的细胞中引起细胞凋亡。
维迪西妥单抗联合PD-1抑制剂如特瑞普利单抗,既往在la/mUC患者中已展现了令人鼓舞的抗肿瘤活性和可控的安全性。此次我们报告了在未经治疗的HER2有表达的la/mUC患者中进行的开放标签、II期、多中心的RC48-G001研究(NCT04879329)的安全性导入期(Part1)的队列C(维迪西妥单抗+帕博利珠单抗) 的初步疗效和安全性结果。
研究设计和方法
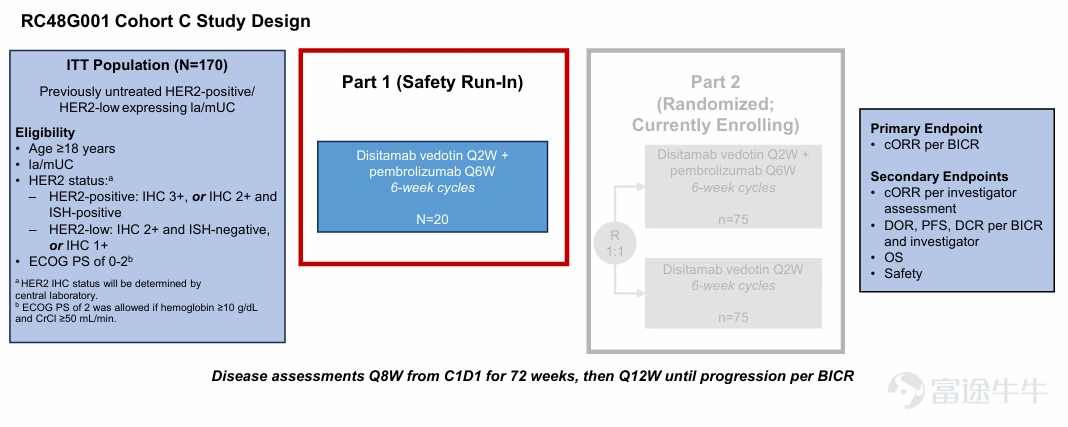
研究结果
基线特征,患者分布和暴露
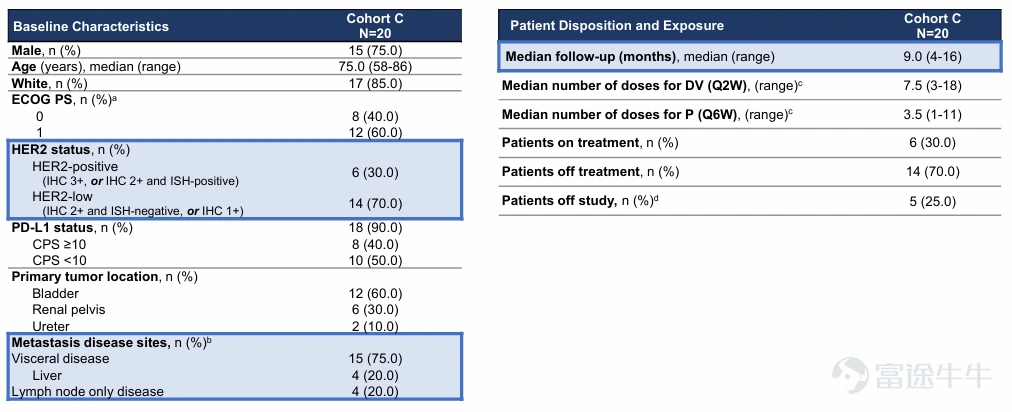
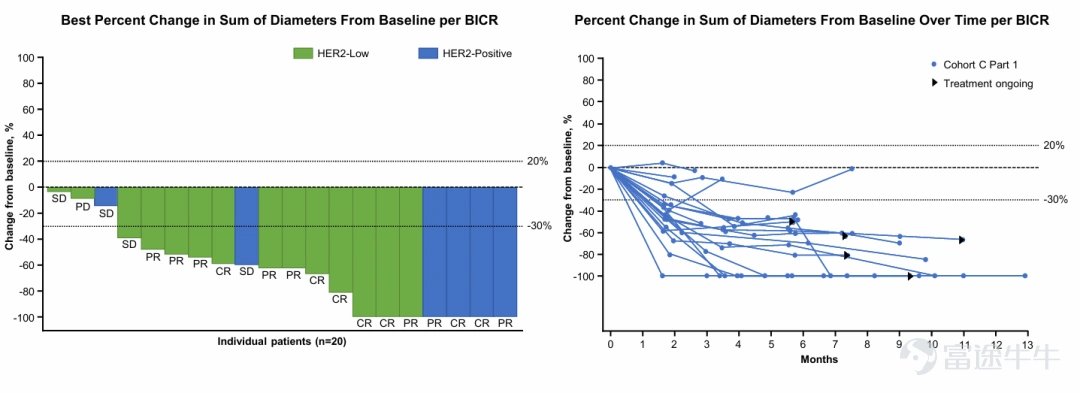
BICR确认的ORR
HER2过表达和HER2低表达的患者均对维迪西妥单抗联合帕博利珠单抗产生应答。

BICR评估的直径总和较基线的百分比变化
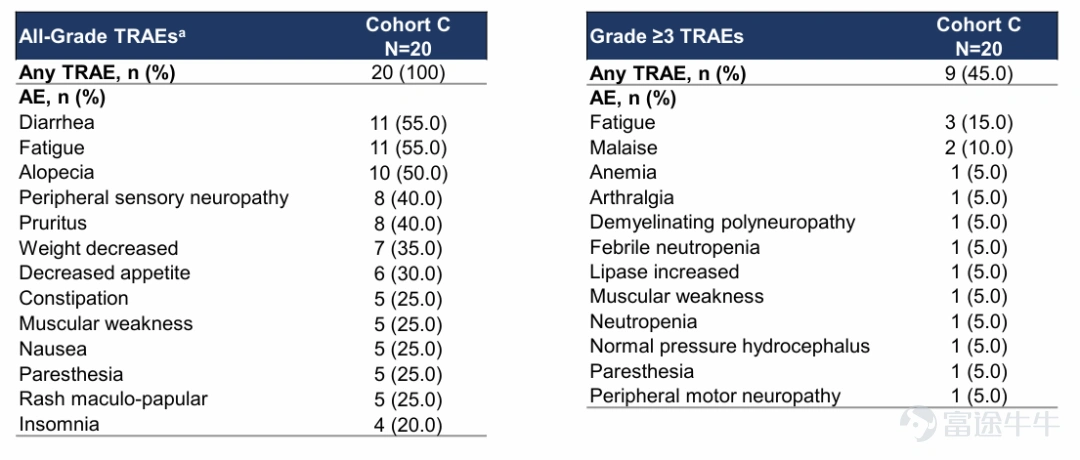
维迪西妥单抗联合帕博利珠单抗的不良事件
维迪西妥单抗和帕博利珠单抗的剂量调整、延迟给药和剂量降低
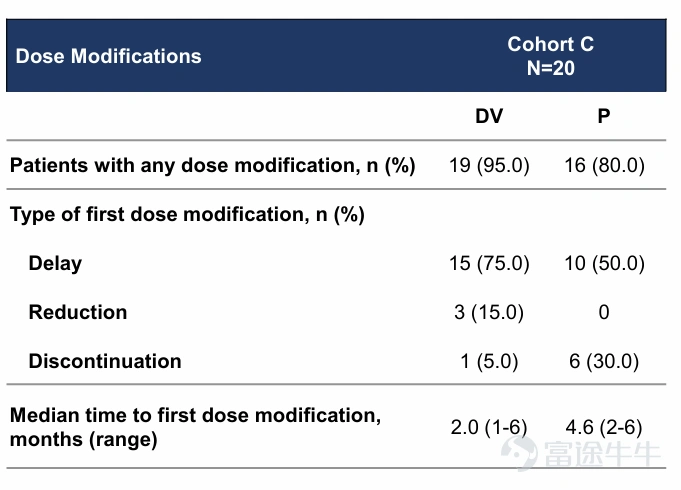
最常见的导致剂量延迟的TEAE如下:
维迪西妥单抗(≥10%):周围感觉神经病变、食欲下降、疲劳和感觉异常。
帕博利珠单抗(≥5%):贫血、食欲下降、疲劳、发热性中性粒细胞减少症、脂肪酶增加和瘙痒。
最常见的导致剂量降低的TEAE如下:
维迪西妥单抗(≥10%):周围感觉神经病变、食欲下降和疲劳。
最常见的导致治疗中止的TEAE如下:
维迪西妥单抗(≥5%):脱髓鞘性多发性神经病变、正常压力脑积水、感觉异常、周围运动神经病变和尿脓毒症。
帕博利珠单抗(≥5%):脱髓鞘性多发性神经病变、正常压力脑积水、周围运动神经病和尿脓毒症。
研究结论
维迪西妥单抗联合帕博利珠单抗在未经治疗的HER2有表达的la/mUC患者中表现出了令人鼓舞的初步抗肿瘤活性。15例患者(75%)达到经BICR确认的ORR,7例患者(35%)达到CR 。中位DOR未达到。维迪西妥单抗联合帕博利珠单抗在HER2过表达和HER2低表达的la/mUC患者中均产生应答。维迪西妥单抗联合帕博利珠单抗具有可控的安全性,与既往维迪西妥单抗单药研究中的结果一致。研究中未观察到治疗相关的5级不良事件。
目前正在一项III期研究评估维迪西妥单抗联合帕博利珠单抗在一线治疗中与化疗对比的疗效和安全性(SGNDV-001; NCT05911295);正在并计划在北美、拉丁美洲、欧洲、澳大利亚和亚洲入组患者。
专家简介

郭军 教授
– 北京大学肿瘤医院主任医师,教授,博士生导师
– 北京大学肿瘤医院黑色素瘤与肉瘤内科主任
– 北京大学肿瘤医院泌尿肿瘤内科主任
– 中国临床肿瘤学会(CSCO)副理事长兼秘书长
– 国际黑色素瘤协会(MWS)副主席
– 欧洲肿瘤内科学会(ESMO)黑色素瘤与皮肤肿瘤分会主席
– 国家癌症中心国家肿瘤质控中心黑色素瘤专委会主任委员
– CSCO黑色素瘤专家委员会主任委员
– CSCO肾癌专家委员会副主任委员
– CSCO免疫治疗专委会副主任委员
– CSCO尿路上皮癌专委会副主任委员
– CSCO前列腺癌专委会副主任委员
– CFDA国家药品注册评审专家
– 国家卫生计生委合理用药专家委员会委员(抗肿瘤用药专业组)

盛锡楠 教授
– 北京大学肿瘤医院主任医师,教授,博士生导师
– 北京大学肿瘤医院泌尿肿瘤内科副主任
– 中国抗癌协会泌尿生殖肿瘤整合康复专业委员会副主任委员
– 中国抗癌协会泌尿系统肿瘤专业委员会常委
– 中国临床肿瘤学会(CSCO)理事
– 中国临床肿瘤学会肾癌专家委员会常委兼秘书长
– 中国临床肿瘤学会尿路上皮癌专家委员会常委
– 国家肿瘤质控中心膀胱癌质控专家委员会委员
– 北京肿瘤防治研究会泌尿肿瘤分委会候任主任委员
– 北京抗癌协会泌尿生殖肿瘤专委会青委会主任委员
– 北京医学会肿瘤分会常委
本文作者可以追加内容哦 !

