一石激起千层浪。
百时美施贵宝(BMS)手里的一把价值百亿美元的锋利宝剑,终于出鞘了:9月26日,KarXT获FDA批准上市,成为数十年来首个获批的全新机制的精神分裂症治疗药物。
KarXT是BMS在2023年12月斥资140亿美元收购Karuna而获得的潜在超级大药,Evaluate预期其2030年销售额有望达到31亿美元。
这对于拳头产品面临专利悬崖、渴求新产品补缺的BMS,无疑将是摆脱困境的一次重大转折。更值一提的是,这还不是BMS未来带给市场的唯一惊喜。
01
宝剑出鞘
“宝剑出鞘时,所向披靡日。”所有药企都希望自家新药能成为横扫市场的锋利宝剑,BMS亦不例外。
被寄予厚望的KarXT,会是那把所向披靡的锋利宝剑吗?
“数十年来用于治疗精神分裂症的首个新机制药物”,是KarXT身上最大的标签。这既凸显了KarXT在创新性上的里程碑突破,也反映了其蕴含巨大的市场价值。
不同于传统的抗精神病药主要靶向多巴胺受体,KarXT的作用机制新颖,不直接阻断多巴胺受体,是一款非靶向多巴胺能与5-羟色胺能信号通路的口服M1/M4型毒蕈碱乙酰胆碱受体激动剂。
临床研究显示,在所有3项安慰剂对照研究中,KarXT都达到了主要终点,显著改善了精神分裂症患者的阳性和阴性症状,尤其与现有抗精神病药的常见副作用(包括体重增加、嗜睡和运动障碍)无关。
今年4月,BMS披露了EMERGENT-4试验长期数据中期分析结果:在52周时,KarXT能显著改善精神分裂症患者所有症状的疗效指标。根据阳性和阴性综合征量表(PANSS)总分,超过75%的参与者在一年内症状比基线改善了30%以上。
在长期试验中,KarXT还展现出良好的长期代谢特征,大多数受试者在临床研究过程中体重减轻,一年内平均体重减轻2.6公斤。这意味着,相比于传统的抗精神病药物,KarXT展现出了独特的疗效和安全性。

除精神分裂症外,KarXT还在开发用于治疗阿尔茨海默病。两项适应症都是长期存在且治疗需求迫切的疾病领域。
据统计,全球约有2100万精神分裂症患者,5500万阿尔茨海默病患者,并且还在持续增长。然而,目前市场上缺乏兼具疗效和安全性的新型药物。
基于种种因素,行业媒体Evaluate在2024年制药行业展望报告中预测,KarXT为目前按净现值计算的前10大最有价值管线,2030年销售额有望达到31亿美元。华尔街分析师甚至认为,KarXT巅峰时期的年销售额将超过100亿美元。
值得一提的是,再鼎医药拥有KarXT在大中华区的权益,目前正在国内开展评估KarXT用于精神分裂症的Ⅲ期桥接注册临床研究,并已完成所有国内患者的入组,有望于2025年上半年提交新药上市申请。
今年5月,Karuna公司等在中国启动了一项评价KarXT治疗阿尔茨海默病相关的精神行为症状的国际多中心(含中国)Ⅲ期临床研究。再鼎医药表示,将在大中华区加入KarXT针对阿尔茨海默病相关的精神疾病的全球Ⅲ期研究。
02
横刀立渊
从豪掷140亿美元收购就能看出,KarXT被BMS寄予了厚望。
当前,许多跨国制药巨头都面临同样的困境:拳头产品遭遇专利悬崖(仿制药的威胁)导致销售增速下滑。
尤其是BMS。根据交银国际研报披露,全球头部MNC药企中,BMS所承受的专利悬崖风险敞口最大,已到期和未来三年内将到期品种的销售占2023年总收入的68%。
BMS有三大拳头产品:血液学疾病业务的Revlimid(来那度胺)、肿瘤业务的Opdivo(纳武利尤单抗)、心血管疾病业务的Eliquis(阿哌沙班),2023年销售额分别达到60.97亿美元、100.31亿美元、122.06亿美元。
其中,Revlimid曾是百亿美元级的“超级重磅炸弹”,但随着核心专利于2019年到期,2023年的销售已跌至峰值的一半以下;PD-1单抗Opdivo在2023年首次突破百亿美元大关,为公司贡献了两成收入,但专利即将在2028年到期,意味着高光时刻要且行且珍惜了。
尤其是支柱产品Eliquis,近年来销售增长已明显乏力,加之化合物专利和制剂专利将分别于2026年和2031年到期,最早2028年就有Eliquis仿制药在美国上市。更糟糕的是,由于美国实施医保谈判,Eliquis还将于2026年进行价格调整。
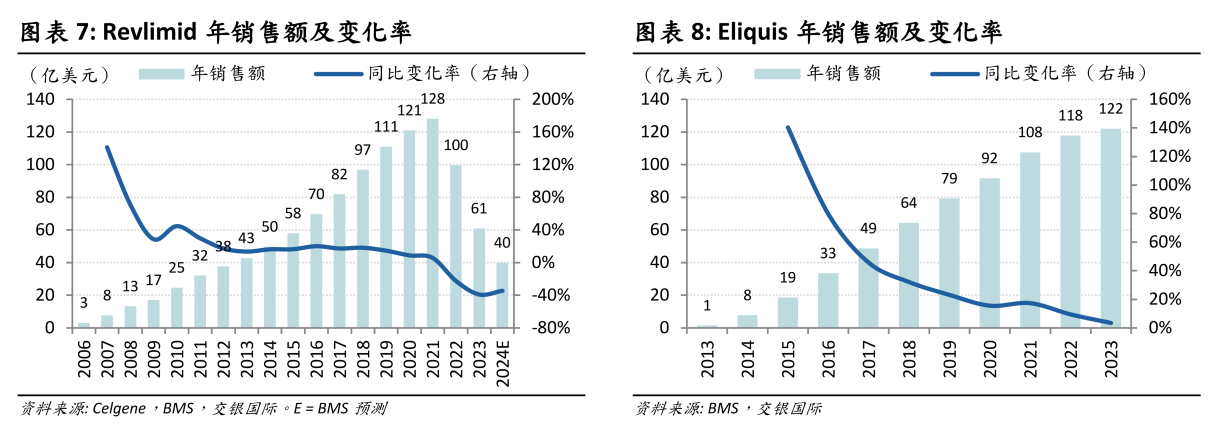
专利悬崖的严峻挑战,如同让BMS站在了深渊的峭壁之上。
为此,BMS毅然决然地选择了横刀立渊:斥重金并购和引进高潜力新产品,在各个疾病领域广纳博收、积蓄力量,从而填补缺口、摆脱困境。
斥资140亿美元收购而来的KarXT,只是其中一把锋利宝剑。BMS要实现的“星辰大海”,是在多个疾病业务全面开花,实现“八方来财”。
例如,在血液学领域,BMS豪掷740亿美元收购血液巨头新基制药,将Revlimid和Pomalyst(泊马度胺)收入囊中,其中泊马度胺是专利过期药物Revlimid的接棒产品。
在心血管领域,BMS斥资131亿美元收购MyoKardia,拿下了治疗阻塞型肥厚性心肌病的Mavacamten,之后又以3.5亿美元从联拓生物收回了Mavacamten在中国、新加坡等多个市场的权益。
尤其在肿瘤领域,BMS大额交易频现:以41亿美元收购Turning Point,拿下第四代ALK抑制剂Repotrectinib,以超10亿美元引进Tubulis公司的差异化ADC偶联技术平台,以48亿美元收购Mirati拿下KRAS G12C抑制剂Krazati等多款肿瘤产品,以总额84亿美元引进百利天恒HER3/EGFR双抗ADC药物BL-B01D1。
BMS的触手还延伸到自免领域,今年4月以超18亿美元引进Repertare用于治疗自免疾病的疫苗。
除了广泛布局多个疾病业务,BMS还实施了裁员计划,目标到2025年底前节省15亿美元的成本,同时优化管线,将资源集中到“最适合开发的资产”上。
03
海阔天空
自2019年以来,为了搜罗高潜力的潜在大药以及巩固MNC巨头的地位,BMS砸下了上千亿美元的真金白银,足见其雄心和决心。
重金之下,丰富管线已成。各个疾病业务摩拳擦掌,有望带来可观的收入。这也预示着BMS正在迎来“海阔天空”。
例如,血液学疾病业务的泊马度胺,近几年销售额保持在30亿美元左右;心血管疾病业务的Mavacamten,BMS预计其销售峰值将在2029年达到40亿美元。
其中,Mavacamten是MyoKarida研发的第一代心肌肌球蛋白抑制剂,于2022年4月获FDA批准用于治疗症状性纽约心脏协会(NYHA)心功能II-III级的梗阻性肥厚型心肌病(oHCM)成人患者,之后又分别于2023年6月、2024年5月在欧盟、中国获批上市。
HCM市场患者数量多且治疗药物获批较少,存在巨大未被满足的临床需求。据C司统计,仅美国就有大约68万-108万名HCM患者,其中三分之二为oHCM;中国估计约有110万至280万HCM患者。
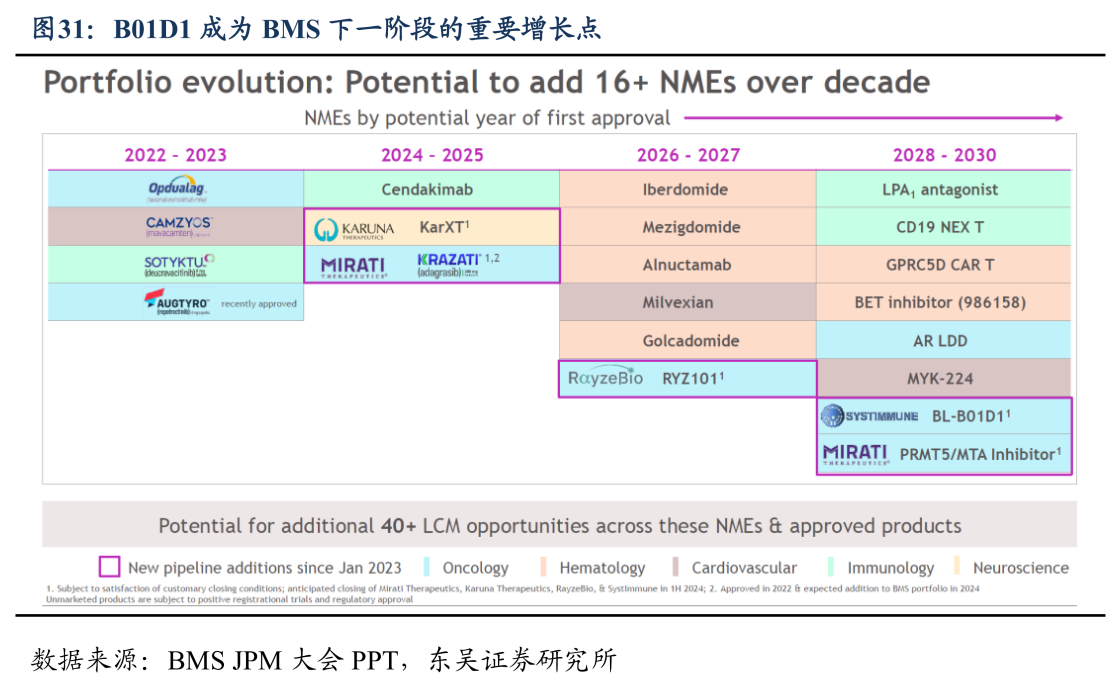
肿瘤业务也颇具看点,Repotrectinib(瑞普替尼)是第四代ALK抑制剂,主要靶向ALK、ROS1和NTRK等基因突变,也是一种不限癌种的靶向药。
目前,Repotrectinib已获FDA批准两项适应症:用于治疗ROS1阳性非小细胞肺癌成年患者,以及用于患有以下实体肿瘤的成人和12岁及以上的儿童患者:具有神经营养酪氨酸受体激酶(NTRK)基因融合,局部晚期或转移性,或手术切除可能导致严重发病率,并且治疗后病情进展或没有令人满意的替代疗法。
值得一提的是,再鼎医药拥有Repotrectinib在大中华区的权益,目前NMPA已批准其用于治疗ROS1阳性NSCLC患者。
重磅KRAS G12C抑制剂Krazati,目前已获FDA批准两项适应症,包括用于治疗携带KRAS G12C突变的经治NSCLC患者,以及与西妥昔单抗联合使用,治疗经FDA批准的检测确定为KRAS G12C突变的局部晚期或转移性结直肠癌(CRC)成年患者。
目前,Krazati及其联合疗法还在开发用于晚期结直肠癌、及其他实体瘤的临床试验,并展现出积极疗效。此外,再鼎医药也拥有Krazati在大中华区的权益。
备受关注的还有百利天恒的HER3/EGFR双抗ADC药物BL-B01D1,目前正在开展7个III期临床,覆盖肺癌、乳腺癌、鼻咽癌等多个癌种,而且还具有与O药等免疫疗法联用一线治疗肺癌等肿瘤的市场潜力。
今年9月,百利天恒在2024 ESCO年会上首次公布了BL-B01D1在尿路上皮癌(UC)、食管鳞癌(ESCC)和胆道癌(BTC)的临床研究数据,其中:对于既往接受过一线化疗的UC患者,ORR达到90%;用于BTC患者的ORR为28.6%、DCR为76.2%;2.5 mg/kg(RP2D)剂量组ESCC患者的ORR为42.3%,6个月生存率为64.5%。
04
结语
BMS的战略是全面发展,通过“收购 引进”双轮驱动在多个疾病领域广泛布局。这一战略使得BMS在面对专利悬崖时,能够迅速填补产品缺口,并通过KarXT的成功上市带来新的增长点。
可以肯定的说,那个意气风发的全球制药巨头并未远去。
参考资料:
1.各家公司的财报、公告、官微
2.《数十年来首款!百时美施贵宝“first-in-class”小分子疗法获FDA批准》,药明康德,2024.09.27
3.《医药行业~跨国处方药企:MNC重磅产品专利悬崖下众生相,危与机并存,龙头各显神通-240718》,交银国际研报
4.德邦证券、东吴证券研报
$百时美施贵宝(NYSE|BMY)$ $再鼎医药(HK|09688)$ $再鼎医药(NASDAQ|ZLAB)$
@东方财富创作小助手 #盘面热火朝天,股友嗓子冒烟# #大摩、高盛看好!大佬:买中国资产# #机构深夜发文标题仅一字“干”# #A股收复3000点,后市怎么看?#
本文作者可以追加内容哦 !

