
5月26日,Lexicon Pharmaceuticals宣布,FDA已批准SGLT-1/2双效抑制剂Sotagliflozin(索格列净)的上市申请,用于降低成人患者的心血管死亡、因心力衰竭而住院或接受急救的风险。这些患者患有心力衰竭,或患有2型糖尿病、慢性肾病,并携带其它心血管疾病风险因子。
Sotagliflozin是口服的钠-葡萄糖协同转运蛋白1型和2型(SGLT1和SGLT2)的双重抑制剂。SGLT1负责胃肠道中的葡萄糖吸收,对SGLT1的抑制可抑制消化道对葡萄糖和半乳糖的吸收;而SGLT2负责肾脏对葡萄糖的重吸收,对SLGT2抑制则是减少肾小管对葡萄糖的重吸收。
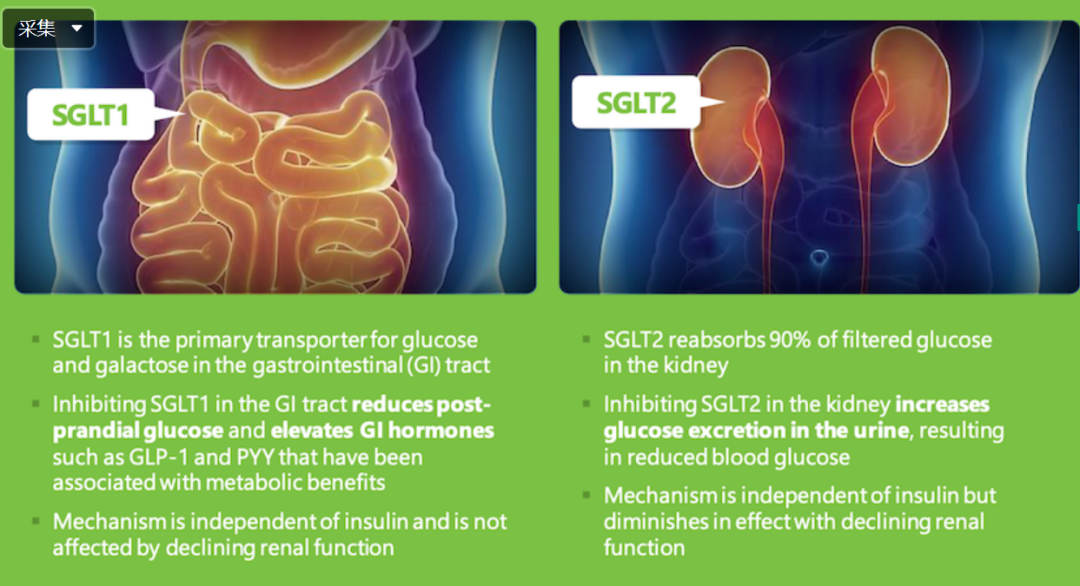
Sotagliflozin作用机制(来源:Lexicon官网)
Sotagliflozin的本次获批是基于两项多中心、随机、双盲、安慰剂对照的III期研究的实验数据,包括1):因心力衰竭恶化而住院的2型糖尿病患者中进行的III期SOLOIST-WHF研究;2)在2型糖尿病合并中度肾功能受损且伴心血管危险因素患者中进行的III期SCORED研究。
研究结果显示,SOLOIST-WHF和SCORED均达到了各自的主要终点(主要复合终点为心血管死亡、因心力衰竭住院人数和因心力衰竭急诊),两项试验的总体耐受性与安慰剂相似。中位数随访时间16个月,结果显示Sotagliflozin治疗可以显著降低2型糖尿病合并中度肾功能受损且伴心血管危险因素患者的心血管死亡、因心衰住院或因心衰急诊的复合终点事件发生率。
虽然Sotagliflozin于2019年4月在欧盟成功获批用于治疗1型糖尿病,但该药物在美国的上市之路可谓是一路波折。2019年3月22日,Lexicon收到了FDA就Sotagliflozin治疗成人1型糖尿病新药上市申请发出的完整回复函(CRL),指出该药物可能会增加糖尿病酮症酸中毒的风险。
Lexicon又于2021年12月30日提交Sotagliflozin治疗成人2型糖尿病患者心力衰竭的新药上市申请。不过在2022年2月28日,Lexicon自愿撤回。2022年5月31日,Lexicon又重新提交了Sotagliflozin治疗心力衰竭的新药上市申请,并于2022年7月27日获得FDA受理。Copyright 2023 PHARMCUBE. All Rights Reserved. 欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。
本文作者可以追加内容哦 !

