K药联合化疗一线治疗胆道癌新适应症上市申请获FDA受理

6月8日,默沙东宣布K药联合化疗(吉西他滨和顺铂)一线治疗晚期或不可切除胆道癌(BTC)的新适应症上市申请已获FDA受理,PDUFA日期定为2024年2月7日。 此次申请主要基于III期随机、双盲、安慰剂对照的KEYNOTE-966研究。结果显示,与单独化疗相比,K药组合疗法显著改善了患者总生存期(12.7 vs. 10.9个月;P=0.0034),研究达到主要终点。这也是K药胆道癌第一项顺利完成且成功的III期研究。
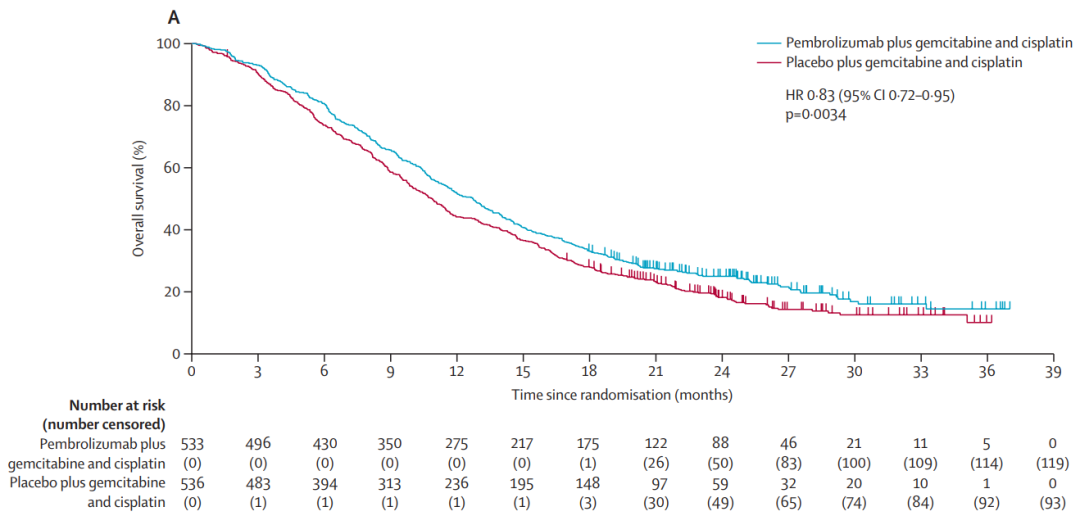
来源:Lancet BTC(包括胆管癌和胆囊癌)是一组罕见且具有侵袭性的胃肠道癌症,也是第二常见(最常见为肝细胞癌)的原发性肝癌,占所有肝癌的15%。据估计,全球每年约有21万例BTC新确诊病例和17万例死亡病例。由于这种疾病早期通常没有明显的症状,因此大多数(70%)患者确诊时已是晚期,治疗选择有限且预后较差。大约5%-15%的患者只能存活5年。 截至目前,已有6款产品获批用于治疗BTC,但仅度伐利尤可作为一线方案,且度伐利尤是第一款获批用于治疗BTC的免疫疗法。
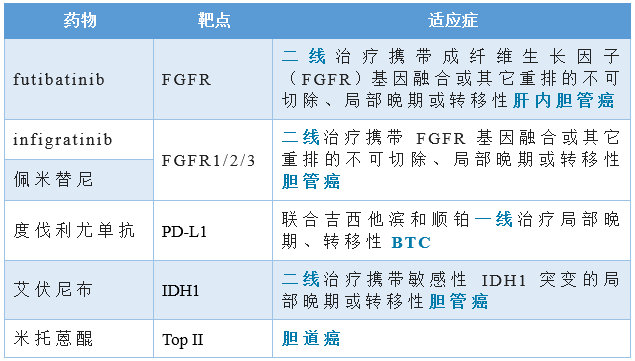
另有18款产品处于III期研究阶段,但仅K药、恩沃利单抗(康宁杰瑞)、替吉奥(Taiho)、特瑞普利单抗(君实生物)和NUC-1031(NuCana)开发了一线方案,其中替吉奥已完成了2项III期研究(一线治疗)。 Copyright 2023 PHARMCUBE. All Rights Reserved. 欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。
免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。
医药魔方读者调研问卷
感谢陪伴 期待反馈
郑重声明:用户在社区发表的所有信息将由本网站记录保存,仅代表作者个人观点,与本网站立场无关,不对您构成任何投资建议,据此操作风险自担。请勿相信代客理财、免费荐股和炒股培训等宣传内容,远离非法证券活动。请勿添加发言用户的手机号码、公众号、微博、微信及QQ等信息,谨防上当受骗!

郑重声明:东方财富网发布此信息的目的在于传播更多信息,与本站立场无关。东方财富网不保证该信息(包括但不限于文字、视频、音频、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关信息并未经过本网站证实,不对您构成任何投资建议,据此操作,风险自担。


 另有18款产品处于III期研究阶段,但仅K药、恩沃利单抗(康宁杰瑞)、替吉奥(Taiho)、特瑞普利单抗(君实生物)和NUC-1031(NuCana)开发了一线方案,其中替吉奥已完成了2项III期研究(一线治疗)。 Copyright 2023 PHARMCUBE. All Rights Reserved. 欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。
另有18款产品处于III期研究阶段,但仅K药、恩沃利单抗(康宁杰瑞)、替吉奥(Taiho)、特瑞普利单抗(君实生物)和NUC-1031(NuCana)开发了一线方案,其中替吉奥已完成了2项III期研究(一线治疗)。 Copyright 2023 PHARMCUBE. All Rights Reserved. 欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。 
