 7月27日,Biohaven宣布,FDA拒绝受理trigriluzole用于治疗嵴髓小脑性共济失调(SCA)的新药申请(NDA),原因为trigriluzole治疗SCA的III期BHV4157-206研究未达主要终点。该公司表示,未来将要求与FDA召开A类会议以讨论trigriluzole的情况。
7月27日,Biohaven宣布,FDA拒绝受理trigriluzole用于治疗嵴髓小脑性共济失调(SCA)的新药申请(NDA),原因为trigriluzole治疗SCA的III期BHV4157-206研究未达主要终点。该公司表示,未来将要求与FDA召开A类会议以讨论trigriluzole的情况。  Trigriluzole是一款第三代兴奋性氨基酸转运蛋白2(EAAT2)调节剂,可调节人体主要的兴奋性神经递质谷氨酸水平。该分子通过增加神经胶质细胞中EAAT的表达并增强其功能来增加神经元突触对谷氨酸的摄取,从而降低神经元突触中的谷氨酸水平。 BHV4157-206研究是一项随机、双盲、安慰剂对照的III期临床试验,共纳入218例成年SCA患者,旨在评估trigriluzole(200mg)的疗效和安全性。研究的主要终点为修订版共济失调功能评定量表(f-SARA)总分相比于基线的变化。 结果显示,在总体SCA人群中,trigriluzole组与安慰剂组患者的f-SARA评分变化均为4.9分,无显著统计学差异。Biohaven表示,造成该结果的原因是研究期间SCA患者疾病进展的情况低于预期。
Trigriluzole是一款第三代兴奋性氨基酸转运蛋白2(EAAT2)调节剂,可调节人体主要的兴奋性神经递质谷氨酸水平。该分子通过增加神经胶质细胞中EAAT的表达并增强其功能来增加神经元突触对谷氨酸的摄取,从而降低神经元突触中的谷氨酸水平。 BHV4157-206研究是一项随机、双盲、安慰剂对照的III期临床试验,共纳入218例成年SCA患者,旨在评估trigriluzole(200mg)的疗效和安全性。研究的主要终点为修订版共济失调功能评定量表(f-SARA)总分相比于基线的变化。 结果显示,在总体SCA人群中,trigriluzole组与安慰剂组患者的f-SARA评分变化均为4.9分,无显著统计学差异。Biohaven表示,造成该结果的原因是研究期间SCA患者疾病进展的情况低于预期。  Biohaven根据基因型对疗效数据进行事后分析后发现,在SCA3型患者亚组(占总人群41%),trigriluzole组患者的f-SARA评分变化显示出治疗获益(P=0.053)。
Biohaven根据基因型对疗效数据进行事后分析后发现,在SCA3型患者亚组(占总人群41%),trigriluzole组患者的f-SARA评分变化显示出治疗获益(P=0.053)。 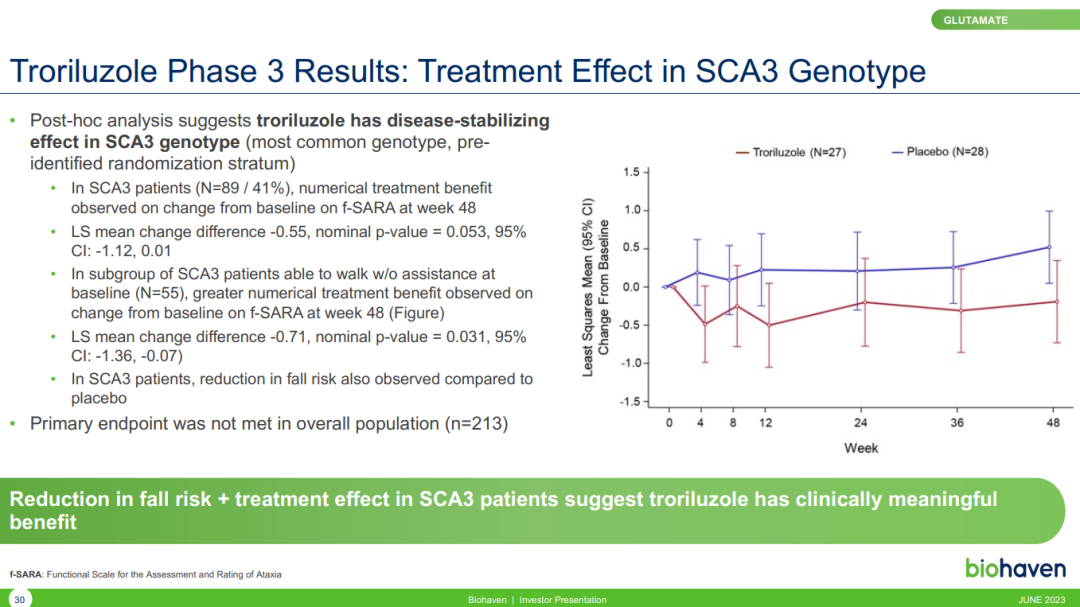 此外,在总体人群中,trigriluzole组可以行走的患者跌倒风险降低了58%(10% vs. 23%;P=0.043)。 SCA是一种显性遗传性疾病,其特征是进行性共济失调,影响手、手臂和腿的协调以及平衡和言语能力。SCA通常在成年早期出现症状,并在数年内进展。疾病进展后,患者可能需要依靠轮椅行动,或者因步态不协调而易跌倒、因言语障碍而无法沟通、吞咽困难,甚至过早死亡。症状的范围和疾病进展速度取决于SCA的类型、发病年龄和其他遗传因素。目前,美国尚无SCA疗法获批上市,而全球内仅taltirelin(促甲状腺素释放激素类似物)在日本获批用于治疗SCA。
此外,在总体人群中,trigriluzole组可以行走的患者跌倒风险降低了58%(10% vs. 23%;P=0.043)。 SCA是一种显性遗传性疾病,其特征是进行性共济失调,影响手、手臂和腿的协调以及平衡和言语能力。SCA通常在成年早期出现症状,并在数年内进展。疾病进展后,患者可能需要依靠轮椅行动,或者因步态不协调而易跌倒、因言语障碍而无法沟通、吞咽困难,甚至过早死亡。症状的范围和疾病进展速度取决于SCA的类型、发病年龄和其他遗传因素。目前,美国尚无SCA疗法获批上市,而全球内仅taltirelin(促甲状腺素释放激素类似物)在日本获批用于治疗SCA。Copyright 2023 PHARMCUBE. All Rights Reserved.
追加内容
本文作者可以追加内容哦 !

