
近日,蓝鸟生物公布2023年中报:上半年公司营收927.1万美元(6,684万人民币,按最新汇率1 美元 =7.21 人民币计算),同比增长167.6%;其中产品收入同比增长233%,达到913万美元(6,582万人民币)。而研发费用支出为8842万美元(6.37亿人民币),同比下降38%。现金及现金等价物2.45亿美元(17.66亿人民币)。
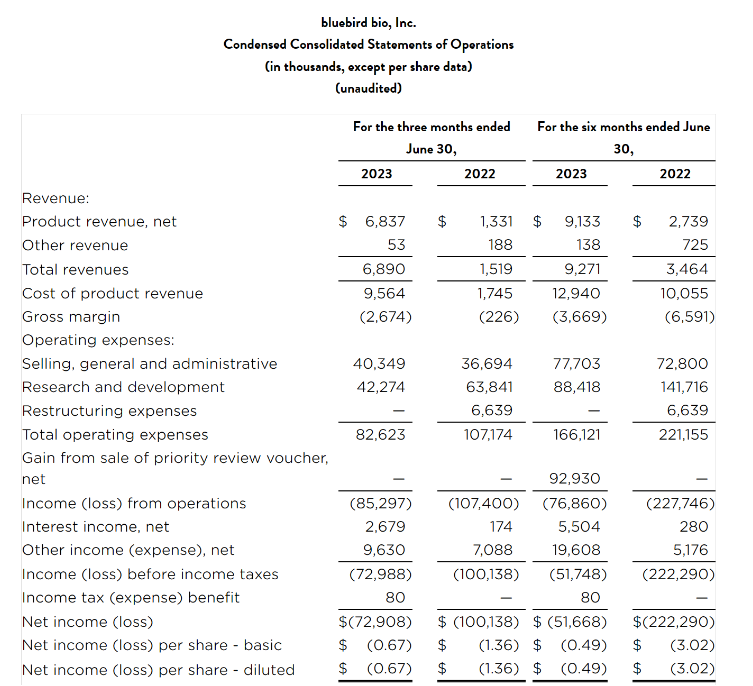

公司目前市值3.6亿美元。
细胞和基因治疗产品(Cellular and gene therapy),简称CGT产品,包括DNA、RNA、寡核苷酸、病毒、细菌和自体或异体细胞等多种形态产品,是一种全新类型的药物,其充满想象力、可能性和治疗性的生物医学应用潜能已初现端倪。
蓝鸟生物共有3款基因疗法,其中ZYNTEGLO和SKYSONA这2款已经进行商业化,今年6月21日,FDA接受了第3款基因疗法lovo-cel的BLA优先审查,用于镰状细胞病(SCD)患者。公司表示lovo-cel的价格可能高达226万美元,具体价格会在FDA批准后确定,FDA已将PDUFA的目标日期设定为2023年12月20日。
如果获得批准,lovo-cel预计将在2024年初进行商业上市。bluebird估计,大约20,000名SCD患者(美国SCD人群的五分之一)可能符合基因治疗的条件。
公司研发管线(部分)
 截图来源:药融云全球药物研发数据库
截图来源:药融云全球药物研发数据库细胞疗法
从细分赛道来看,今年上半年阶段完成融资的细胞治疗企业所涉及的领域较为多样化,其中自体CAR-T仍是主流,通用型CAR-T疗法的企业尚处于早期融资,此外还涉及了TCR-T、TIL、iPSC、NK、CIK、Treg、巨噬细胞、干细胞等,在几大主流细胞疗法快速发展的同时,其他类型的细胞疗法逐渐兴起。在细胞治疗领域,有多家企业完成了较高金额的融资,包括了驯鹿生物、原启生物、来恩生物等。
就在不久前,驯鹿生物/ $信达生物(HK|01801)$ 联合开发的BCMA CAR-T疗法伊基奥仑赛注射液获批上市,用于治疗复发或难治性多发性骨髓瘤(MM)成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂),这也是国内首款BCMA CAR-T疗法。
伊基奥仑赛注射液审评
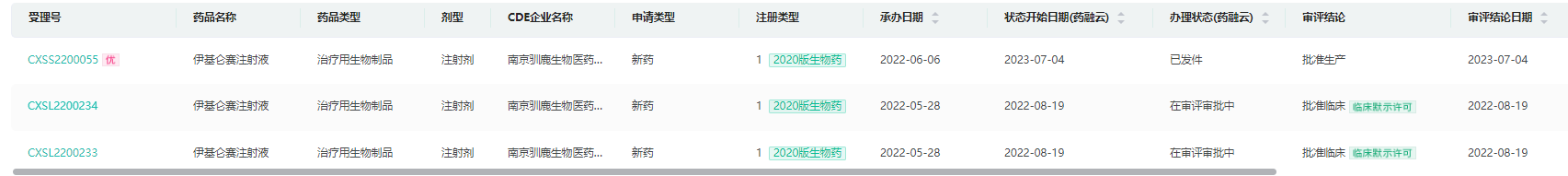 截图来源:药融云中国药品审评数据库
截图来源:药融云中国药品审评数据库基因疗法
基因疗法赛道的融资主要集中在基因编辑和AAV基因疗法上,其中至善唯新和本导基因融资均超过2亿元。值得一提的是,至善唯新在A型血友病AAV基因疗法领域进展较快,国内在这一领域进入临床的企业屈指可数,至善唯新的ZS802应用的自主开发的全球最小的肝脏特异启动子能够解决病毒载体包装难题,显著提高药物质量,而其自主改造优化的凝血VIII因子序列,能够通过突变特定位点氨基酸残基,显著提升药物活力。
本导基因研发的BD111是一款体内基因编辑疗法,旨在利用其原创性的新型基因治疗载体——类病毒体VLP转导CRISPR基因编辑工具直接靶向切割单纯疱疹病毒的基因组,达到降低甚至清除HSV-1病毒基因组的目的,从而实现对疱疹病毒型角膜炎的治疗。2022年6月,BD111获得了美国FDA孤儿药资格批准,今年4月其IND申请获得CDE批准,是全球首个CRISPR抗病毒基因编辑药物,也是国内首个获批进入临床的体内基因编辑药物。
BD111基本信息
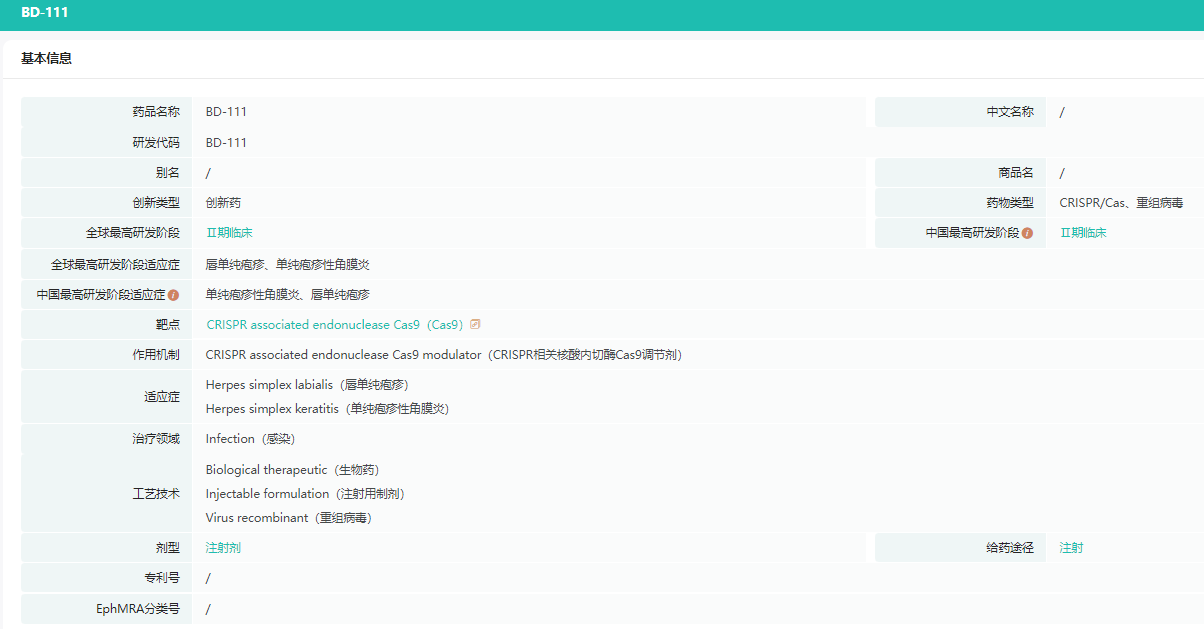 截图来源:药融云全球药物研发数据库
截图来源:药融云全球药物研发数据库参考资料:
1.公司官网
2.药融云数据库
<END>

本文作者可以追加内容哦 !


