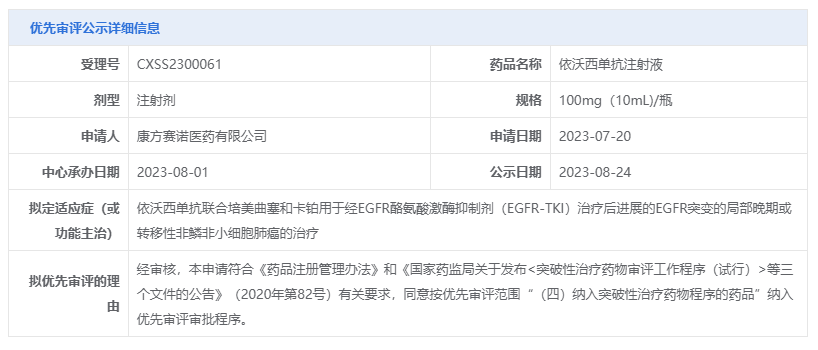
8月24日,CDE官方显示,康方生物的依沃西单抗注射液拟纳入优先审评,拟定适应症为依沃西单抗联合培美曲塞和卡铂用于经EGFR酪氨酸激酶抑制剂(EGFR-TKI)治疗后进展的EGFR突变的局部晚期或转移性非鳞非小细胞肺癌的治疗。
依沃西单抗是康方生物自主研发的全球首创PD-1/VEGF双特异性抗体。
HARMONi是一项国际多中心、随机、双盲的Ⅲ期注册性研究,计划在美国,加拿大,欧洲和中国招募超过400名患者。HARMONi研究在中国的部分亦称为“AK112-301研究”,目前,AK112-301研究在国内已完成患者入组。
此前,2022 ASCO上披露的II期临床研究结果显示:依沃西单抗治疗EGFR-TKI耐药的EGFR突变的晚期nsq-NSCLC的ORR为68.4%,DCR为94.7%;中位PFS为8.2个月,6个月PFS率为69.3%。
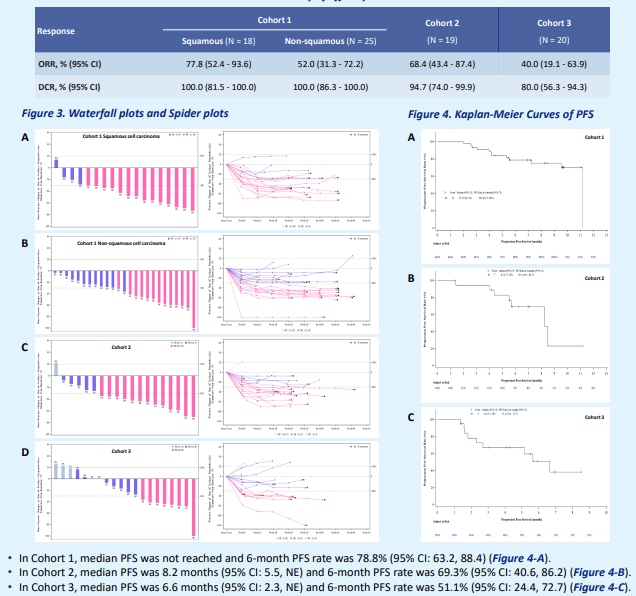
HARMONi,又称AK112-301,是一项多中心、随机、双盲的III期研究。
研究旨在对比依沃西单抗联合培美曲塞和卡铂与安慰剂加培美曲塞和卡铂治疗经一种三代EGFR-TKI(尤其是奥希替尼)治疗进展的EGFR突变、局晚期或转移性非鳞状NSCLC的患者的有效性和安全性。
HARMONi将从美国、加拿大、欧洲和中国招募患者。康方生物负责中国患者入组工作,该部分已完成;Summit公司则负责美国、加拿大和欧洲的患者入组工作。
2022年12月,康方生物的依沃西单抗以总交易额高达50亿美金(5亿美金首付款),外加销售净额两位数提成的合作方案,授予美国Summit Therapeutics公司在美国、欧洲、加拿大和日本的开发独家许可权,创下中国单个创新药物对外权益许可最高交易金额记录。
本文作者可以追加内容哦 !

