1.疫苗
疫苗接种是预防和控制传染病传播最具效益的方法之一。病原体及其代谢物被制备成一种免疫制剂,可通过人工衰减、解毒、失活或基因工程等方法实现传染病防控[1]。传统疫苗,包括减毒活疫苗和灭活疫苗,可在宿主细胞中引起强烈和长期有效的免疫反应,因此在疫苗市场上占有突出地位。出于对传统疫苗潜在病原性、难以生产等因素的考虑,一些新型疫苗,特别是基于病毒样颗粒(Virus-Like Particles,VLPs)的基因工程疫苗,因具有更强的免疫原性和安全性而受到广泛关注(Fig.1)[2]。
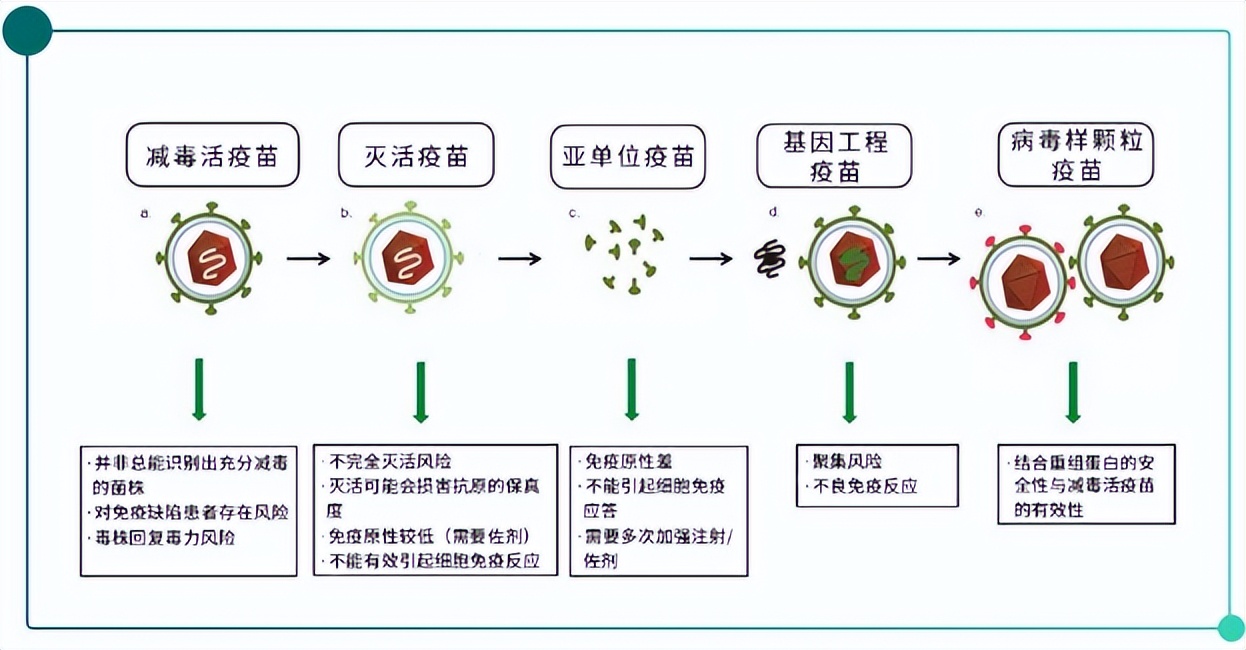
Fig.1 疫苗分类
2.VLPs
VLPs(病毒样颗粒)疫苗是指具有类似于天然病毒粒子空间结构的多聚体颗粒的一类疫苗。VLPs是含有某种病毒的一个或多个结构蛋白的空心颗粒,在形态上与真正的病毒粒子相同或相似,但由于缺乏遗传物质不能进行自主复制,因此不具有致病性和传染性。
从结构上来说,VLPs可以分为无包膜VLP 与有包膜VLP(Fig.2),VLP疫苗甚至可构建双层、三层包膜,实现多价疫苗与多联疫苗的效果。无包膜VLPs,如HPV、HEV等疫苗,结构相对简单,可在原核系统或真核系统中表达,尤其是表达量高和易放大的大肠杆菌与酵母表达系统。而包膜VLPs结构复杂,需要宿主膜参与构建,可选择在酵母、昆虫细胞以及植物细胞等真核系统中表达[3]。不同的表达系统在VLP的含量和完整VLP的比率上有差异,进而影响免疫原性。
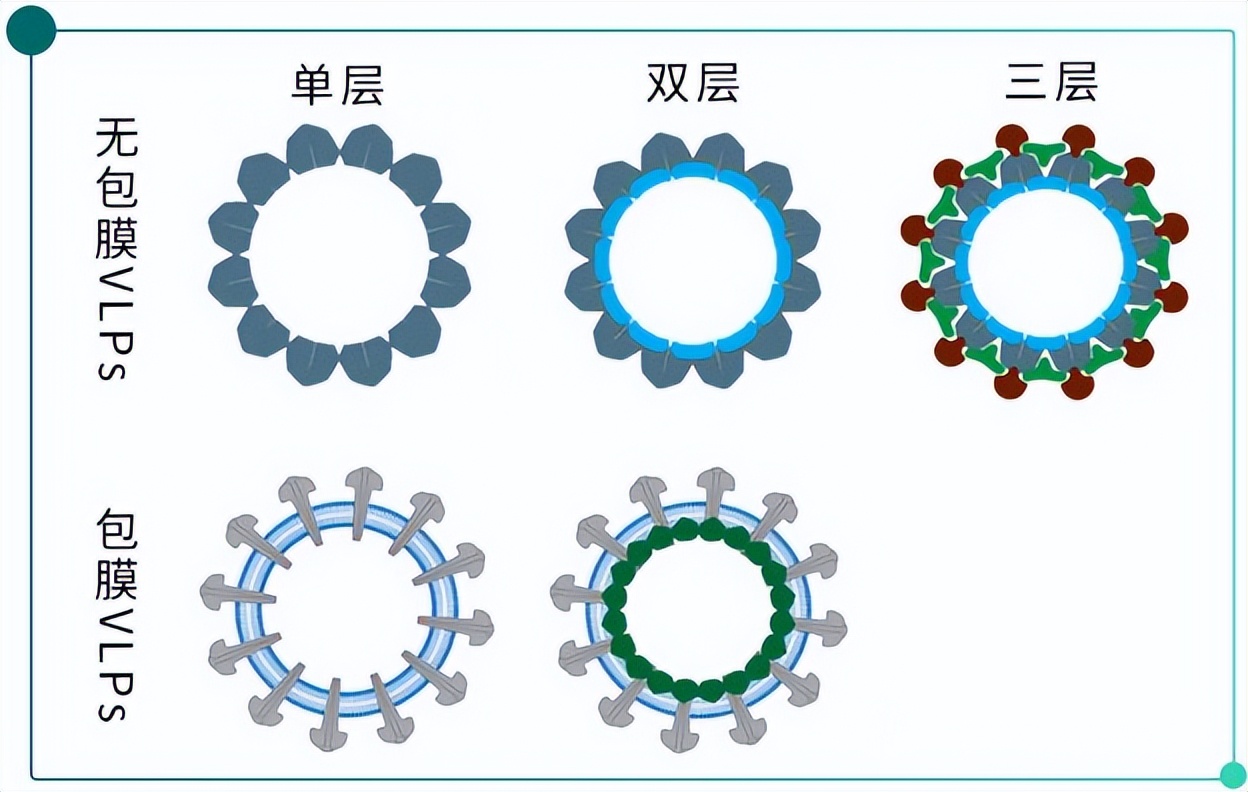
Fig.2无包膜VLPs与包膜VLPs
3.上市的VLPs疫苗
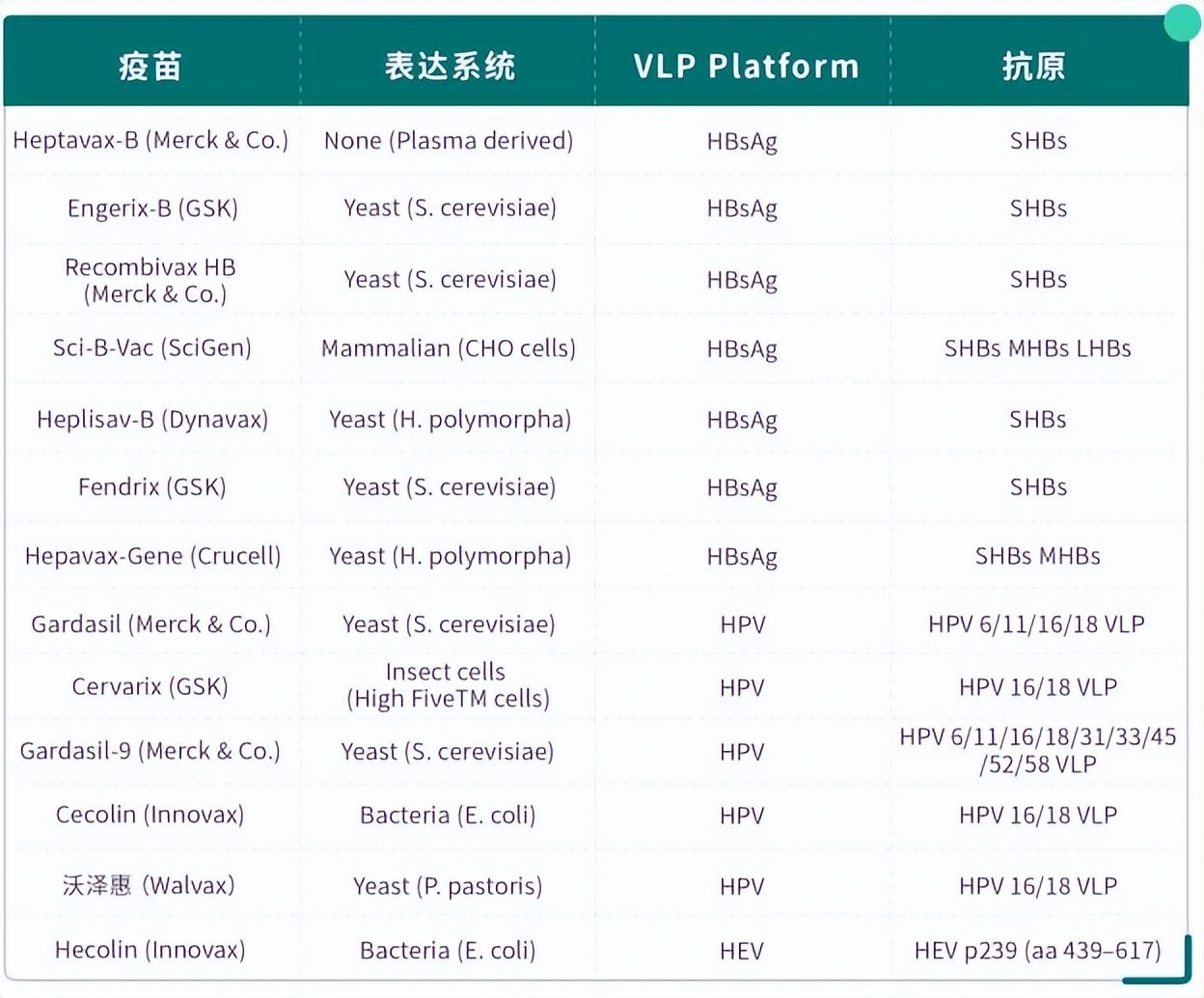
目前,几种基于VLP的疫苗已经上市(Table 1.),包括预防乙型肝炎病毒(HBV)的Recombivax HB和Engerix-B,预防人瘤病毒(HPV)的Gardasil, Cervarix和Gardasil-9,以及应用于预防戊型肝炎病毒(HEV)的Hecolin等。
Table 1.已上市的病毒颗粒样疫苗
HBV乙型肝炎病毒疫苗
乙型肝炎病毒(Hepatitis B virus, HBV)是乙型肝炎的主要病原,属于包膜DNA病毒,包含由脂质和三种包膜蛋白组成的外膜。目前,疫苗接种是预防HBV感染最有效的方法[4]。
迄今为止,HBV的VLP疫苗已经开发了三代。Heptavax-B是一代疫苗,该疫苗是从乙肝患者血样中分离得到乙肝表面抗原颗粒,属于灭活疫苗。
出于对一代疫苗安全性和来源不确定性的考虑,第二代基于HBV VLPs的基因工程疫苗Recombivax HB(MSD)和Engerix-B(GSK)获批上市,两者均使用酿酒酵母系统表达HBsAg(具有规则的正二十面体对称结构)。2018年,在汉逊酵母中表达的含有重组HBsAg及兼具Toll-like receptor 9激动剂佐剂的新型乙肝疫苗Heplisav-B批准上市,其免疫原性高于Engerix-B(接种3针,每针间隔6个月),仅接种2针即可(间隔1个月)。
第二代疫苗仅含有单一抗原(Small S Antigen of HBsAg)疫苗实现血清保护的时间长,因此为提高乙肝疫苗的有效性和保护效力,第三代疫苗Sci-B-Vac(PreHevBrio)在CHOHBsAg的VLPs,更接近天然结构而具有更高的免疫原性[5]。
Table 2.二代、三代乙肝疫苗对比

HPV人瘤病毒疫苗
宫颈癌是全球女性癌症死亡的第二大常见原因,全世界约70%的宫颈癌由高危HPV亚型16和18导致。四价Gardasil(MSD)是第一个被批准作为人瘤病毒(HPV)预防性的疫苗。在酵母中表达得到的重组蛋白L1自组装成VLP,主要为HPV 6/11/16/18这四种HPV类型引起的病毒感染提供保护。2014年,默沙东公司进一步推出的九价疫苗Gardasil-9,有着更高的总抗原量和铝佐剂含量,除了Gardasil提供的预防HPV 6/11/16/18病毒之外,该疫苗还对HPV 31/33/45/52/58病毒具有额外的预防作用。
2009年,FDA批准了一种名为Cervarix(GSK)的二价疫苗,该疫苗采用杆状病毒昆虫细胞表达系统,主要靶向HPV 16/18,因为Cervarix拥有一种新型的AS04佐剂系统,对HPV 16/18具有更好的免疫原性和长期保护作用。
2019年12月,馨可宁正式获得国家医药品监督管理局批准在中国使用,用于HPV 16/18预防。相比酵母和昆虫/杆状病毒表达系统,馨可宁应用的大肠杆菌(E.coli)表达体系可以节省成本。同样用于预防HPV 16/18的沃泽惠于2022年5月在中国批准上市,该疫苗则由毕赤酵母表达。
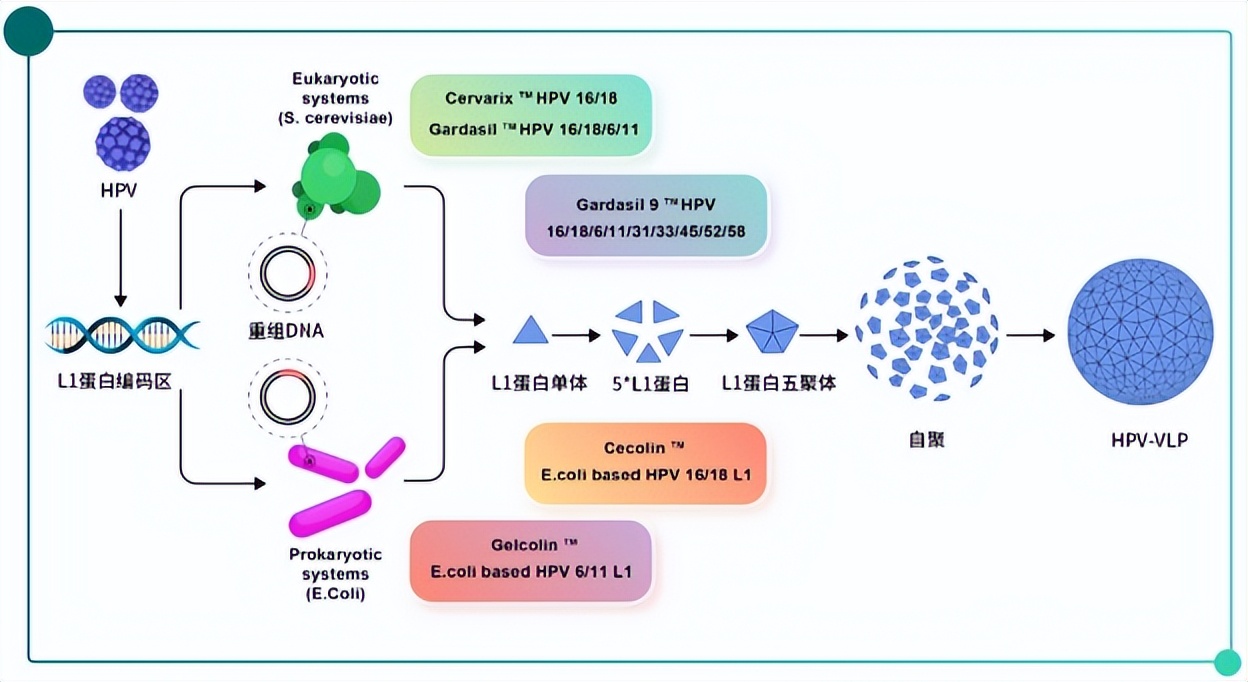
Fig.3HPV疫苗 [6]
截至2022年12月31日,中国正处于临床研究阶段的人瘤病毒疫苗共有20种。其中瑞科生物、万泰生物、沃森生物、博唯生物、康乐卫士的九价HPV疫苗以及相关产品已进入III期临床阶段[7]。
人瘤病毒含有两种病毒编码的蛋白质,分别为 L1 和 L2。这两种蛋白质形成二十面体衣壳, L1 是主要的结构蛋白。目前,已上市的预防性HPV疫苗都是基于仅含有L1蛋白的自组装VLPs,因为L1蛋白是病毒的主要结构蛋白,可以自组装成具有高免疫原性的VLPs,能够诱导强烈的类型特异性免疫应答。微小衣壳蛋白L2作为HPV类型中高度保守的蛋白,被认为是开发下一代泛HPV疫苗的合适靶点。Schellenbacher等人构建了一种同时表达L1和L2蛋白的嵌合HPV疫苗(HPV 16 L1-HPV 16 L2),并在佐剂诱导下针对HPV 16产生广谱中和抗体[8]。
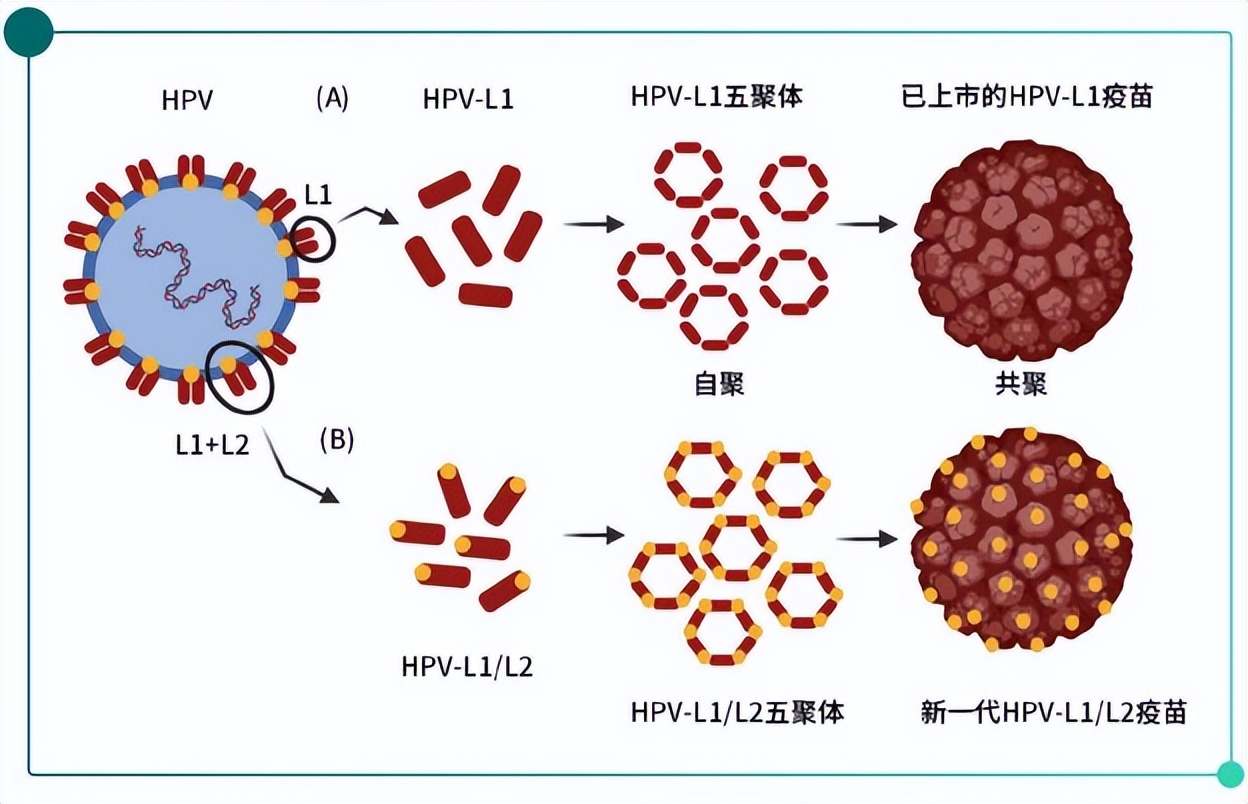
Fig.4 HPV 结构蛋白
HEV戊型肝炎病毒疫苗
HEV是一种非包膜单链RNA病毒,其基因组包含3个开放阅读框,ORF2编码唯一的结构蛋白。厦门万泰生物技术有限公司研制的基于截断的pORF2的HEV239 (Hecolin)于2012年在中国获批,该疫苗由大肠杆菌表达,是全球首个且唯一的戊肝疫苗。
4.下游纯化工艺
VLPs表达系统的多样性也导致下游纯化工艺不具有普适性。Fig.5 为一般下游工艺流程图[9]。
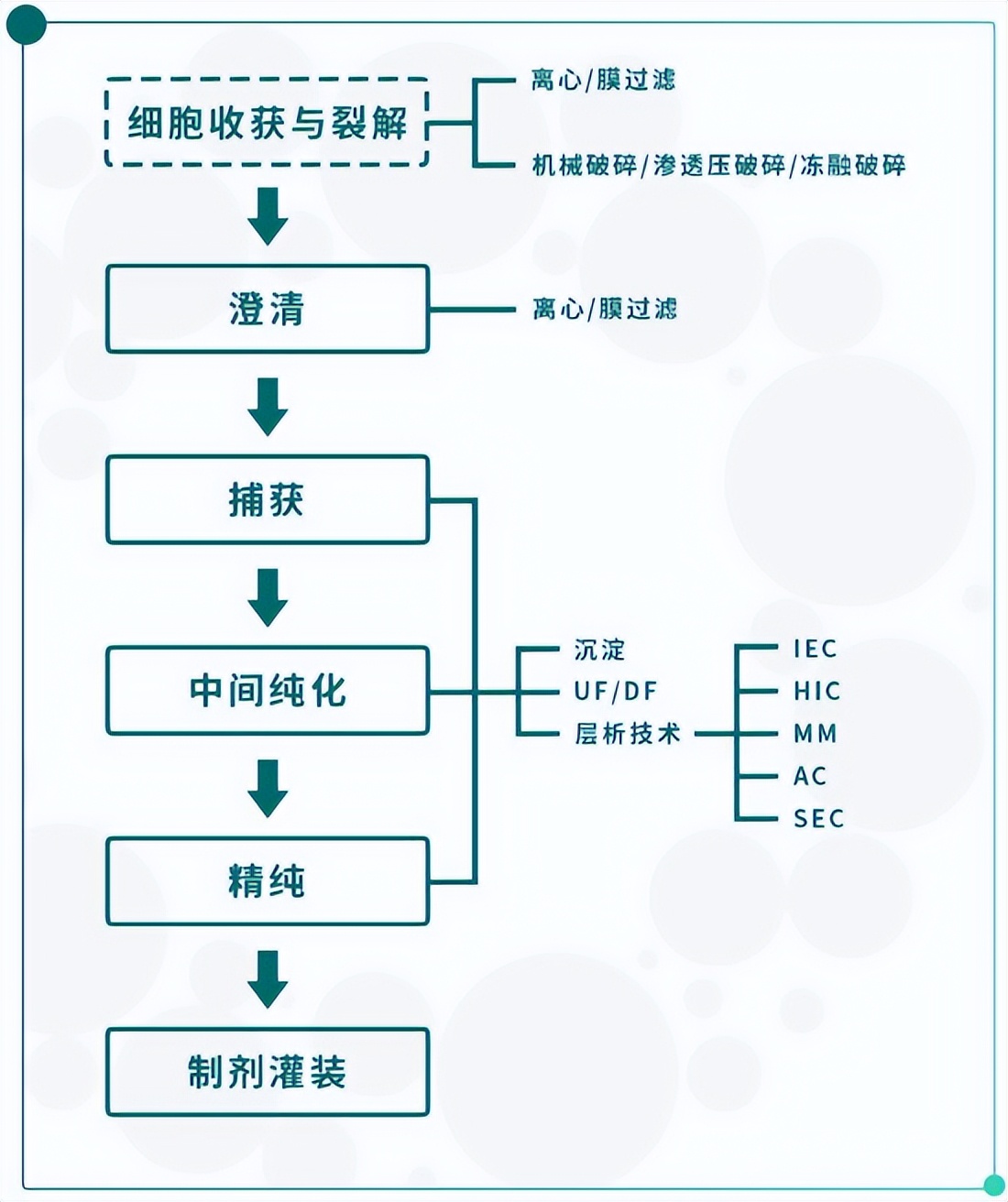
Fig.5 VLP疫苗的下游工艺流程
纯化包括粗纯、中间纯化及精纯等阶段。色谱法是VLPs下游工艺的核心操作单元,包括亲和层析、离子层析、疏水层析、分子筛层析以及复合模式层析。
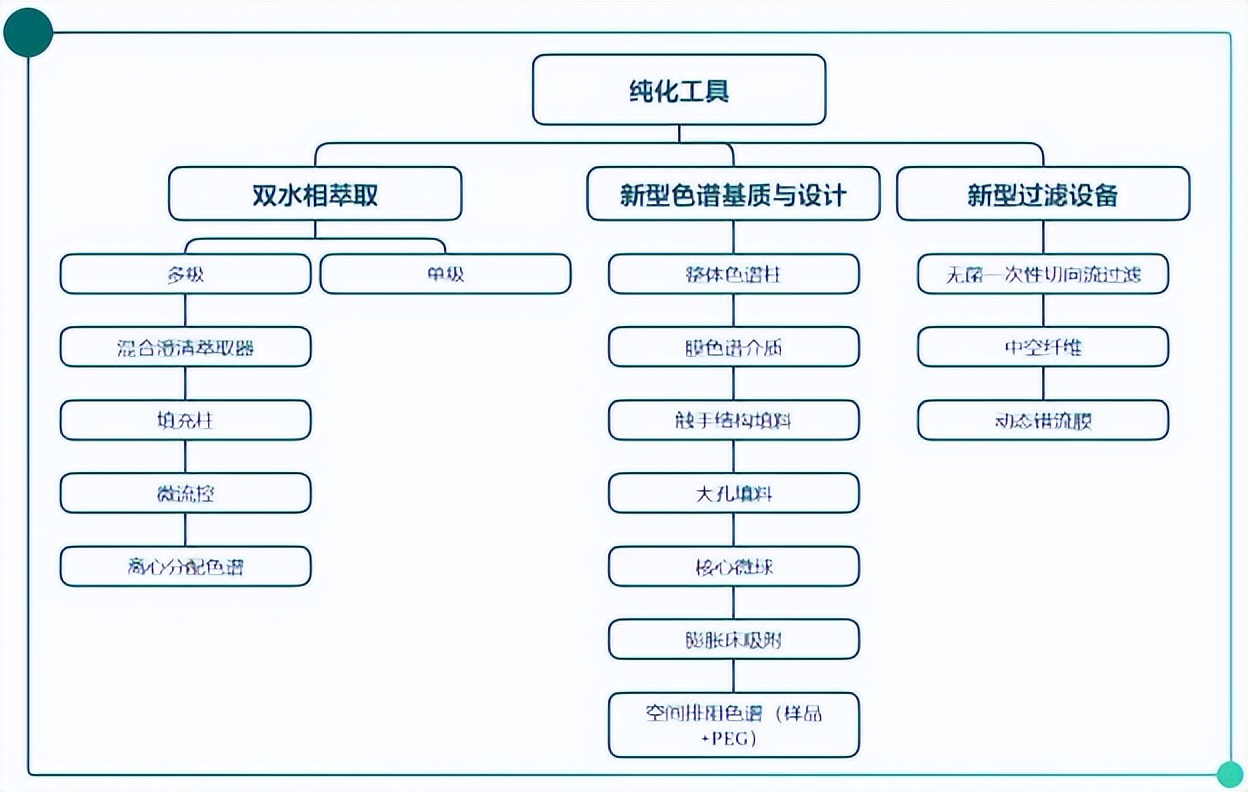
Fig.6 VLPs纯化技术
HBV疫苗生产工艺
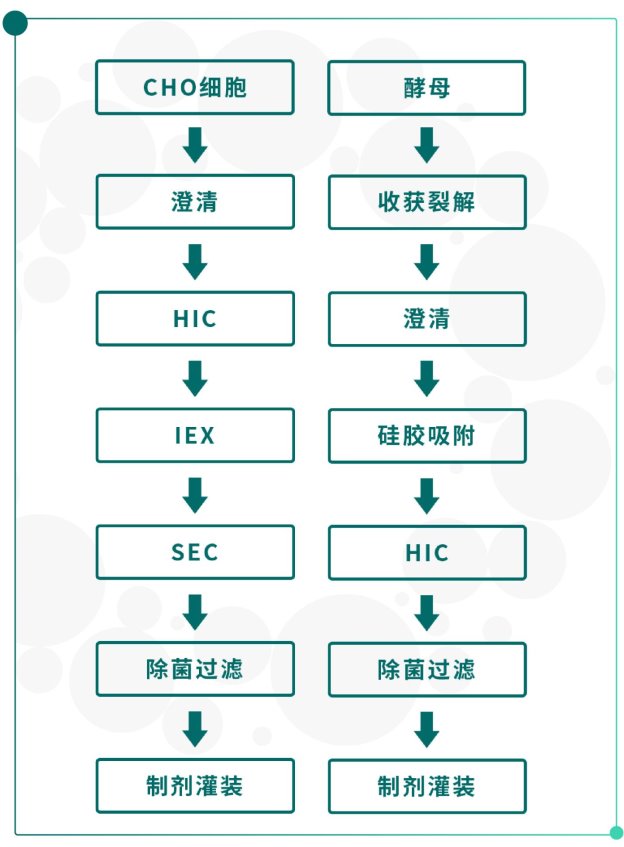
Fig.7 CHO细胞与酵母表达系统制备HBsAg工艺流程
国内乙肝疫苗有三种技术路线(Fig.7),分别是CHO细胞、汉逊酵母和酿酒酵母。酵母细胞在制备HBsAg时多为胞内表达,需收获裂解后澄清,疏水捕获(HBsAg蛋白的疏水键可与疏水配基结合),流穿模式下阴离子去除大量HCP等杂质,分子筛精纯去除小分子杂质。而CHO细胞表达系统多为胞外表达,料液中含少量HCP,无需裂解过程。CHO含糖基化HBsAg,更接近天然结构,纯化过程与酵母表达系统相比简单,可在粗纯阶段选择疏水作用相对较弱的填料。
博格隆提供系列疏水填料,Diamond HIC系列及Diamond HIC Mustang系列填料是以高刚性琼脂糖为基架偶联相对应的疏水基团,反压低、流速快,适合生物分子的大规模分离纯化。

Fig.8 Diamond Butyl填料
HPV疫苗生产工艺
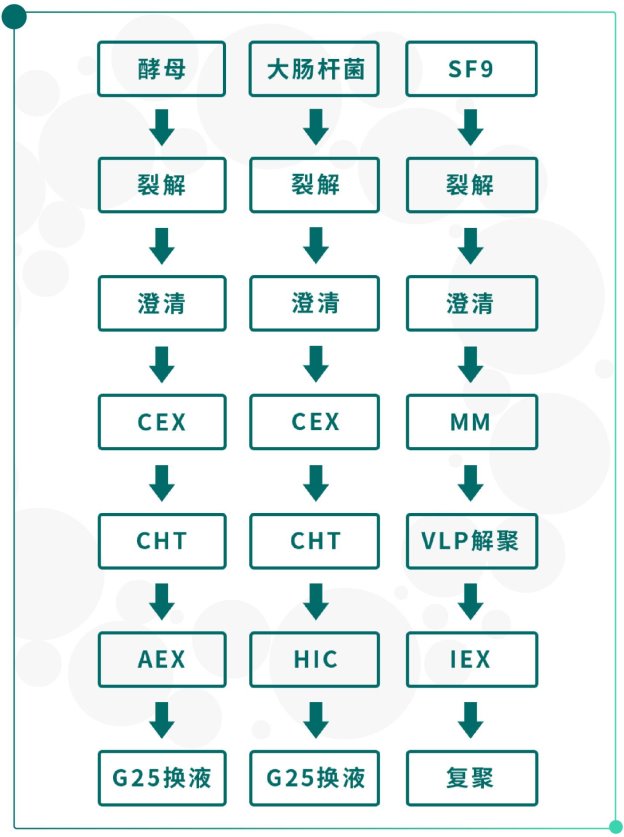
Fig.9 HPV疫苗纯化工艺流程
上市HPV疫苗源于大肠杆菌、酵母以及杆状病毒/昆虫细胞三种表达系统(Fig.9),下游纯化工艺一般以强阳离子捕获。
博格隆MegaPoly 50 HS 具有特殊的孔径结构,较大的贯穿孔和扩散孔可在提供高动态载量的同时降低扩散对层析的影响,赋予产品高流速、高载量、高分辨率的特性,在捕获阶段提供更快速,更高效的分离纯化选择。后续通过羟基磷灰石(CHT Ⅱ)、离子或疏水层析进行精纯。纯化过程中,大肠杆菌表达系统需注意去除内毒素,杆状病毒/昆虫细胞表达系统需注意去除重组杆状病毒(BV)基因组及HCD。离子交换可显著去除HCP、HCD以及大肠内毒素,不同粒径的离子交换介质可应用于捕获或精纯阶段。
博格隆Diamond IEX系列填料是将离子交换基团偶联到带有葡聚糖长链的高刚性琼脂糖上,延伸臂增加配基密度从而提高蛋白载量,高效分离纯化蛋白。

Fig.10 Diamond DEAE(左)与Diamond Q(右)填料
多模式层析因为能同时提供不同类型的相互作用力,所以在 VLPs 纯化工艺开发中占据优势地位。
博格隆Diamond Layer 400和Diamond Layer 700是新型的多模式纯化层析介质,分子量排阻分别为400KD和700KD,其双层结构由具有阴离子和疏水作用的核心微球和具有分子筛作用的薄层钝化外壳(一层不带配基的琼脂糖)组成。小于对应分子量的杂质进入微球内部与配基基团结合,病毒颗粒会被阻隔在微球外。因此,相对于传统分子筛,其最大的优势在于上样量大大提高,且在放大过程中可有效减小柱体积。该类介质专为病毒和其它生物大分子的中间纯化和精细纯化而设计,是疫苗生产中病毒纯化介质的极佳选择。

Fig.11 Diamond Layer 700 填料
为了提高疫苗质量,所有表达系统均需进行解聚再复聚的步骤。因为杂质除了位于颗粒表面外,还可能结合在颗粒内部,解聚状态下纯化可更彻底地去除HCP与HCD。天然HPV颗粒含有L1蛋白与L2蛋白,而目前HPV疫苗不含L2蛋白,导致在组装过程中出现颗粒不均一的情况,因此解聚后复聚可以使颗粒均一,增强免疫原性。可以在层析过程中添加适量DTT解聚,后续复聚前需置换缓冲液去除还原剂。
为达到更好的VLPs 疫苗纯化效果,下游纯化应根据目的抗原的性质及表达体系的复杂性选择合适的层析方式,并搭配膜层析技术提高免疫原性和安全性。
[1] Recent Progress on the Versatility of Virus-Like Particles. VACCINE, 2020, 8, 139.
[2] Production of virus-like particles for vaccines. NEW BIOTECHNOLOGY, 39, pp.174-180.
[3] Bioengineering Virus-Like Particles as Vaccines. BIOTECHNOLOGY AND BIOENGINEERING,111 (3) , pp.425-440.
[4] Hepatitis B vaccine development and implementation. HUMAN VACCINES &IMMUNOTHERAPEUTICS, 16 (7) , pp.1533-1544.
[5] Virus-like particle vaccinology, from bench to bedside. CELLULAR & MOLECULAR IMMUNOLOGY ,19 (9) , pp.993-1011
[6] An Update on Human Papilloma Virus Vaccines History Types Protection and Efficacy. FRONTIERS IN IMMUNOLOGY,12
[7] 人用疫苗市场发展现状与未来 趋势研究报告.
[8] Chimeric L1-L2 virus-like particles as potential broad-spectrum human papillomavirus vaccines. JOURNAL OF VIROLOGY, 83 (19) , pp.10085-10095.
[9] Next generation vaccines and vectors: Designing downstream processes for recombinant protein-based virus-like particles. BIOTECHNOLOGY JOURNAL, 10 (5) , pp.715-U100.
本文作者可以追加内容哦 !


