摘要:代谢相关脂肪肝炎(MASH/NASH)无药可治局面被打破,巨大市场需求待挖掘。
01 非酒精性脂肪肝炎(NASH)临床需求亟待满足
1.1 非酒精性脂肪性肝炎:疾病进程逐渐恶化,纤维化难以逆转
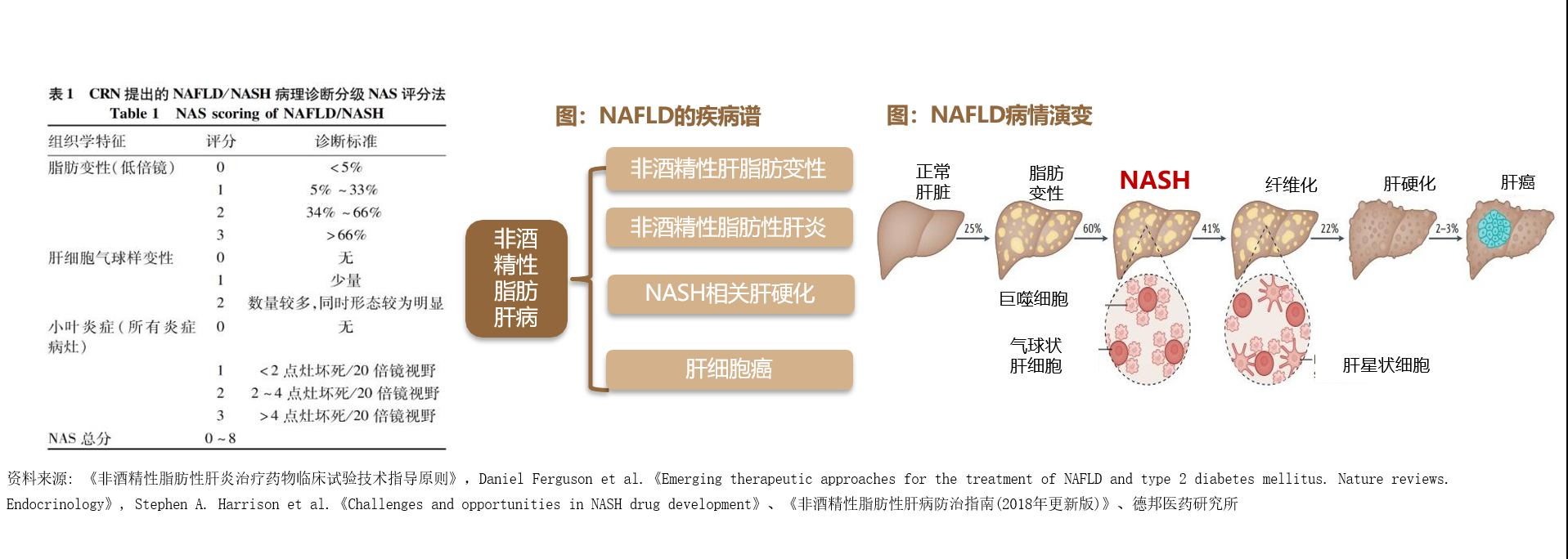
非酒精性脂肪性肝病(NAFLD)已取代慢性乙型肝炎成为我国最常见的慢性肝病(现已更名为代谢相关脂肪性肝病(MAFLD)),是指除酒精和 其他明确损肝因素所致的肝细胞内脂肪过度沉积(>5%)为主要特征的临床病理综合征,是一种与胰岛素抵抗、遗传易感密切相关的代谢性、应激性肝损伤。疾病谱包括非酒精性肝脂肪变(等同非酒精性脂肪肝NAFL)、非酒精性脂肪性肝炎(NASH)及NASH相关肝硬化和肝细胞癌。
NAFLD活动评分(NAS) NAS评分包括脂肪变性、小叶炎症、气球化细胞三部分,总分反映了疾病等级和纤维化的严重程度。
非酒精性脂肪性肝炎(Nonalcoholic Steatohepatitis,NASH)NASH被定义为5%以上的肝脏脂肪变性,合并炎症、肝细胞损伤,伴或不伴肝纤维化。可进展为肝硬化、肝衰竭和肝细胞癌。NASH难以自发缓解,不合并肝纤维化或仅有轻度纤维化(F0-1)为早期NASH;合并显著肝纤维 化或间隔纤维化(F2-3)为纤维化性NASH;合并肝硬化(F4)为NASH肝硬化。(现更名为代谢相关脂肪性肝炎(MASH))。
1.2 NAFLD患病率超过30%,加重我国疾病负担
肥胖和2型糖尿病发病率的上升加剧了非酒精性脂肪性肝病(NAFLD)的流行,据“诺和诺德医学资讯”报道,中国成年人中NAFLD患病率高达 29.2%,10年内整体增长10%,中国NASH患病率约为2.4%-6.1%。NAFLD和NASH患病率随年龄增长,在50-59岁的年龄组达到峰值,随后在60岁后下降 ,男性发病率高于女性。
我国NAFLD/NASH疾病负担急剧加重。我国病毒性肝炎与NAFLD/NASH合并率高,共同促进肝纤维化发生,在我国肝脏相关死亡中 NAFLD/NASH所占比例将进一步提升,预计2030年占比34%。我国NASH患者常常合并其他代谢疾病,如肥胖、二型糖尿病、高血压、高血血脂症等。
1.3 市场空间巨大,需求亟待满足
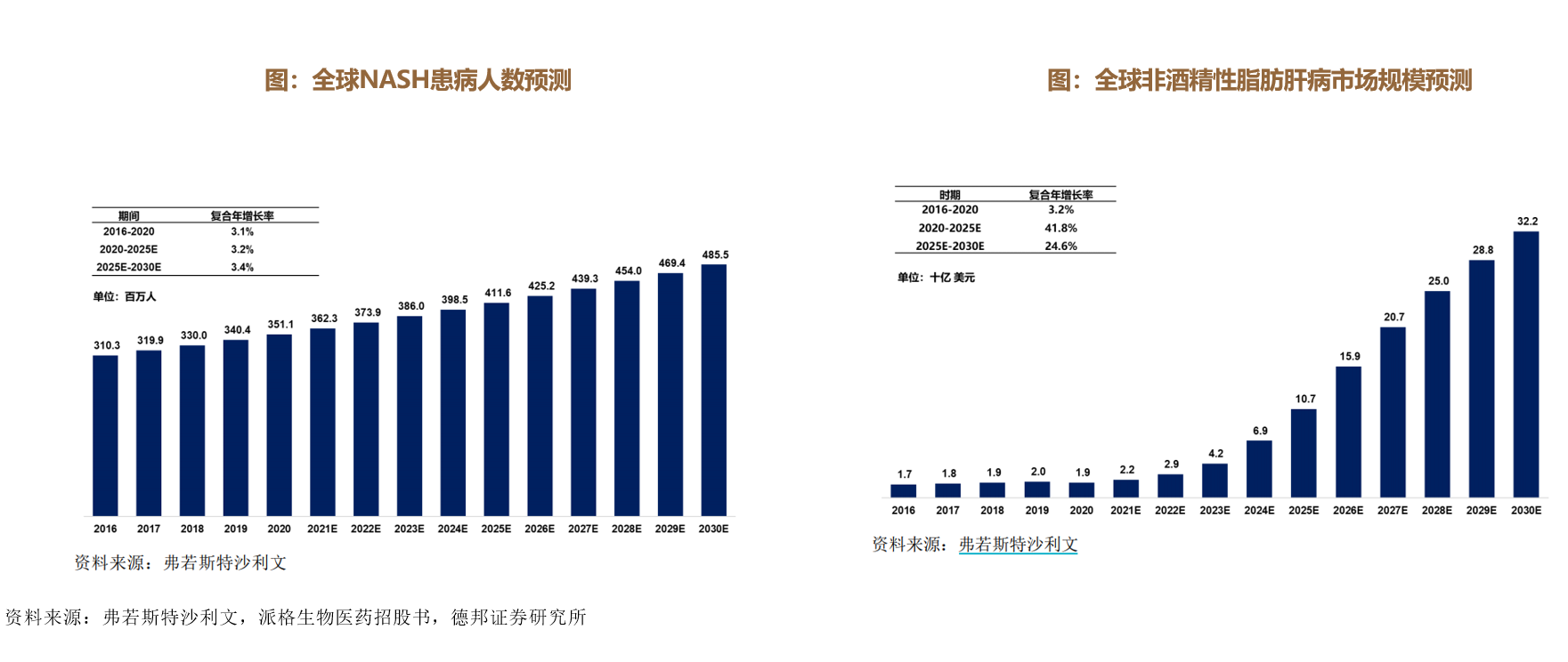
近年来,全球NASH患病人数呈上升趋势,由NASH 导致肝癌的比例也持续上升,而肝癌已成为全球第四大癌症死因。据弗若斯特沙利文报告,全球NASH患病人数从 2016 年的 3.1 亿人已上升到2020年的3.5亿;2021-2030 年,全球 NASH 患病人数将持续增长,预计2030年将达到 4.9 亿人。
据弗若斯特沙利文报告,全球非酒精性脂肪肝病相关药物的市场规模已从2016年的17亿美元增至2020年的19亿美元,复合年增长率为 3.2%;非酒精性脂肪肝病药物市场呈现快速增长的趋势,预计2030年将达到 322 亿美元。
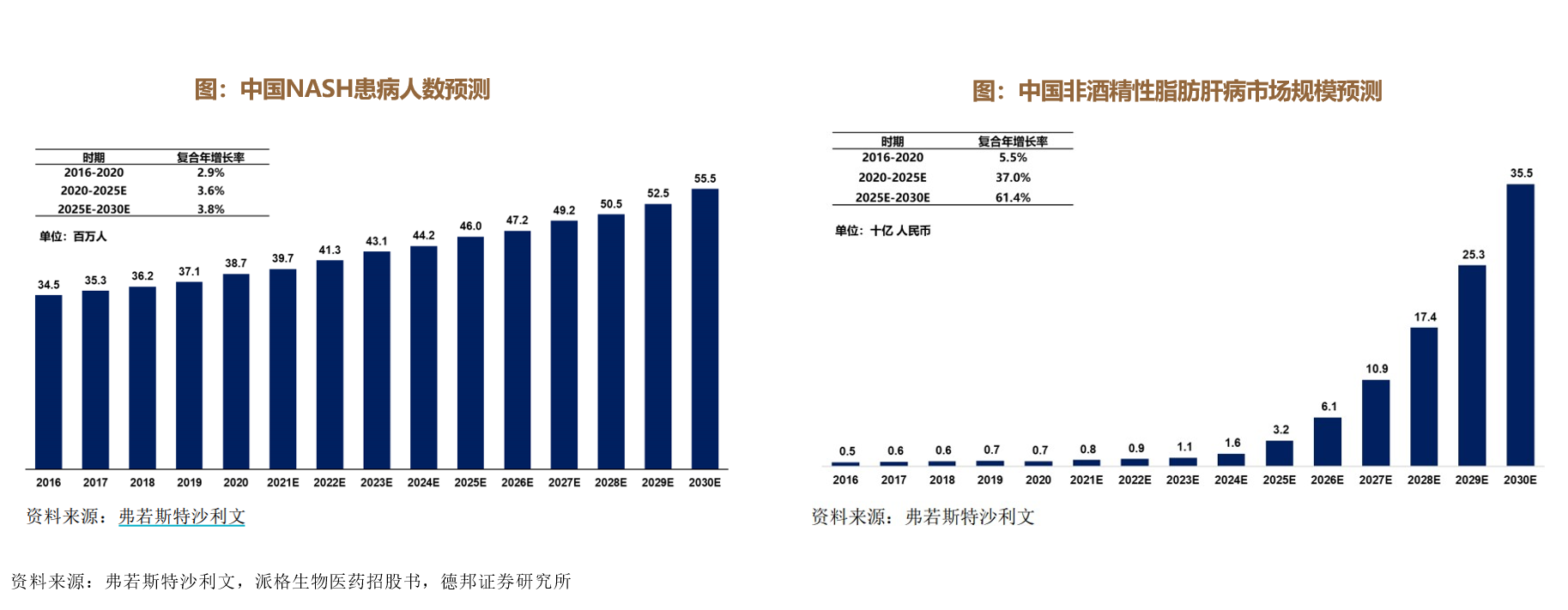
中国 NASH患病人数呈上升趋势,据弗若斯特沙利文报告,2020 年已达到3,870 万人;2021-2030 年,中国的NASH患病率以更快的速度增长,2030年将达到5,550 万人。
据弗若斯特沙利文报告,中国非酒精性脂肪肝病相关药物的市场规模,从2016年的5亿元增至 2020 年的7亿元,年复合增长率为 5.5%;非酒精性脂肪肝病市场规模,将于2030年达到355 亿人民币。
02 MASH药物研发捷报频传,首款新药迎来获批
2.1 NASH治疗药物:干预代谢、纤维化和炎症
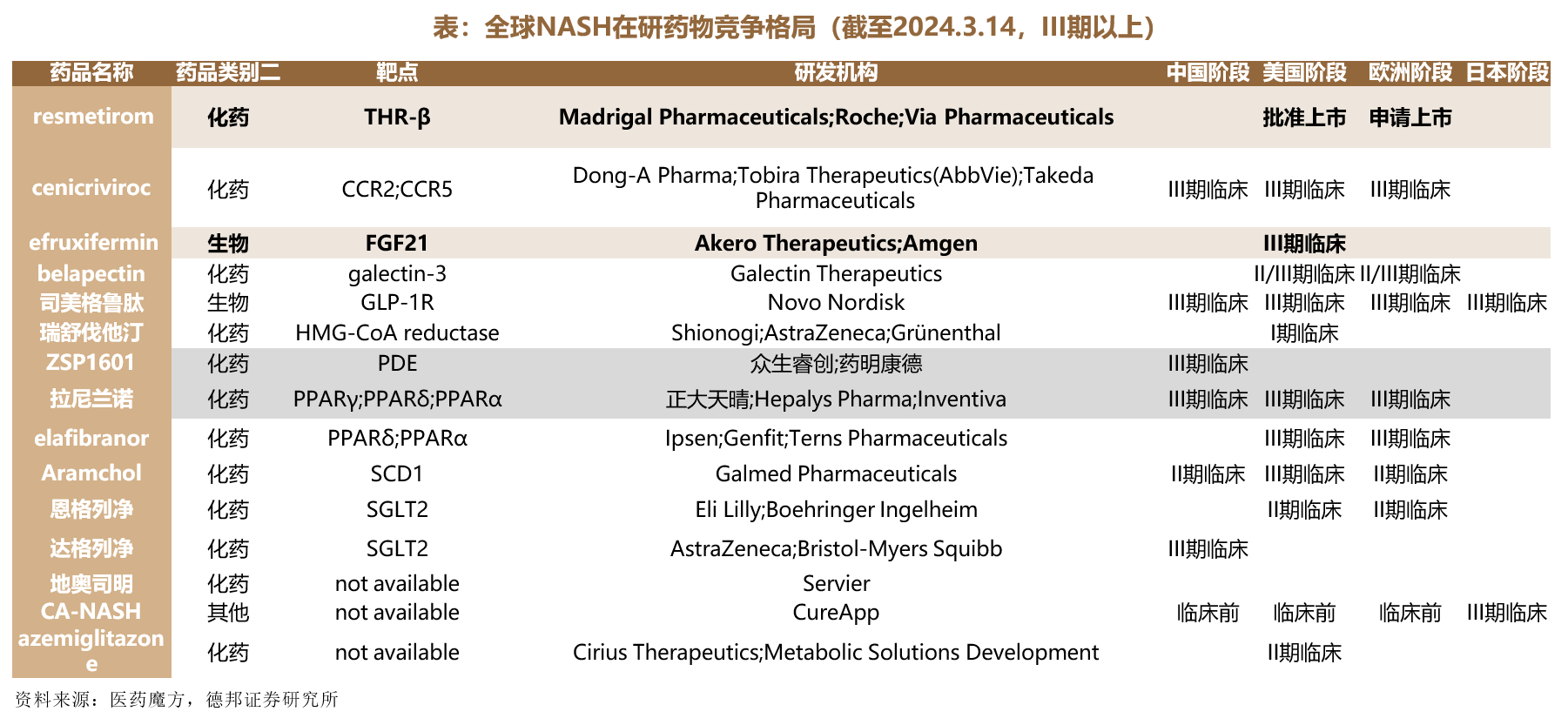
在研治疗NASH的三种最常见途径是作用于新陈代谢,纤维化和炎症。靶向新陈代谢的研究最为热门,涉及靶点包括FXR,GLP-1R,PPAR,FGF21,THR-等,从给药方式来看,GLP-1和FGF21的常规给药方式为注射,其余均为小分子靶向化药。

研发进度:THR-、 FGF21 、GLP-1前景明确
2.2 MASH药物研发捷报频传,首款新药迎来获批
2022-2023年多项临床研究传来捷报,NASH药物研发迎来了转机。
2022年9月,Akero公布了Efruxifermin(FGF21类似物)治疗NASH的IIb期数据,肝穿刺活体组织学数据惊艳四座;
2022年12月,Madrigal宣布Resmetirom(THR-激动剂)治疗NASH的III期MAESTRO研究达到了双重主要终点。公布结果的当日, Madrigal股价大涨268%,市值超过了40亿美元。
2023年6月,多个GLP-1类药物接连公布NASH适应症数据,强势发起冲击。
2023年6月,发表的Gastroenterology & Hepatology上关于司美格鲁肽(GLP-1)治疗NASH的II期临床结果显示司美格鲁肽组脂肪变性减少 显著高于安慰剂。
2023年6月,默沙东(MSD)公布efinopegdutide(GLP-1/GCGR)治疗非酒精性脂肪性肝病(NAFLD)的IIa期临床试验结果,efinopegdutide与司美格鲁肽相比,显著降低患者肝脏脂肪水平。
2023年6月,礼来公布了Retatrutide(GIP/GLP-1/GCG)在NASH治疗中的最新临床试验数据,所有剂量组的Retatrutide均展现出了强大的 肝脏脂肪减少效果,且NASH相关的生物标志物也有显著改善。
2023年9月13日,Madrigal宣布Resmetirom(THR-激动剂)治疗NASH的上市申请获得FDA受理并被授予优先审评资格,PDUFA日期为
2024年2月6日,礼来公布替尔博肽 SYNERGY-NASH 数据,NASH消退且纤维化没有恶化的患者剂量组和安慰剂组的比例分别是:74% 和 13%。
2024年3月4日,Akero Therapeutics公布了HARMONY研究96周初步积极结果,该项IIb期研究评估了其主要候选产品efruxifermin (EFX)
2024年3月14日,FDA批准Resmetirom(商品名:Rezdiffra)上市,用于治疗伴有肝纤维化的非酒精性脂肪性肝炎成人患者。这是FDA批准的首款治疗NASH的创新药物。
资料来源:医药魔方公众号,医脉通公众号,CPHI制药在线公众号,德邦证券研究所。
03 国内药企NASH研发看点
3.1 中国NASH在研药物竞争格局
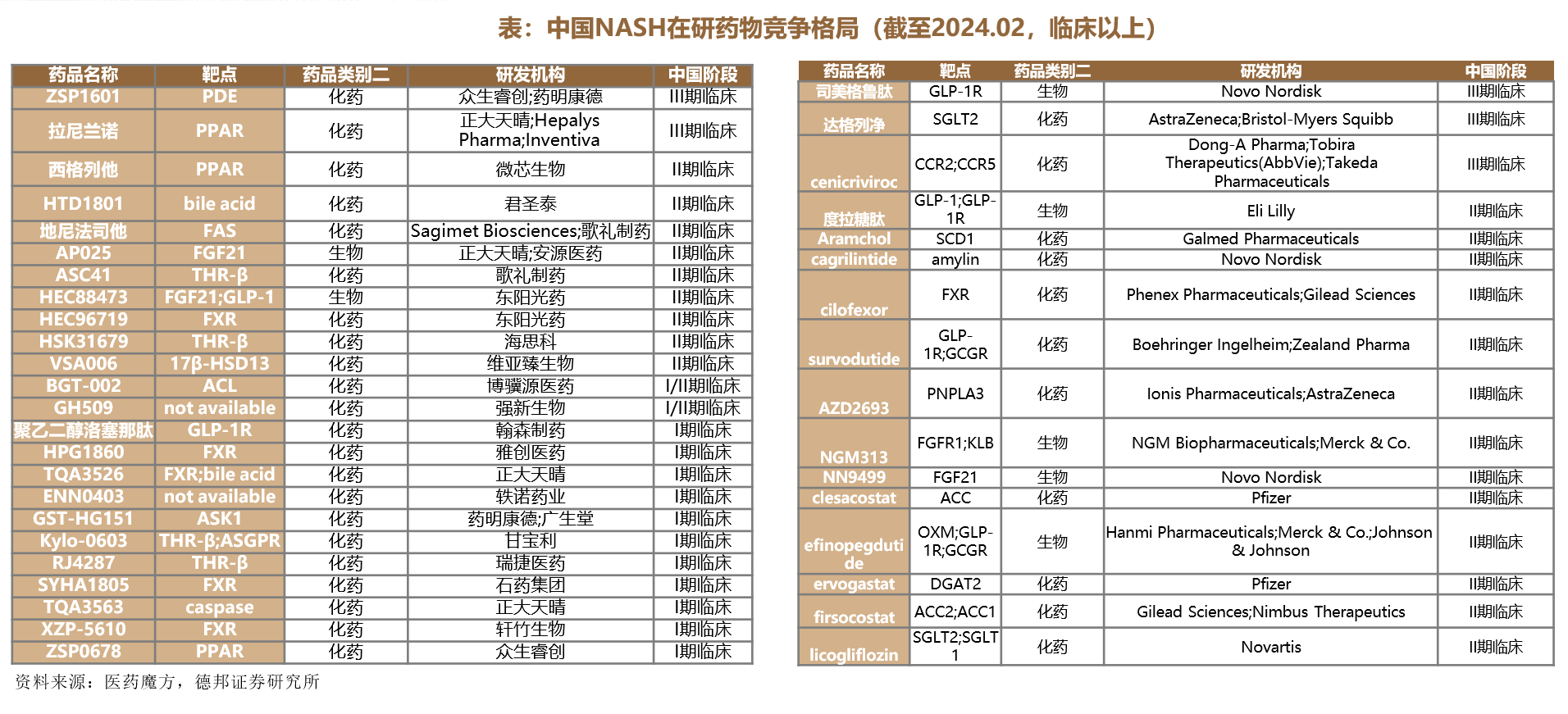
04 风险提示
1. 临床研发失败风险
创新药研发II期到III期阶段因为疗效不及预期而失败的比例较高,III期由于受试者的数量增多,以及临床试验过程中的影响因素增多,可能导致临床数据不及II期而研发失败。
2. 竞争格局恶化风险
我国创新药研发靶点扎堆现象严重,同质化竞争可能导致产品商业化价值的萎缩。
3. 销售不及预期风险
产品销售受到本身特性,竞争格局,销售队伍,行业发展等多方面因素影响,存在销售不及预期风险。
4. 行业政策风险
随着进入医保的创新药品种增多加之近几年疫情的支出影响,医保基金的压力逐年增加,可能导致药物的谈判价格不及预期,存在受到行业政策或监管政策影响的风险。
免责声明:本文系本网编辑转载,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。如涉及作品内容、版权和其它问题,请在30日内与本网联系,我们将在第一时间删除内容。
本文作者可以追加内容哦 !

