
亨廷顿疾病(Huntington’s disease, HD)是一种遗传性神经退行性疾病,由单个基因Huntingtin(HTT)缺陷导致,其特征是运动控制丧失以及认知能力和情绪稳定性的下降,常表现为不自主的舞蹈动作,因此又名亨廷顿舞蹈病。该病遗传方式是显性遗传,HTT基因的一个特定区域(CAG重复区)会异常扩展,该片段编码一个长度可变的ployQ链。当这个polyQ链长度超过35个重复时,会导致蛋白质功能异常,进而损害脑细胞。更长的polyQ链倾向于形成寡聚体(oligomers)、聚集体(aggregates)和包涵体(inclusion bodies),这些结构的形成被认为是导致神经毒性的源头。关于HD发病机制还有另外一种假说,CAG重复序列可能通过RNA层面的毒性作用影响疾病的发展。虽然已知突变型mHTT蛋白会产生聚集,但聚集与神经毒性之间的联系仍不清楚。
近日,来自美国斯坦福大学的Judith Frydman课题组在Nature Cell Biology上发表了研究论文Polyglutamine-mediated ribotoxicity disrupts proteostasis and stress responses in Huntington’s disease。在本研究中,作者探讨了HTT蛋白翻译和聚集的调控机制,发现了CAG扩展的突变体HTT蛋白通过核糖体毒性导致翻译过程中的过早终止,从而释放出易于聚集的mHTT蛋白,并进一步破坏细胞内蛋白质稳态和应激功能。这些发现不仅加深了科学家对HD发病机制的理解,也为其治疗提供了潜在的干预方案。

在人类和小鼠的HTT mRNA的5’非编码区中存在着一个保守的上游开放阅读框(uORF),uORF位于主要的ORF之前可以在mRNA被翻译成蛋白时起到调节作用。作者分析ribo-seq数据时发现uORF和主要的ORF都有核糖体启动,当用cycloheximide(CHX)处理阻断翻译的延长时,核糖体占据了uORF的整个区域,但没有延伸到主要的ORF区域,这表明uORF通过减少主要的ORF翻译启动抑制HTT基因在体内的翻译。而在thapsigargin(Tg)处理诱导应激反应的情况下,大部分mRNA翻译效率下降,但是HTT和另外一种同样含有uORF的Atf4基因在应激条件下却表现出mRNA翻译增强。这表明含有uORF的mRNA在不同情况下与众不同的翻译行为可能对HD的发病机制和疾病进展由重要影响。进一步分析发现uORF是通过调节翻译的起始来控制HTT蛋白的聚集,能够延迟包涵体的形成并减少倾向于聚集的mHTT片段的生成。此外,使用翻译起始抑制剂4EGI-1可以进一步减少这些神经毒性片段的产生,并在动物模型中改善症状。
接下来,作者研究了polyQ序列对HD疾病发展的作用。他们利用一种病毒载体来表达、标记并检测细胞中HTT新生链,研究发现polyQ链的扩展增加了核糖体碰撞和过早终止的风险,从而导致了聚集倾向的mHTT片段的释放。在翻译具有更长polyQ链的mHTT蛋白时,会招募更多的翻译质量控制(ROC)和蛋白质量控制(PQC)因子,特别是蛋白酶体与清除mHTT相关的因子。与此相反的是翻译延伸因子eIF5A在翻译mHTT蛋白时的显著减少,其与mHTT的相互作用可能导致聚集并影响神经功能。同时,随着HD小鼠模型年龄的增长,eIF5A的变化与疾病的症状恶化相关联,表明核糖体碰撞和相关的泛素化降解可能是HD神经退行的关键因素。更加重要的是,作者还发现mHTT与eIF5A相互作用并阻隔其功能,改变了数百种mRNA上的翻译延伸,进而破坏了蛋白质稳态,这一过程形成了蛋白质稳态功能障碍的恶性循环,因此可能加剧了HD的症状。
为了证实作者这一发现的可能性,研究人员随后探讨了HD中细胞如何响应由polyQ扩展引起的内质网应激和折叠错误蛋白质反应。研究发现,HD细胞在处理蛋白质折叠错误的应激时存在缺陷,这种应激反应引起了翻译启动因子eIF2a的磷酸化,以及由此诱发的整合应激反应。尤其是mHTT导致的eIF5A减少妨碍了保护性因子的有效翻译,通过补充eIF5A可以在一定程度上提高HD细胞在内质网应激下保护因子的表达。作者认为通过减少eIF5A的丢失或增加其活性可以作为治疗HD的潜在策略。
最后,作者认为如果mHTT使细胞对应激反应更加敏感,那么HD细胞对增加核糖体碰撞的药物就会特别敏感,这些药物通过减慢翻译延伸来触发核糖体碰撞。然而,这些细胞对通过减慢翻译启动的药物反应较弱,因此降低翻译启动速率可以减少核糖体碰撞和过早终止。这些结果说明在HD细胞中,通过调节翻译启动与延伸的平衡,可以潜在的减轻病理状态下核糖体碰撞和相关的应激反应,这为HD治疗提供了可能的干预途径。
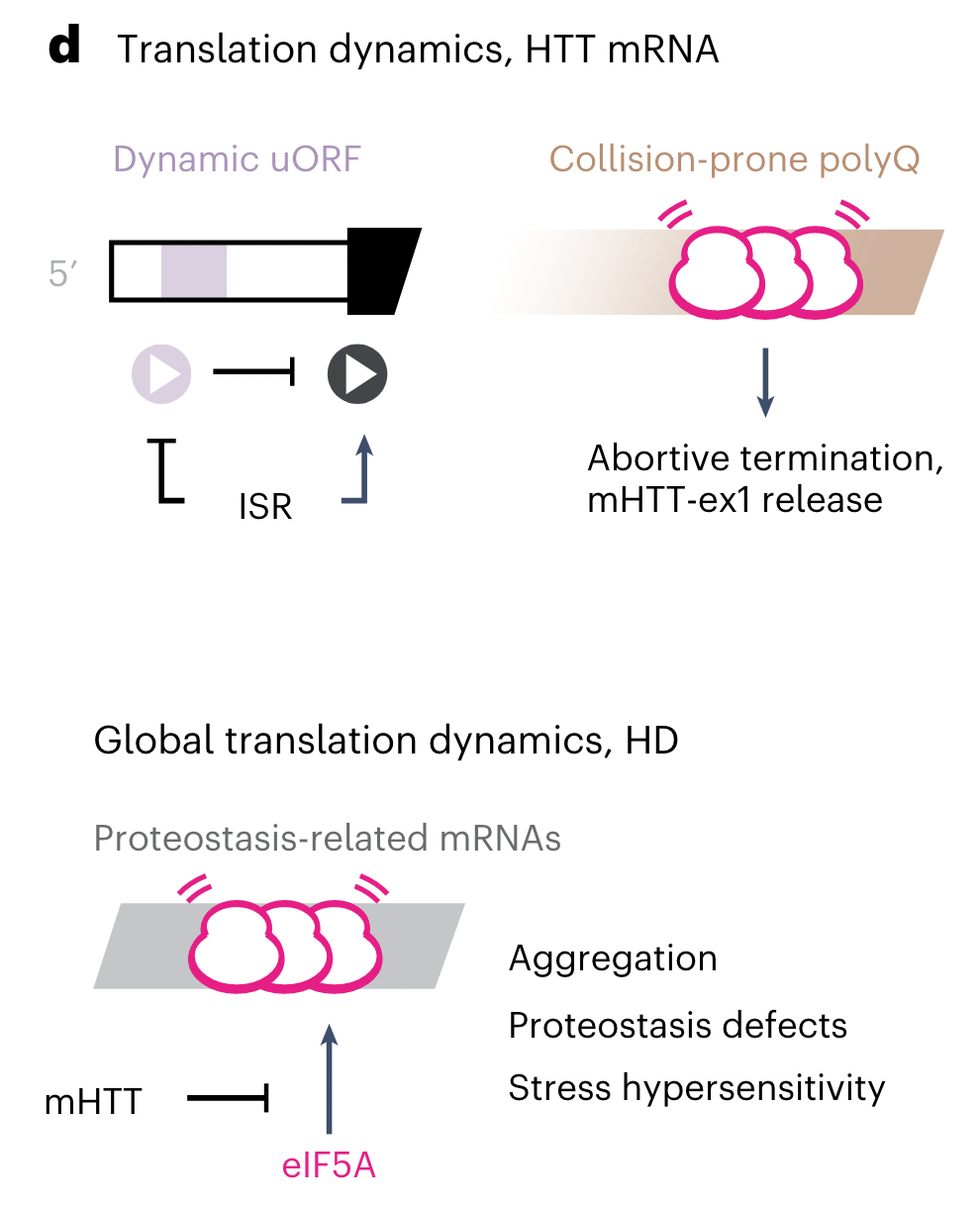
总的来说,这篇文章发现了降低mHTT水平和对抗其细胞毒性的靶点,CAG扩张会因核糖体碰撞而导致翻译终止,释放出具有神经毒性的mHTT片段,从而通过聚集隔绝eIF5A和其他蛋白质质量控制因子,导致神经元细胞蛋白质稳态障碍,抑制保护性应激反应的诱导。这些发现将有助于指导HD疾病治疗,提供了全新的干预策略。
本文作者可以追加内容哦 !

