
研究介绍
•
研究背景
Background
地塞米松(Dexamethasone,DXMS)是糖皮质激素(GC)的一种,具有抗炎、抗内毒素、抑制免疫、抗休克及增强应激反应等药理作用。于1957年首次合成,并列名于世界卫生组织基本药物标准清单之中,为基础公卫体系必备药物之一。
2020年6月,COVID-19 治疗随机评估 (RECOVERY) 平台试验的初步数据表明,地塞米松可挽救 COVID-19 重症患者生命,可将需要机械通气的重症 COVID-19 患者的 28 天死亡相对风险降低约 30%,对于仅吸氧的患者,可将其死亡率降低约20%。1
尽管地塞米松的临床有效性已得到证实,但仍有大量患者的病情发展为危重并最终死于 COVID-19,这些患者对地塞米松的治疗反应显然无效或几乎无效。总体而言,地塞米松在重症 COVID-19 中的作用机制尚不清楚,并且缺少治疗反应或治疗失败的生物标志物,治疗失败的案例无疑强调了寻找地塞米松挽救生命相关的分子标志的重要性。
研究意义
Significance
来自德国神经退行性疾病研究中心和柏林夏里特医学院的研究人员,在期刊《Cell》发表新的研究成果,“The life-saving benefit of dexamethasone in severe COVID-19 is linked to a reversal of monocyte dysregulation”。
研究结果将地塞米松的作用与特异性免疫调节和单核细胞失调的逆转联系起来,并强调了单细胞组学在监测体内免疫调节药物靶向作用和为精准医学方法中的患者分层提供依据方面的潜力。2(图1)
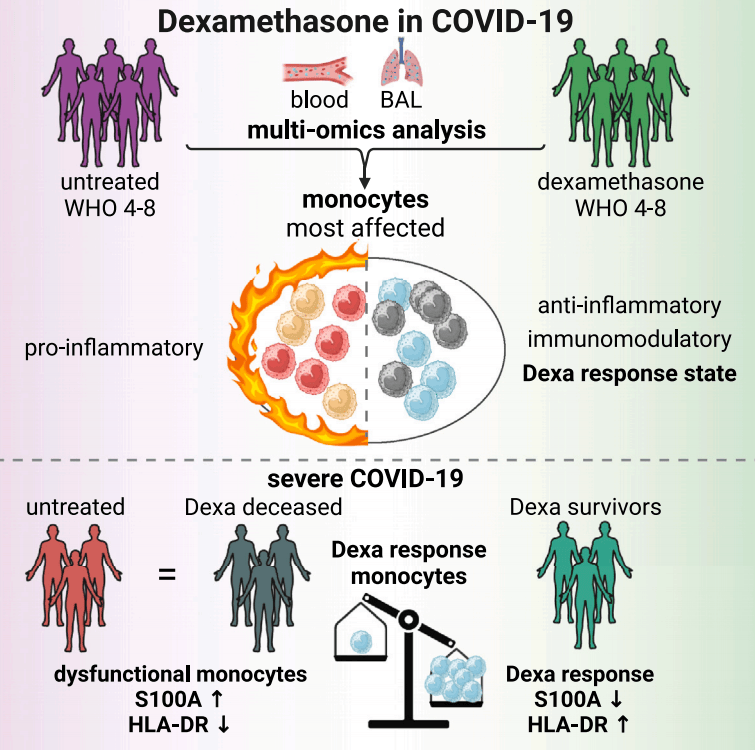
图1
研究方法
•
研究亮点
1、单细胞转录组测序(scRNA-seq):
用于识别地塞米松治疗引起的单核细胞状态的特定变化,并分析其与临床结果的关联。
2、质谱流式检测(CyTOF):
区分和量化血液中的各类免疫细胞,包括它们的数量和比例,以及它们在地塞米松治疗前后的变化。
3、基因富集分析(GSEA)和基因集变异分析(GSVA):
用于分析全血转录组数据,以确定与地塞米松治疗反应相关的基因集,并评估治疗效果。
研究发现
•
一、地塞米松治疗引出的免疫调节
为了确定地塞米松治疗在 COVID-19 患者中诱导的细胞和分子变化,研究人员选取2020年3月至2021年2月期间感染SARS - CoV - 2 D614G毒株的COVID - 19患者,分为地塞米松治疗组(Dexa)和未治疗的对照组(ctrl.),利用CyTOF、scRNA-seq和多色流式细胞术,对全血和外周血单核细胞(PBMCs)进行高维单细胞分析。
地塞米松治疗组中,白细胞的数量显著增加,特别是中度疾病患者。这种增加主要是由于B细胞和中性粒细胞的变化,而在重度疾病患者中则没有观察到差异。此外,单核细胞的比例在中度疾病患者中相对减少。通过使用CyTOF和scRNA-seq技术,研究人员能够观察到免疫细胞组成的整体变化,地塞米松治疗引起了转录改变,在单核细胞和B细胞中最为明显,且许多与地塞米松治疗相关的基因上调,同时一些与炎症相关的基因表达下调。(图2)
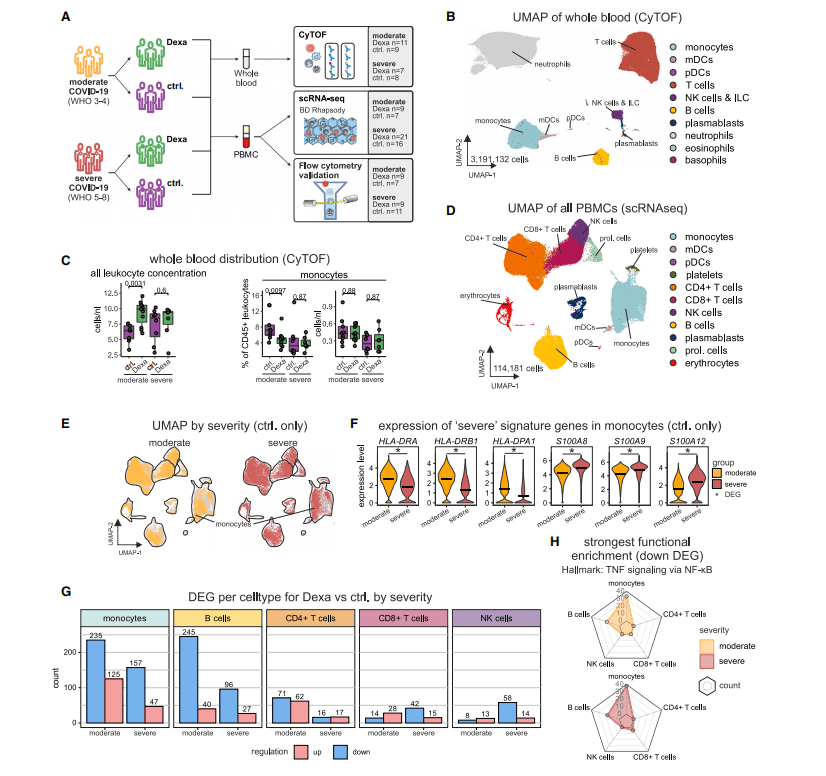
图2
二、地塞米松诱导的独特细胞状态
研究人员比较了地塞米松治疗组与对照组的重度和中度COVID-19患者单核细胞中的差异表达基因(DEGs)。观察到地塞米松治疗抑制了几种促炎基因的表达,并诱导了与疾病严重程度无关的包括已知 GC 反应在内的基因程序,例如 IL1R2、TSC22D3、CD163等。
此外,研究人员还发现了一个特定的单核细胞亚群,表现出最高的糖皮质激素反应基因的富集,这表明地塞米松治疗在单核细胞中引起了特定的分子变化。(图3)
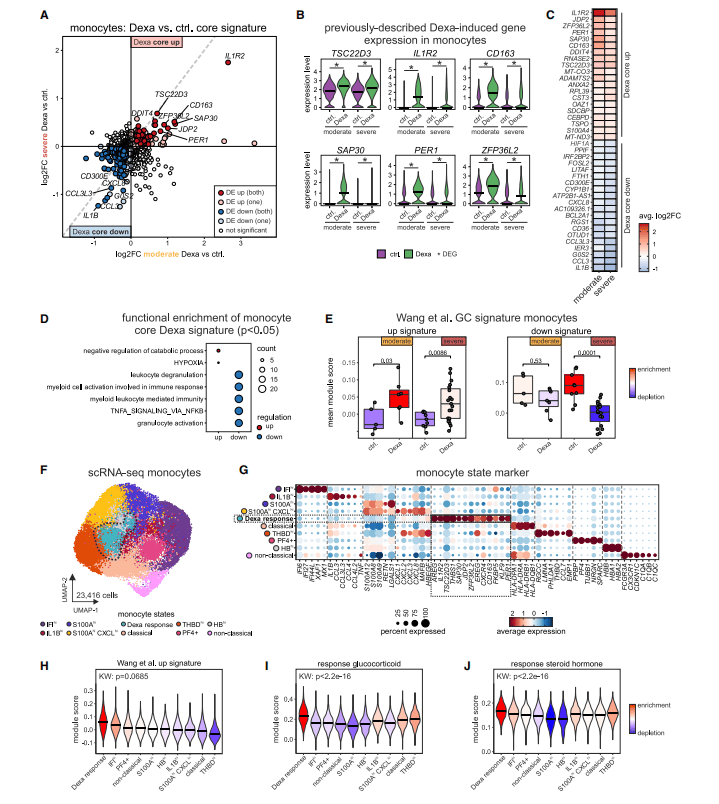
图3
三、与临床生存率相关的诱导调节
鉴于仍有部分患者接受地塞米松治疗后无效,研究人员试图探究哪些机制有助于临床治疗获益。
发现地塞米松在大多数中度COVID-19患者中,普遍诱发Dexa反应单核细胞状态,在重度COVID-19患者中不太明显,相比于重症幸存者,重症死亡患者的Dexa反应状态单核细胞的频率显然更低。地塞米松治疗的临床效果或与单核细胞对治疗的反应有关。
此外,地塞米松治疗逆转了重症COVID - 19患者单核细胞中先前报道的转录失调,使HLA - DRB1、HLA - DRA等基因的表达恢复,S100A等报警素表达下调。在肺部支气管肺泡灌洗液(BAL)的分析中也发现,地塞米松治疗后幸存者的BAL单核细胞和巨噬细胞中也存在类似的转录反应。(图4)
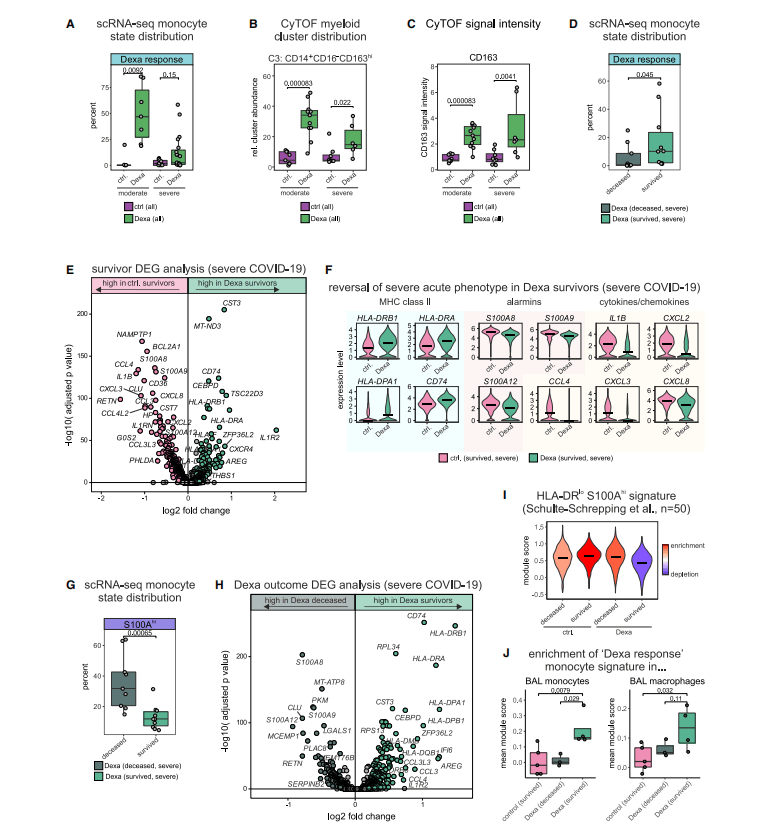
图4
这些数据将药物干预的临床效果与血液和肺部免疫细胞的分子表型联系起来,可以揭示治疗干预的作用机制,并在临床终点之前识别对特定治疗无反应的患者。结果强调了单核细胞反应在严重 COVID-19 病理生理学中的因果相关性。
四、与地塞米松疗效相关的CD14+单核细胞
为了研究在转录水平上观察到的地塞米松治疗反应的差异是否反映在单核细胞的表观遗传谱上,研究人员选取治疗开始时需要补充氧气但无需有创机械通气的患者(WHO评分为4 - 5分),生成治疗反应者和非反应者的血液样本全基因组DNA甲基化谱。
研究人员发现在治疗开始后的早期阶段(中位2天),CD14+单核细胞在促炎程序方面的表观遗传学差异已经显现,且这些差异早于转录变化。以及从单核细胞转录组中获得的与结果相关的特征基因的富集,进一步支持了该基因程序对治疗成功的重要性。(图5)
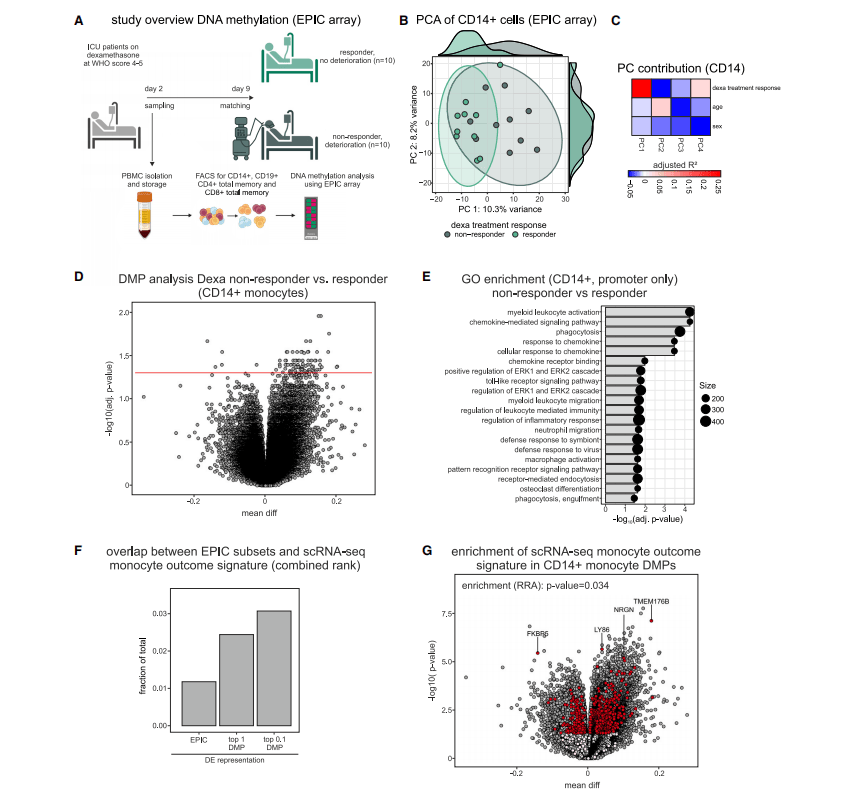
图5
五、全血转录组分析以及分层结果
鉴于明显的与结果相关的转录变化,研究人员对来自两个独立COVID - 19队列(单中心和多中心)的患者进行全血批量转录组分析,以验证地塞米松治疗相关的单核细胞转录特征是否能在全血转录组中体现,并用于分层患者结果。
在平均治疗后4天(单中心队列)和2天(多中心队列)采集的全血转录组中,基于单核细胞转录组的特征基因标志能够富集,并且可以根据疾病严重程度和结果对患者进行分层。
治疗后4天采集的样本中可以检测到单核细胞转录组的临床结果相关基因特征富集;在独立队列中,治疗后2天采集的样本中只能检测到基于下调基因的特征基因的富集,说明地塞米松治疗效果在治疗开始后2至4天之间开始在全血转录组中显现。(图6)
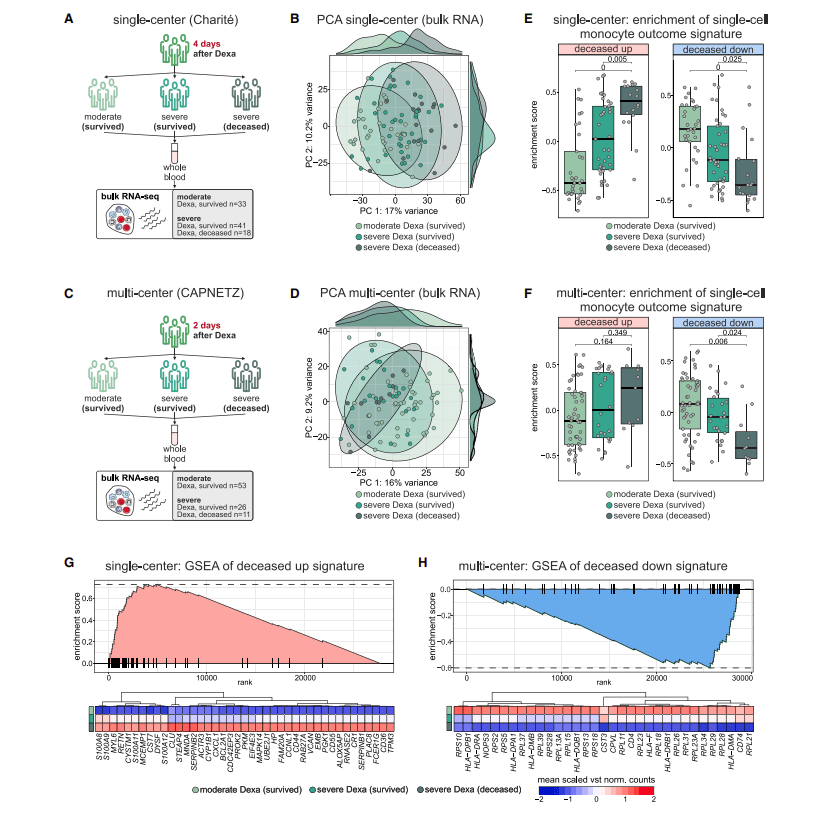
图6
这表明,单细胞测序技术能够揭示药物治疗的体内效应,并且这些分析中获得的基因特征可以应用于更大的临床队列,以在治疗开始后的早期时间点对患者进行分层。
研究讨论
•
研究局限性
1、研究基于两个观察性队列:
并非专门设计用于研究地塞米松治疗效果,且受限于早期疫情阶段,免疫和病毒学特征可能随时间变化。
2、由于伦理原因:
在重症COVID - 19患者中扣留地塞米松是不道德的,难以生成新的数据来进一步验证研究结果。
小结
Summary
这项研究为地塞米松治疗对 COVID-19 患者的免疫调节作用提供了单细胞水平的解析分子表型信息,这些信息可用于未来关于地塞米松治疗重新评估的临床决策。结合基于转录组的反向药物靶点预测方法和随机对照试验,该方法可以为未来新发传染病的更快药物再利用解决方案奠定基础,甚至可能成为开发其他感染性和非感染性疾病精准医学的蓝图。
参考文献
[1] Horby, Peter., Lim, Wei Shen., Emberson, Jonathan R., Mafham, Marion., & Bell, Jennifer L.. (2020). Dexamethasone in Hospitalized Patients with Covid-19. The New England journal of medicine, 384(8), 693-704.
[2] Knoll, Rainer., Helbig, Elisa T., Dahm, Kilian., Bo, Olufemi., & Hamm, Frederik.. (2024). The life-saving benefit of dexamethasone in severe COVID-19 is linked to a reversal of monocyte dysregulation. Cell.
PROFILE
Anna C. Aschenbrenner
波恩大学、德国神经退行性疾病中心(DZNE)预防、衰老和系统免疫学组组长

研究小组使用最新的免疫学、功能基因组学方法和计算机辅助分析高维数据集的方法,借助统计和生物信息学方法进行研究。研究重点是免疫系统的老化过程;感染是免疫系统过早老化的诱因;以及改善免疫系统,防止衰老过程。
END
文案 | 姜笑南
排版 | 姜笑南
审核 | 姜笑南
发布|姜笑南
世界生命科学大会
RECRUIT
关注我们,获取生命科学
学界前沿|促进更多的学术交流与合作
业界前沿|促进更快的产品创新与应用
政策前沿|促进更好的治理实践与发展
本文作者可以追加内容哦 !

