
《港湾商业观察》施子夫 王璐
日前,持续冲刺科创板的武汉禾元生物科技股份有限公司(以下简称,禾元生物)回复了第二轮审核问询函。
2022年末,禾元生物正式递表上交所,保荐机构为海通证券。
在回复第二轮审核问询函时,禾元生物部分更新了2023年经营数据。不过,公司仍未更新招股书,公司招股书仍停留在递表时,这显得并不多见。
禾元生物是一家创新型生物医药企业,拥有植物生物反应器技术平台。公司建立了“一个独特植物表达体系,两个技术平台”的核心技术体系:利用水稻胚乳细胞生物反应器高效重组蛋白表达平台(OryzHiExp)和重组蛋白纯化技术平台(OryzPur),建立了完善的药品、药用辅料及科研试剂的产业化体系。
01
连年亏损,现金流持续为负
第二轮审核问询函提及,根据招股说明书,公司归属于母公司普通股股东的净利润分别为-4993.57万元、-5335.16万元、-1.34亿元和-5829.87万元,截至2022年6月30日,未弥补亏损为4.28亿元。请发行人按照《上海证券交易所科创板股票发行上市审核问答》第2条要求,充分披露最近一期存在累计未弥补亏损的原因分析、影响分析和趋势分析,并结合在研管线研发进度、各项费用的支出规划、预计药品的销售情况等,披露达到盈亏平衡状态时主要经营要素需要达到的水平。
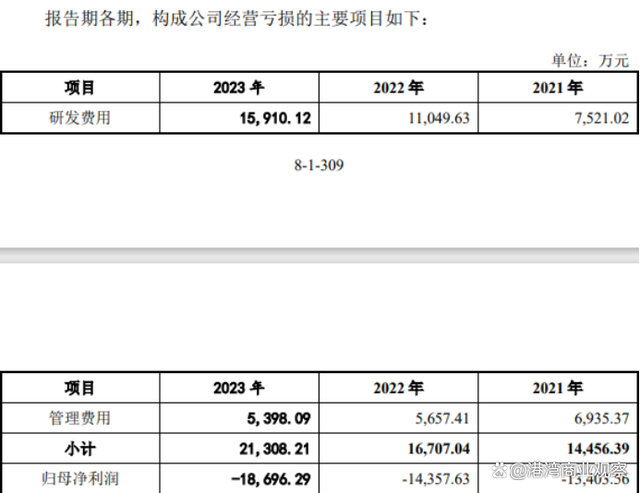
根据禾元生物回复,报告期内公司研发费用及管理费用是导致公司出现持续亏损的主要因素。
公司详细表示,报告期内,公司研发费用主要为药品研发过程中涉及的临床试验及技术服务费、人员薪酬、设备材料费等。随着公司新药研发管线不断推进、研发人员规模不断扩大,公司研发开支持续增长。公司管理费用主要为专业服务费、职工薪酬、折旧摊销费。其中专业服务费主要包括诉讼费和咨询服务费,2021年,公司聘请境外律师积极应对337调查导致诉讼费大幅增加;2021年,公司进行了股权融资并聘请中介机构准备首发上市事宜,发生了较多咨询服务费支出。
同时,公司药品尚未获批上市销售,营业收入主要来源于药用辅料、科研试剂的销售,营收规模相对较小,暂无法弥补上述大额开支,导致报告期内公司处于持续亏损状态。综上所述,公司尚未盈利且最近一期存在累计未弥补亏损系经常性因素导致,符合创新药研发企业的特征。
2021年-2023年,禾元生物归母净利润分别为-1.34亿元、-1.44亿元和-1.87亿元。看起来,公司的亏损态势仍在扩大。
同一时期,公司经营活动产生的现金流量为-8797.24万元、-6640.34万元及-1.23亿元;投资活动产生的现金流量为-1.75亿元、-3.58亿元及-1.02亿元。截至2023年12月31日,公司账面货币资金余额合计2.36亿元,目前持有的货币储备足以保障公司核心产品HY1001完成III期临床研究并递交注册申请。
02
HY1001预计2025获批上市,2027盈利
禾元生物表示,公司HY1001项目已完成III期临床试验,研究结果显示其已达到主要和次要临床研究终点,展现出良好的安全性。公司已于2024年6月完成了与CDE的Pre-NDA沟通会议,CDE认为HY1001具有明显临床价值,符合优先审评审批纳入条件,目前公司正在按照优先审评审批要求准备注册资料。公司将加快推进HY1001项目新药注册申请,推动核心产品植物源重组人血清白蛋白获批上市销售。
据招股书显示,公司在研产品植物源重组人血清白蛋白注射液(OsrHSA,HY1001)是利用水稻胚乳细胞表达,经提取、纯化的重组人血清白蛋白产品。于2017年4月获得国家食品药品监督管理总局(现为国家药品监督管理局)颁发的《药物临床试验批件》,2019年11月获得《临床试验通知书》同意变更I期临床试验方案。2019年8月获得美国FDA批准进入临床研究;2020年7月在美国完成I期临床研究。2022年12月,HY1001已经完成II期临床试验,达到主要临床研究终点。HY1001的注册分类为:治疗用生物制品1类。
根据沙利文数据分析,2020年,中国人血清白蛋白药物市场规模达到258亿元人民币,2025年预计达到425亿元人民币,复合年均增长率10.5%,2030年市场规模预计570亿元人民币,2025年至2030年复合年均增长率6.0%。截至本招股说明书签署日,国内市场尚无重组人血清白蛋白上市药品,公司的植物源重组人血清白蛋白注射液目前已完成国内开展的III期临床试验。
禾元生物回复审核问询函表示,根据研发计划,HY1001预计将于2025年获批上市,将成为首批上市的重组人血清白蛋白药物,产品预计潜在市场空间大。结合发行人在研管线进度、各项费用的支出规划、预计药品的销售情况等因素,在满足以下测算假设及要素分析的前提下,预计2027年实现盈利。
03
337调查对技术不存在不利影响?
此外,审核问询函还提及,根据首轮回复,发行人与 Ventria Bioscience 存在知识产权纠纷。Ventria Bioscience 向美国国际贸易委员会提出对发行人的 337调查申请,并在堪萨斯州地方法院提起相关诉讼,目前尚未结案。请发行人说明:上述事项最新进展情况,对公司相关技术产品的影响。
2023年5月,发行人就337调查终裁结果向美国联邦巡回上诉法院提交了上诉状。2023年6月,美国联邦巡回上诉法院批准了美国国际贸易委员会(以下简称“ITC”)延期至2023年7月31日提交上诉答辩状的申请。截至本回复出具日,ITC已向美国联邦巡回上诉法院递交了答辩状,Ventria Bioscience作为诉讼参与人向美国联邦巡回上诉法院递交了其对诉讼标的享有权利或利益的证明文件,该案件仍处于审理阶段。截至本回复出具日,堪萨斯州诉讼仍处于中止审理状态。
2024年3月,发行人向美国特拉华州联邦地区法院提起诉讼,指控Ventria Bioscience开发、生产、销售植物源重组人血清白蛋白产品的行为侵犯发行人多项美国专利,并要求其支付利润损失、赔偿金、利息和维权支出等。2024年5月,Ventria Bioscience对发行人的起诉进行应诉并提起反诉。同月,发行人提交反诉答复,特拉华州法院正式签发案件排期令(Scheduling Order)。截至本回复出具日,法院尚未作出判决。
禾元生物认为,公司主要系通过自主研发不断积累并形成核心技术,合法拥有核心技术的相关知识产权,核心技术来源清晰,合法合规,发行人积极通过法律手段保护知识产权,该诉讼事项对公司相关技术不存在不利影响。(港湾财经出品)
本文作者可以追加内容哦 !

