
9月4日,IN8bio在提交给美国证券交易委员会的文件中表示,其正在纽约市和阿拉巴马州伯明翰的工厂裁减约49%的员工。同时,在执行管理团队和公司董事会实施11%的现金薪酬削减计划,以保留其现金资源,优化资源配置。IN8bio预计与此次裁员相关的一次性成本约为30万美元,其中几乎全部都是与遣散费相关的现金支出,这些成本将在2024年第三季度发生。
IN8bio是一家临床阶段生物制药公司,专注于发现、开发和商业化用于实体瘤和血液瘤的- T细胞疗法。当前该公司的管线包括:用于治疗恶性胶质母细胞瘤 (GMB)的INB-200、INB-400和用于治疗治疗白血病的INB-400等。
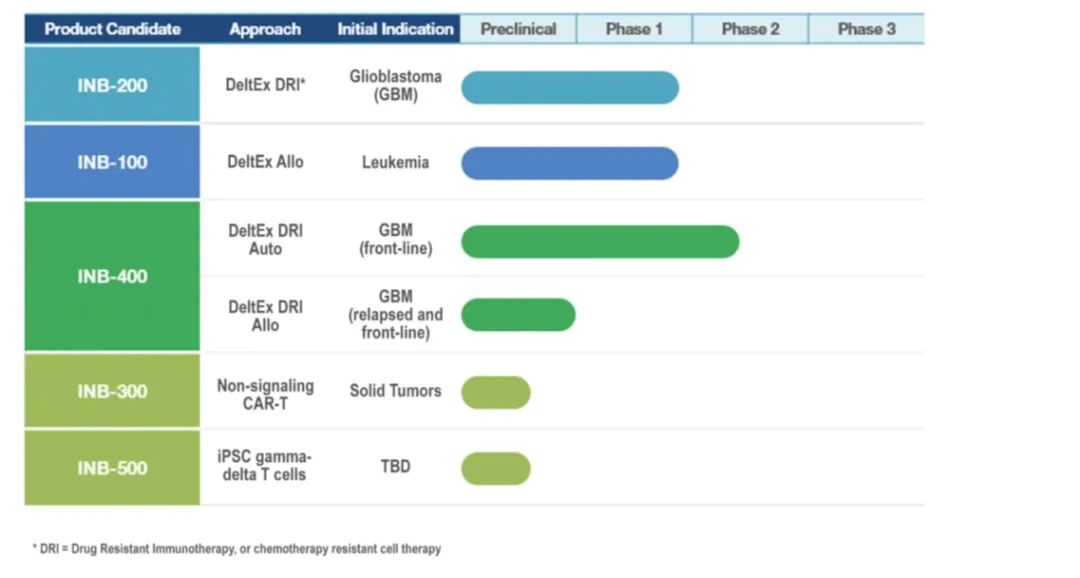
IN8bio 现有管线,数据来源:IN8bio 官网
据IN8bio 2024年上半年财报显示:上半年,IN8bio 累计净亏损额为1720万美元;截至6月30日,公司现金流仅为1020万美元。
另外,IN8bio 还在提交给美国证券交易委员会的文件中称,公司将进行管道优先级排序,包括将专注于INB-100;暂停两项胶质母细胞瘤(GBM)项目INB-200和INB-400,停止INB-200的开发,暂停INB-400的患者入组,只继续对INB-200 1期临床和INB-400 2期临床的参与者进行监测。另外,该公司将探索实体瘤项目的潜在合作机会。
其中,INB-200已完成患者治疗,最多重复六次给药;去年4月,INB-400被FDA授予了孤儿药称号,这是第一个获得FDA该称号的转基因T细胞疗法。
而将重点关注的INB-100是一款来自健康供体的同种异体 T细胞,在体外经过扩增和激活后,被输注到白血病患者体内。在2023年欧洲血液与骨髓移植学会年会上,IN8bio宣布其INB-100在1期临床中,实现了100%的完全缓解(CR)。
此外,迄今为止,INB-100两项试验的患者都超过了预期的无进展生存期(PFS);截至2024年8月1日,自美国临床肿瘤学会(ASCO)和欧洲血液学协会(EHA)年会提供的临床更新以来,尚未报告新的复发病例。
为了证实观察到的无复发生存期和总生存期的改善,并进一步降低未来注册随机对照试验的风险,IN8bio将寻求增加一个对照组,对白血病患者进行前瞻性评估,并对接受INB-100治疗的患者与只接受标准单倍体移植的患者进行比较。而预期的临床成本节约及裁员就是为了扩充现金流,实现以上计划。
值得注意的是,在文件中,IN8bio称:“如果无法及时获得额外资本,或者根本无法获得额外资金,公司将不得不大幅推迟、缩减或停止其研发计划。如果公司无法继续作为一家持续经营的企业,它可能不得不终止其业务并处置其资产,其实现的价值可能大大低于其简明财务报表中所列的价值。”
2023年12月,IN8bio还与若干以医疗保健为重点的机构投资者签订了一份证券购买协议,完成了4690万美元的私募融资。
本文作者可以追加内容哦 !

