美国《生物安全法》未被纳入美参议院《2025财年国防授权法案》
美国参议院官网显示,当地9月19日,针对中国部分生物公司的《生物安全法》未被纳入美国《2025财年国防授权法案》。
《国防授权法案》(NDAA) 是一项美国联邦法律,每年通过一次,用于规定美国国防部的预算、支出和政策。这项法律是决定国防资金如何分配的重要依据,同时确定了军事项目的优先事项和美国的国防战略。
CDMO圈里的 “东北王”
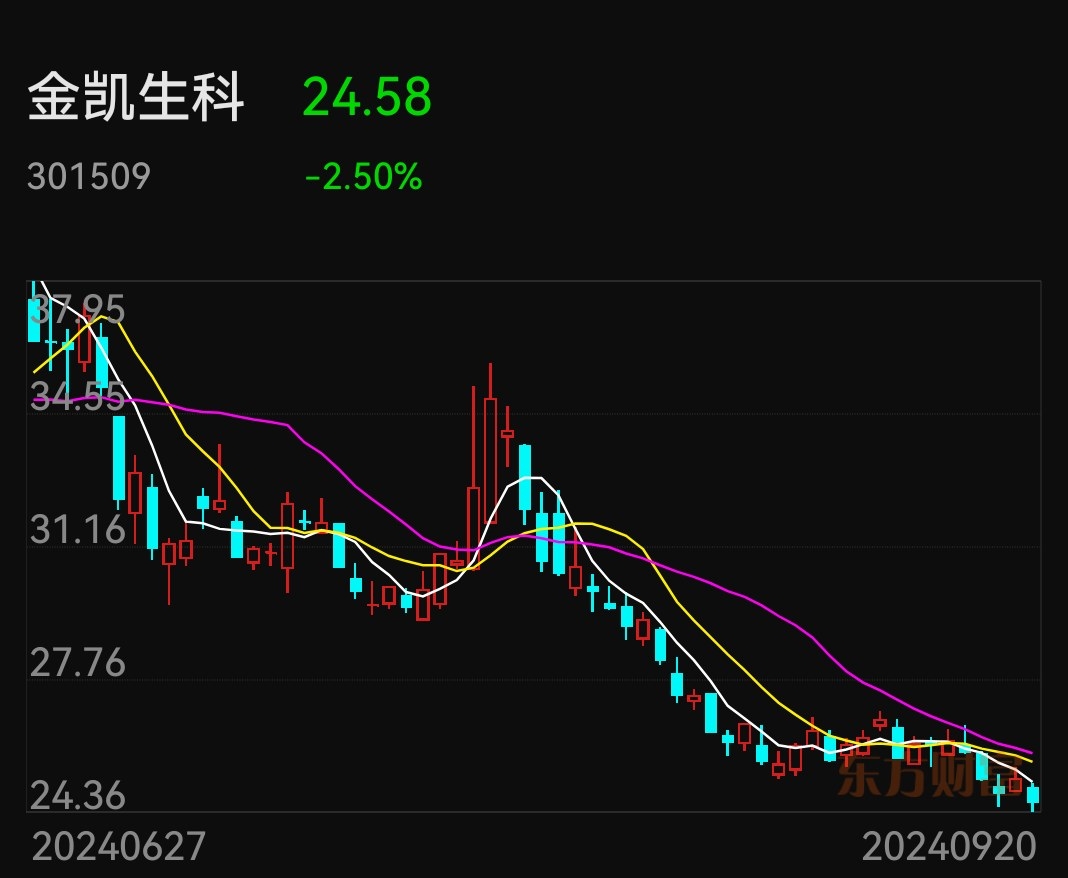
。2023年东北黑土地上诞生了一家CDMO上市企业,为荒漠添了一份绿,这就是金凯生科。公司客户包括拜耳、强生、诺华、赛诺菲、吉利德、阿斯利康、辉瑞、默克、GSK、礼来、武田、勃林格殷格翰等大型MNC,也有Concert Pharmaceutical、Biogen、Principia、Seattle
Genetics 等特色治疗领域的创新药企业。此外,IPO募资12亿元也是主要用于医药项目。
针对中国部分生物公司的《生物安全法》未被纳入美国《2025财年国防授权法案》。$金凯生科(SZ301509)$
《国防授权法案》(NDAA) 是一项美国联邦法律,每年通过一次,用于规定美国国防部的预算、支出和政策。这项法律是决定国防资金如何分配的重要依据,同时确定了军事项目的优先事项和美国的国防战略。
CDMO圈里的 “东北王”
。2023年东北黑土地上诞生了一家CDMO上市企业,为荒漠添了一份绿,这就是金凯生科。公司客户包括拜耳、强生、诺华、赛诺菲、吉利德、阿斯利康、辉瑞、默克、GSK、礼来、武田、勃林格殷格翰等大型MNC,也有Concert Pharmaceutical、Biogen、Principia、Seattle Genetics 等特色治疗领域的创新药企业。此外,IPO募资12亿元也是主要用于医药项目。
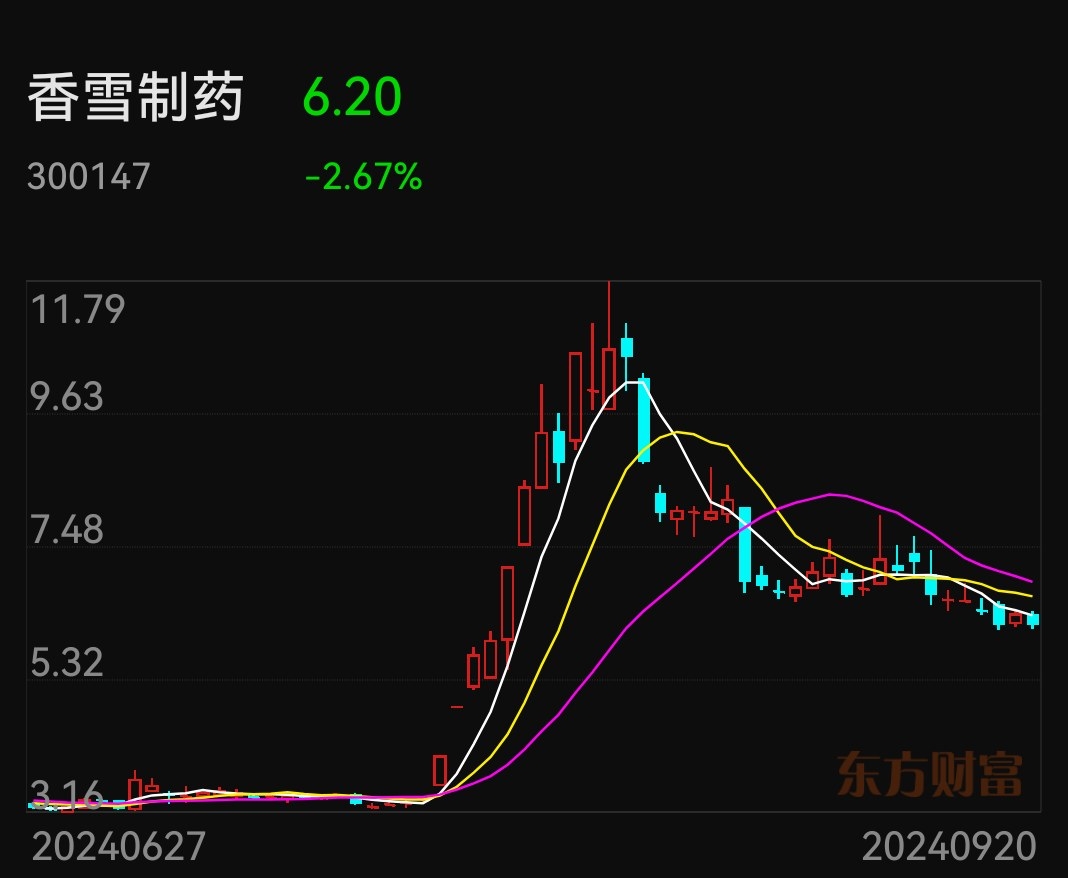
香雪制药的TAEST16001注射液已经在中国完成了I期和II期临床试验的第一阶段,并且已经在美国获得了IND批件,正在进行临床试验。以下是关于TAEST16001的相关信息:
TAEST16001简介
作用机制:TAEST16001是一种TCR-T细胞免疫治疗产品,通过基因工程改造患者的T细胞,使其能够特异性识别并攻击肿瘤细胞。
适应症:主要用于治疗组织基因型为HLA-A*02:01,肿瘤抗原NY-ESO-1表达为阳性的实体瘤,特别是晚期软组织肉瘤。
临床试验进展
I期和II期临床试验结果:TAEST16001在I期临床试验中显示出良好的安全性和耐受性,肿瘤客观缓解率达到41.7%。在II期临床试验中,最佳缓解率为50%,中位无进展生存期(mPFS)为5.9个月。
国际认可:TAEST16001的I期临床试验结果在2022年美国临床肿瘤学会(ASCO)年会上进行口头专题汇报,并发表于国际著名期刊Cell Reports Medicine。2024年6月,II期临床试验阶段性总结数据再次入选ASCO年会。
突破性治疗品种地位
中国:2024年7月30日,TAEST16001注射液被中国国家药品监督管理局(NMPA)药品审评中心纳入突破性治疗品种名单,这标志着该药物在加快关键性临床试验和附条件批准上市方面取得了重大突破。
香雪制药的TAEST16001注射液在治疗晚期软组织肉瘤方面显示出良好的安全性和疗效,其临床试验结果得到了国际顶级学术会议的认可。如果TAEST16001能够成功上市,将为中国乃至全球的肿瘤患者提供新的治疗方案。港股CRO概念股尾盘飙升 发生了什么?
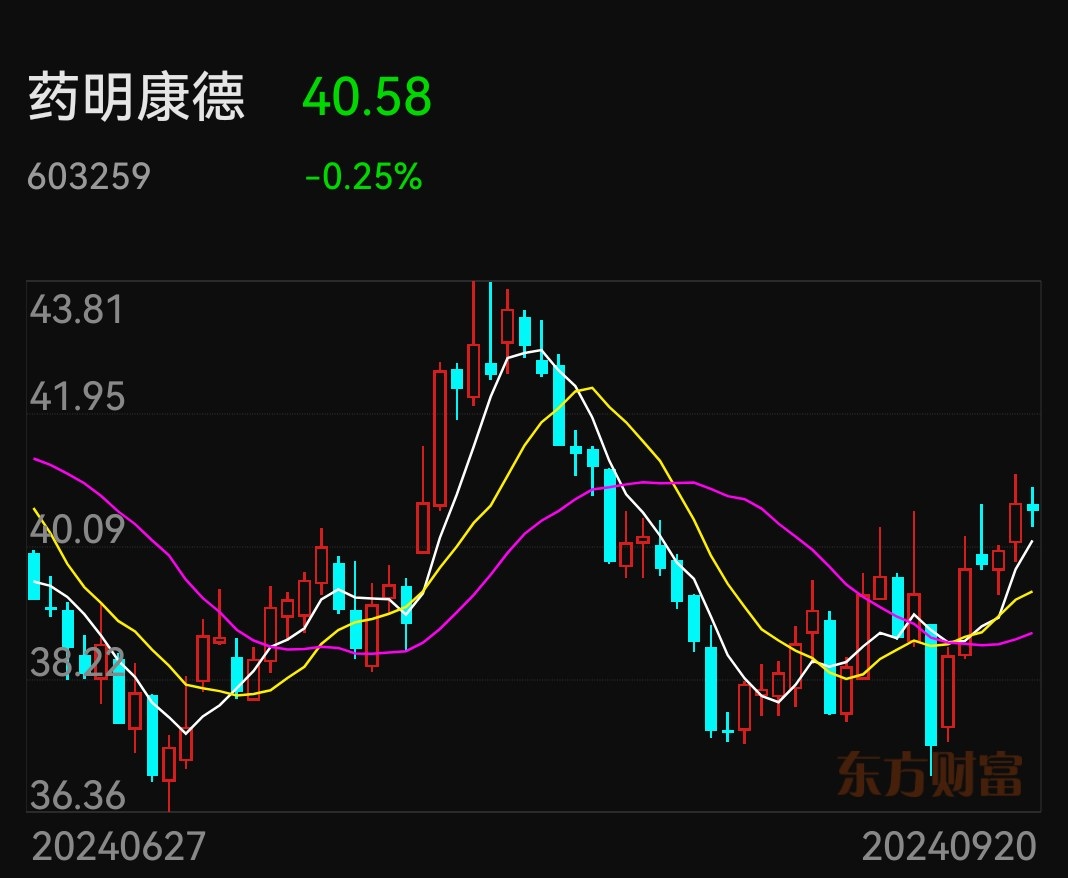
9月20日下午,港股CRO概念股尾盘飙升,截至收盘,药明康德涨11.7%,此前一度涨超15%,药明生物涨10.4%,康龙化成涨12.87%,泰格医药、昭衍新药、凯莱英等跟涨。
有市场消息称,美国参议院发布了ndaa(《国防授权法案》)终稿,本次ndaa实际纳入修正案93个,但并未包含s.amdt.2166(生物安全提案)。(来源:新华财经)$药明康德(SH603259)$
本文作者可以追加内容哦 !


