博安生物纳武利尤单抗注射液I期临床药代动力学比对研究结果发表于《BioDrugs》
博安生物 2024年10月19日 10:07 北京 1人听过
近日,由博安生物自主开发的纳武利尤单抗注射液(BA1104,曾用项目号:LY01015)的I期临床药代动力学比对研究结果在国际期刊《BioDrugs》上发表,为全球首个披露Ⅰ期临床药代相似性结果的欧狄沃(Opdivo)的生物类似药。

论文发布网址:https://doi.org/10.1007/s40259-024-00679-w
纳武利尤单抗是一种针对细胞表面程序性死亡-1(PD-1)受体的人源化单克隆免疫球蛋白IgG4抗体,通过解除肿瘤细胞对免疫细胞的免疫抑制,恢复机体免疫应答,发挥抗肿瘤作用,并延长患者生命周期。以其为代表的肿瘤免疫疗法已成为全球范围内肿瘤治疗的主要手段之一,持续呈现出广阔的临床应用价值。
该Ⅰ期临床研究为在中国男性健康受试者中比较BA1104和欧狄沃的药代动力学特征、安全性、耐受性和免疫原性的随机、双盲、单次给药、平行对照的研究。共有176例受试者以1:1的比例随机接受0.3mg/kg BA1104或欧狄沃单次静脉输液。该研究中药代动力学的主要评价指标为AUC0-∞,次要评价指标为AUC0-t和Cmax,此外还有安全性评价和免疫原性评价指标。
研究结果表明:BA1104和欧狄沃两组之间的AUC0-∞、AUC0-t及Cmax指标符合等效标准,说明两者药代动力学特征相似。此外两者的安全性和免疫原性也高度相似。
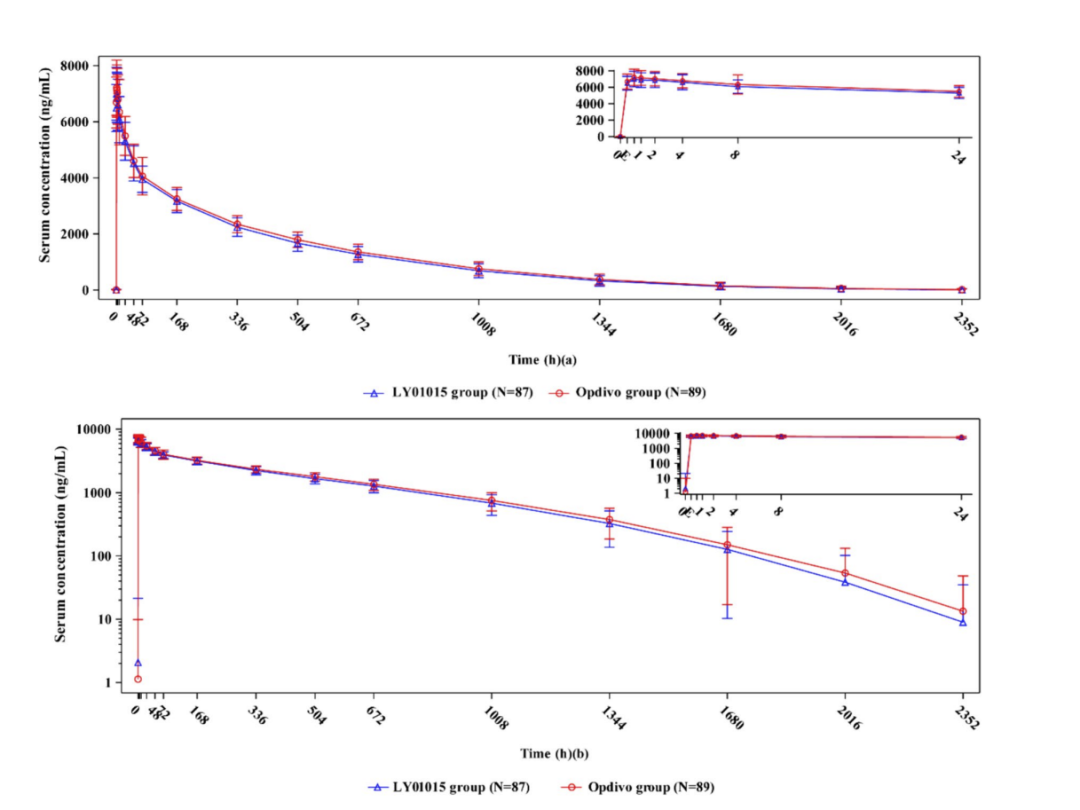
图:平均血清浓度-时间线性图(a)和半对数图(b)。LY01015组(蓝线)和Opdivo组(红线)。数据以平均值标准差的形式呈现。E表示输液立即结束。
博安生物研发总裁兼首席运营官窦昌林博士表示:

“基于博安生物自主知识产权的创新药发现平台,博安生物开发了一系列肿瘤治疗药物,全面布局‘肿瘤免疫+ADC’产品组合,将探索BA1104与公司其它在研肿瘤创新药的联合治疗潜力,包括CD25、CEA/CD3、Claudin 18.2、CD228等靶点,以改善现有标准疗法的治疗效果。”
BA1104的开发进度处于国际领先,为全球首个启动III期临床试验的欧狄沃的生物类似药。目前III期临床研究正在有序进行,该研究为一项随机、双盲、多中心试验,旨在比较BA1104与欧狄沃分别联合化疗药物治疗晚期复发性或转移性食管鳞癌患者的有效性、安全性和免疫原性。根据中、美、欧药品监管机构的生物类似药相关指南,BA1104在完成III期临床试验后可申请同时获批欧狄沃的全部适应症,包括非小细胞肺癌、头颈部鳞状细胞癌、胃或胃食管连接部腺癌、恶性胸膜间皮瘤和尿路上皮癌等十余种肿瘤。BA1104的早日上市将有助于解决未满足的临床需求,可显著提高患者用药可及性。
关于博安生物
博安生物(6955.HK)是一家全面综合性生物制药公司,专业从事生物药开发、生产和商业化,专注于肿瘤、自身免疫、眼科和代谢疾病。公司的新药发现活动围绕多个平台展开,包括全人抗体转基因小鼠及噬菌体展示技术平台、双特异T-cell Engager技术平台、抗体药物偶联(ADC)技术平台及细胞治疗平台。
博安生物拥有完整的涵盖抗体发现、细胞株开发、上游及下游工艺开发、分析及生物分析方法开发、技术转移、非临床研究、临床研究、法规与注册及商业化规模生产的全整合型产业链。在细胞治疗领域,博安生物聚焦新一代增强型及可调控T细胞治疗技术,研发更安全、有效、可负担的细胞治疗产品。
目前,博安生物已有三款产品获批上市,以及多个具有国际知识产权保护的创新型生物药和生物类似药的在研产品组合。公司荣获“国家高新技术企业”认定,并拥有“山东省省级新型研发机构”及“山东省工程研究中心”等省级技术平台,并入选国家级专精特新“小巨人”企业。除了在中国,博安生物也在包括美国、欧洲和日本在内的海外市场从事生物药产品开发。基于差异化的产品组合以及不断成熟的商业化能力,博安生物已构建起覆盖“研发-生产-商业化”的全产业价值链运营体系,为其长期的高质量发展奠定坚实基础。
 阅读 550
阅读 550
本文作者可以追加内容哦 !

