10月30日,翰宇药业生产的利拉鲁肽注射液终于迎来了大规模出口发货。据悉,这笔订单是公司于2023年11月3日公告的商业批量订单,金额约为1.03亿元人民币。此外,翰宇药业与Hikma维持长期独家合作关系,未来将根据美国销售市场需求,持续推进后续订单发货,并获得两位数的销售利润分成。无论是创新药还是仿制药,对于当前的医药企业来说,出海已经不是一道“备选题”,特别是对于本身具有出海资质和实力的公司,出海已经成为了一道“必选题”。
不出海
毋宁死的决心
医保政策改革的不断深化,本土药企面临着产品和利润的双重竞争,我国出台了多项政策鼓励中国药企走出国门。放眼全球,未来将有多款药物专利集中到期,且海外庞大的市场规模。摆在本土药企面前的问题不再是“要不要出海”,而是“如何出海”,在这一点上,翰宇药业已经提前交了一份满分答卷。
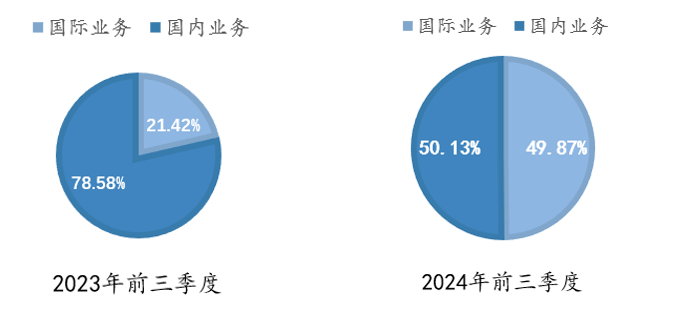
10月29日晚间,翰宇药业(300199)三季度报告披露,前三季度,公司的国际业务收入1.87亿元,同比增长117.53%;国际业务占总营收比重超49%,相较于2023年同期占比21%已经实现飞跃式的增长。其国际订单主要来自美国为首的规范市场以及东南亚等新兴市场,未来还将与合作伙伴一起拓展南美、中东、非洲等机会。
美国是目前全球最大仿制药市场,是全球药企向往之地。这首先得益于美国1984年通过的Hatch-Waxman法案,建立了鼓励药物创新与仿制竞争的双重机制。该法案鼓励仿制药发展,促进仿制药上市并降低药价,开创了简略新药申请(ANDA)、专利挑战及首仿药市场独占期等制度,有效平衡了药物创新与仿制药开发。在仿制药评估、一致性评价、CMC、标签、注册申请及与FDA沟通等主题,FDA发布了一系列指南。
其次,随着2017年中国以成员国身份加入ICH后,与全球法规监管框架趋于一致。中国企业获批美国FDA注射剂ANDA批文数量在2017年之前,一直处于个位数水平,2017年后开始增长至年均约20张批文的水平。2024年6月21日,翰宇药业的利拉鲁肽注射液获得美国首仿药批准(1st Independent Generic),这将在2024年中国仿制药ANDA记录上增添亮眼一笔。对药企而言,选择高标准的美国市场为切入点,并成功打通ANDA审批路径,既是公司国际化的重要证明,也意味着其经验与能力可迅速复制到其他仿制药品种上,企业边际效益得以扩大!
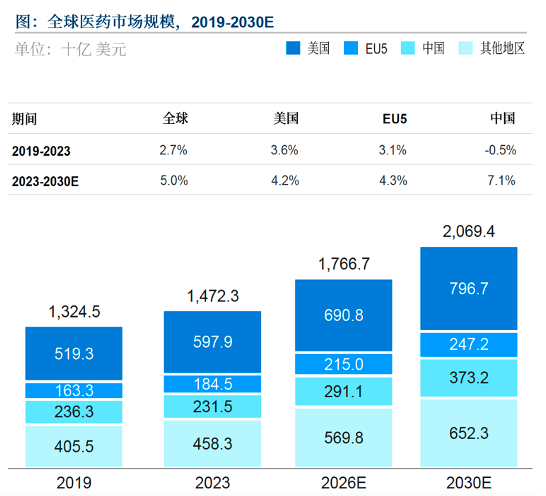
基于 Frost & Sullivan 2024年最新数据显示,2019~2023年,全球医药市场规模以2.7%的年复合增长率从1.32万亿美元,上升至1.48万亿美元,预计到2030年将达2.07万亿美元。医药行业属技术密集型产业,欧美国家凭借先发优势,在医药领域有技术储备,目前主导着全球医药产业。
2023年,美国占全球31.1%(4583亿美元)位居第一、中国占15.7%(2315亿美元)位居第二、EU5(法德意西英)占12.5%(1845亿美元)。美国为例,人均医药支出高达1780美元,约为中国的11倍(2023年我国人均医药支出164美元)。
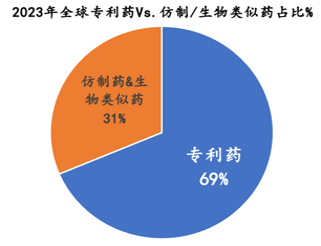
2019~2023年,全球专利药市场以3.3%的年复合增长率从0.89万亿美元扩大至1.01万亿美元,预计到2030年将达1.47万亿美元,复合增速达5.5%。期间,仿制药及生物类似药则以1.4%的年复合增长率从0.44万亿美元扩大至0.46万亿美元,预计到2030年达0.6万亿,复合增速3.8%。
翰宇药业优先布局在美国进行ANDA申报上市的行为看似是在赌,但通过上文的仔细拆分和研究美国本土的政策及市场环境,让人不禁感叹翰宇药业国际化布局所蕴含的智慧。
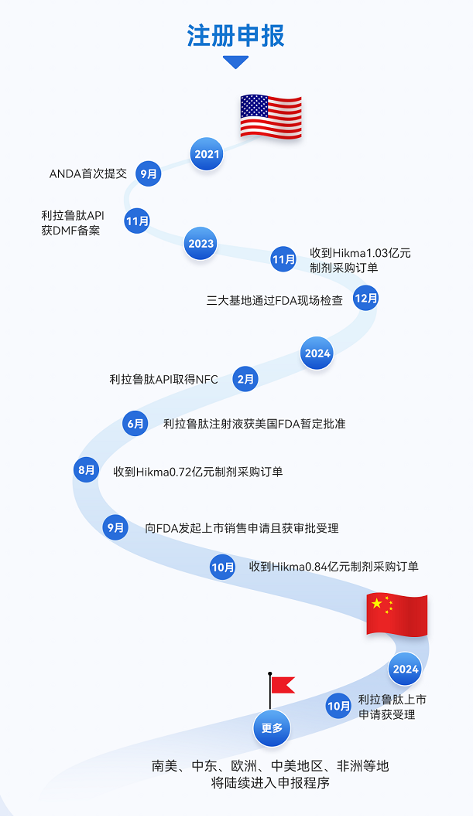
2021年,翰宇药业利拉鲁肽注射液正式提交ANDA申请,已经做好了不出海,毋宁死的决心,之后从原料药DMF,生产基地现场检查,直至2024年6月获得美国FDA暂定批准,可以说是一帆风顺。9月23日,翰宇药业向FDA发起上市销售申请且获审批受理,目标审评日期12月23日。
在向FDA提交上市销售申请并获得审批受理的同时,翰宇药业与跨国制药巨头Hikma已为即将到来的首仿药在美国的上市做好了充分准备。10月30日,利拉鲁肽注射液终于迎来了大规模发货。据悉,这笔订单是公司于2023年11月3日公告的商业批量订单,金额约为1.03亿元人民币。此外,翰宇药业与Hikma维持长期独家合作关系,未来将根据美国销售市场需求,持续推进后续订单发货,并获得两位数的销售利润分成。经过十年的努力,翰宇药业凭借GLP-1制剂的出海契机,迎来了未来业绩长期增长的转折点。满载利拉鲁肽注射液的集装箱运输车正驶出翰宇药业的坪山制剂生产基地,预计将惠及更多美国患者。

利拉鲁肽的天花板并不止于此,欧洲、中东、南美等地区的市场同样不可小觑,一旦美国获批,通过世界卫生组织国际贸易药品认证计划 COPP(Certificate of a Pharmaceutical Product,药品出口销售证明)等国际医药产业政策可实现进一步与全球多个国家接轨。
打铁还需自身硬,没有足够的研发、质量以及生产水平做支撑,全球化布局就是纸上谈兵。作为多肽行业的领军药企,翰宇药业研发投入占比始终保持较高水平,2024年前三季度,研发费用占营业收入比重达18.22%,与利拉鲁肽同属GLP-1管线的减重“神药”司美格鲁肽、替尔泊肽、瑞塔鲁肽等也均有布局。
翰宇药业在质量上的管理则更加精益求精,坪山制剂生产基地、武汉原料药生产基地、龙华总部研发中心均已通过美国FDA现场检查,多次通过欧盟、韩国、巴西等GMP认证检查,对于申报美国FDA的中国药企来说,是难度非常高的一件事。在此基础上,利拉鲁肽的顺利申报是可复制的,并且为未来其他产品的出海提供宝贵的实践经验。
合作出海是更适合的选择
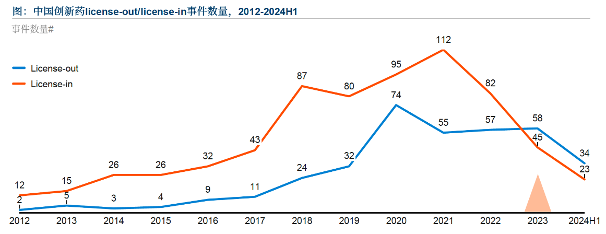
在确定目标市场以及核心产品后,如何使利益最大化,是“独赢”还是“共赢”,就需要企业仔细斟酌更加适合自身的出海模式。据统计,License-out模式成为2023年以来中国医药最主流的出海方式之一,中国本土药企License-out交易数量达到58起,首次超过License-in,开始从“引进”向“输出”转变。由此看来,大多数企业的选择更加偏向于“共赢”。
简单来说,License-out是指中国企业进行创新药研发后,将项目授权、售卖给海外药企,由后者负责海外的后期临床和上市销售;原研发企业获得里程碑付款和销售分成,这里的关键词即为“合作”,与熟悉海外市场环境、销售渠道丰富的企业建立合作关系,更加容易突破环境壁垒,同时也有助于缓解药企的资金压力,支持其后续的研发和运营活动。
翰宇药业可以说将这一模式演绎的炉火纯青,2019年,翰宇药业与国际仿制药巨头Hikma就利拉鲁肽注射液达成合作;2021年,与辉凌医药就中国市场辅助生殖领域达成战略合作,后基于双方合作成绩显著,于2023年将合作范围扩大至全球78个国家和地区;2024年5月,与三生蔓迪就司美格鲁肽注射液(减重适应症)产品达成合作,以中国区域为首开展合作布局;2024年9月,与Mullan就利拉鲁肽独家授权、供应和分销达成共识。
尽管合作方、合作区域、合作产品有所不同,但上述合作都有一个共同点,那就是合作方需向翰宇药业支付合作授权费、里程碑付款、供货价、以及末端利润分成。合作授权费、里程碑付款、供货价已经提前锁定获利空间,而后端利润分成则是更加具有想象空间的部分。
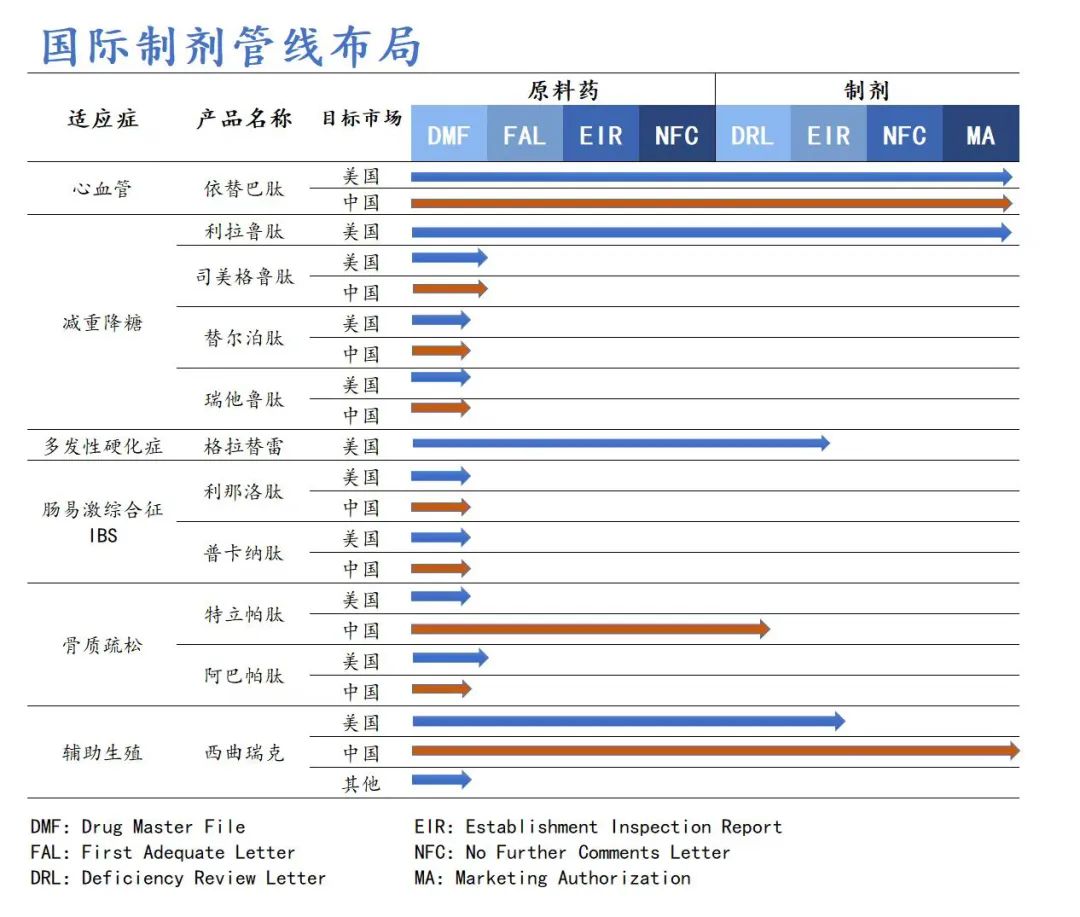
对于翰宇药业而言,利拉鲁肽的出海是公司开启出海“狂飙”模式的钥匙,不管是后续GLP-1管线的司美格鲁肽、替尔泊肽、瑞他鲁肽,还是多发性硬化症的格拉替雷等重磅产品,都将凭借其过硬的品质拥有和国际知名药企对话的机会。但机会并不会自己找上门,每一次的机会都积累于翰宇药业26年来在多肽领域的精耕细作,相信翰宇药业已经做好了抓住机会的准备。
$翰宇药业(SZ300199)$
本文作者可以追加内容哦 !

