中美双报,抗感染经典用药
普利制药注射用盐酸多西环素
获国家药品监督管理局
批准上市!
海南普利制药股份有限公司(以下简称“普利制药”或“公司”)于近日收到国家药品监督管理局签发的注射用盐酸多西环素(规格:0.1、0.2g)的药品注册批件,视为通过一致性评价批准上市,将为拓展国内市场带来积极影响。
普利制药此次注射用盐酸多西环素在中国获批上市的有两种规格:0.1、0.2g。公司注射用盐酸多西环素为中美双报品种,质量安全有保证,将为国内患者提供高品质的用药选择。
诚邀合作,欢迎垂询,国内招商:
GNXS@hnpoly.com
0571-89385059
药物简介
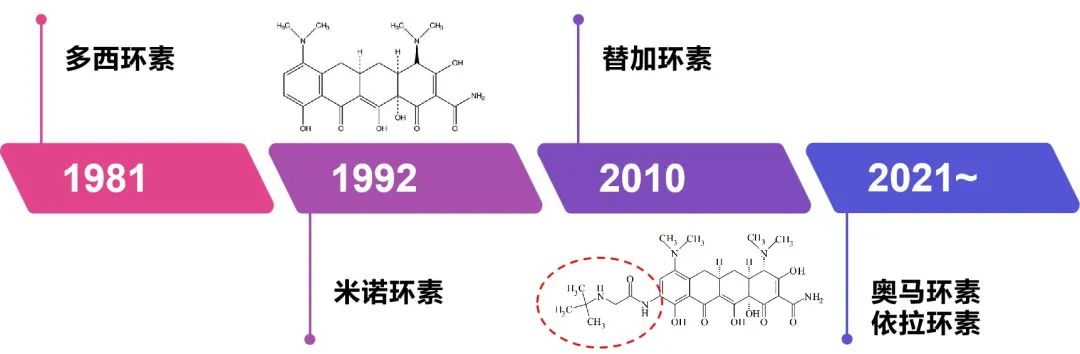
多西环素是一种经典的四环素类抗生素,具有广泛的抗菌作用,能有效抑制非典型致病菌、革兰阳性和阴性菌的生长。
临床上主要用于治疗立克次体病、支原体属感染、衣原体属感染等多种疾病,包括支原体肺炎(呼吸科/儿科)、盆腔炎症性疾病(妇科)、非淋菌尿道炎(泌尿科)等。
销售增量可观,市场竞争小
根据米内网的数据,近几年,多西环素注射剂市场销售增量可观,2022年~2024年H1(H1:上半年)的销售额分别为5800万元、12800万元、9200万元,平均年增长率高达73%。
在销售数量方面,2022年~2024年H1(H1:上半年)分别为144万支、369万支、279万支,平均年增长率高达97%。
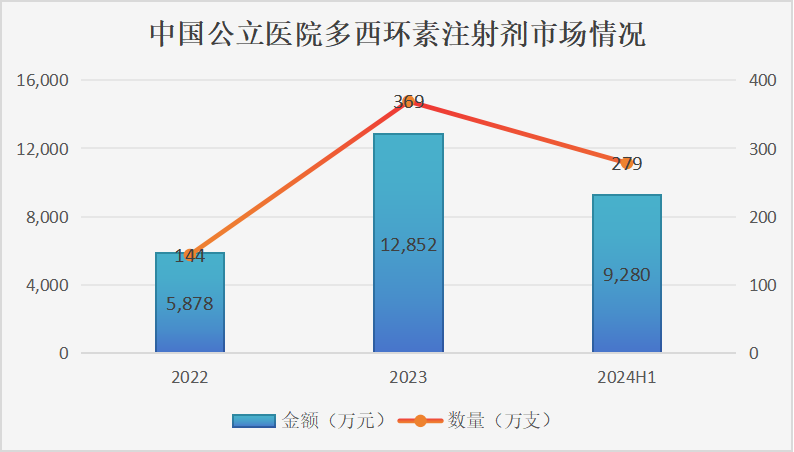
2024H1:2024年上半年
此外,普利制药的注射用盐酸多西环素为同品种第三家通过一致性评价(目前仅3家过评),该品种后续尚无其他厂家进行一致性评价申报。
根据第十批国家集采情况,通常过评厂家达到7家才有可能纳入到集采,目前注射用盐酸多西环素远未达到集采条件且无其他企业申报,该品种竞争压力较小,未来有望为公司业绩增长带来强劲动力。

中美双报,高品质保证
普利制药的注射用盐酸多西环素为中美双报品种,国内与美国市场共用一条生产线,同质量标准,同产品品质,将为国内患者提供高品质的用药选择。
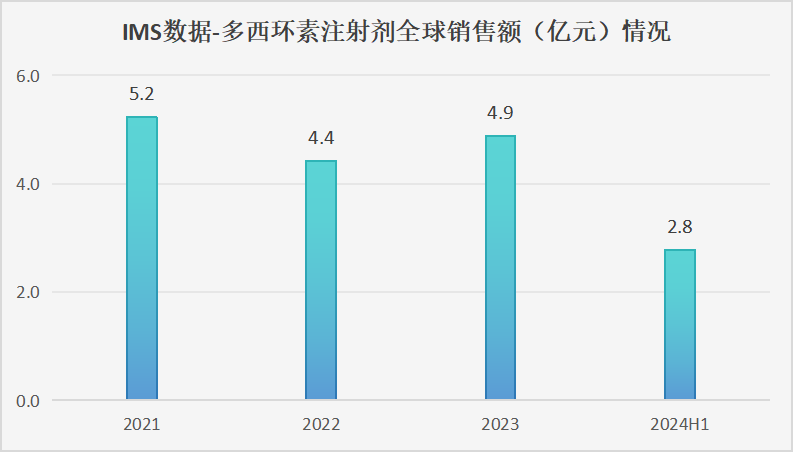
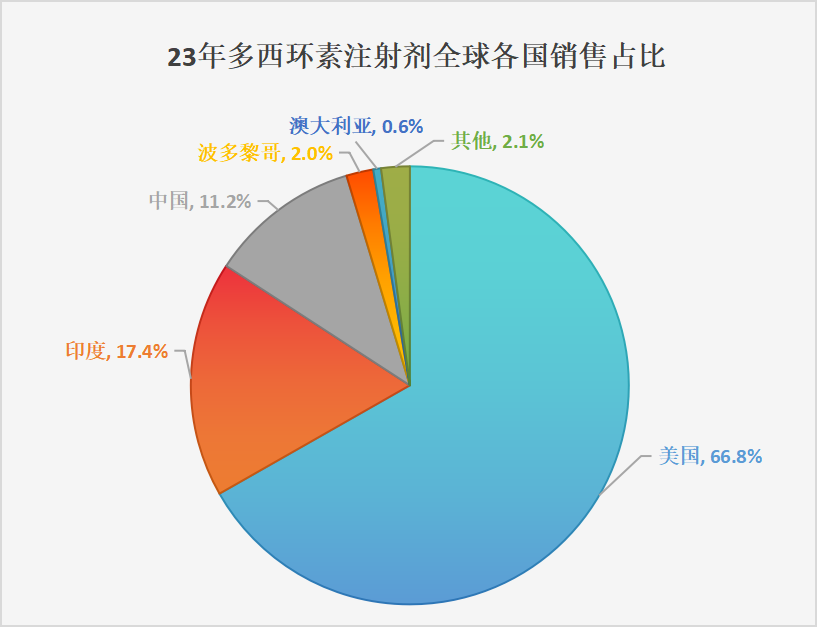
根据IMS数据显示,多西环素注射剂近几年全球销售额数据在5亿元左右,整体市场稳定。其中,美国市场占据了全球66.8%的市场份额(普利已经获批且实现药品出口),中国市场是全球第三大市场(11.2%)。
诚邀合作,欢迎垂询,国内招商:
GNXS@hnpoly.com
0571-89385059
关于普利制药

普利制药 1992 年成立于海口,是中国医药制剂国际化先导企业和国家工信部智能制造示范企业,已被国家工信部纳入工业转型升级中国制造 2025 年儿童药重点项目企业,2023年海南普利通过海关“AEO”高级认证。
此前,海南普利及其子公司浙江普利、安徽普利也曾多次顺利通过美国FDA、欧盟EMA现场审计。作为中国医药制剂国际化先导企业,普利制药多年来一直恪守全球较高质量标准,是国内为数不多的原料药和注射剂研发和生产平台,也是为数不多的同时获得美国、中国、欧盟等药监部门批准的原料药、关键辅料、药物药剂和GMP中间体CMO/CDMO的优质供应商。


