精准认“痘”!圣湘新发传染病Disease X解决方案第一证

近日,圣湘生物自主研发的猴痘病毒核酸检测试剂盒(PCR-荧光探针法)通过国家药品监督管理局审核,获批上市。这是圣湘生物今年获得的第十个三类医疗器械注册证,也是圣湘新发传染病Disease X解决方案斩获的第一个证。

该试剂采用实时荧光PCR技术,可定性检测人皮肤病变拭子中的猴痘病毒特异性保守区域基因,灵敏度为200copies/mL,精准性高,可及性强,可兼容多种荧光PCR平台,搭配自动化核酸提取设备,最快60min出结果,同时采用UNG酶+dUTP防污染体系,内标监控检测全程,保障检测结果的准确性。
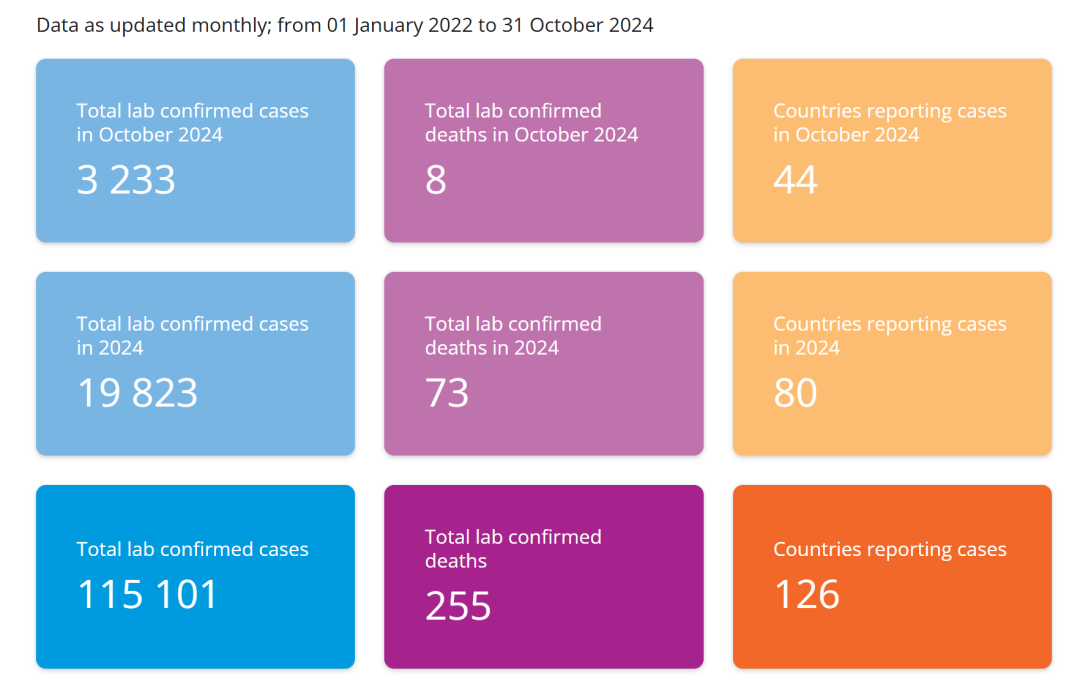
2022-2024年猴痘疫情全球趋势
2024年8月14日,世界卫生组织(WHO)宣布猴痘疫情为国际关注的突发公共卫生事件,截至10月31日,全球126个国家/地区累计报告猴痘确诊病例115,101例;同年11月22日,WHO决定维持对猴痘疫情的最高级别警戒,理由是病例和受影响国家的数量在继续上升。
作为一种典型的病毒性人畜共患病(从动物传播给人的病毒),猴痘病毒(Monkeypox virus, MPV)主要发生在非洲中部和西部地区热带雨林,感染后的主要症状包括发热、淋巴结肿大和全身水疱脓疱,与一些出疹性疾病(如水痘、天花、单纯疱疹等)存在相似之处,仅靠临床症状对病原进行区分并不可靠。
目前实验室检测猴痘病毒的主要方法包括:病毒分离和鉴定、血清学检测、PCR检测、抗原抗体检测等。WHO在8月29日发布的猴痘EUL邀请中指出产品定位在分子产品,血液和抗体检测不推荐用于常规诊断;WHO发布的《全球猴痘战略准备与应对计划》明确指出,PCR检测是针对猴痘病毒诊断的金标准,可以快速、准确地区分猴痘病毒与其他相似病毒,对于疾病的早期诊断和疫情防控非常重要。
近年来,圣湘生物针对猴痘病毒开发了一系列检测产品,可满足各类检测场景需求。其中,猴痘病毒核酸检测试剂在今年8月份成为非洲疾病预防控制中心(Africa CDC)首批推荐检测试剂;2022年到2024年期间,作为FIND基金会推荐使用参考试剂,用于评估其他猴痘检测试剂的准确性。目前,该试剂已经取得欧盟、英国、北爱尔兰、哥伦比亚、印度尼西亚、沙特、摩洛哥等多个地区和国家的注册准入证书,并出口至法国、菲律宾、马来西亚、土耳其、印度尼西亚等20多个国家,助力全球猴痘疫情防控。
圣湘生物此次上市的猴痘病毒核酸检测试剂是圣湘已搭建的新发传染病“Disease X”解决方案的第一证。该方案集仪器、试剂、数智化系统为一体,通过强大的研发生产体系实现7天发现“X”病原,7天研发“X”试剂,7天量产“X试剂”,7天全域覆盖,在28天完成对人源样本和环境污水等样本的“检测—监测—预测”全流程管理,有效提高对Disease X的防控能力,在疾病出现早期及时发现、准确监测,并对其发展趋势进行科学预测,从而为制定合理的防控策略和保障全球公共卫生安全提供有力支持。
本文作者可以追加内容哦 !

