国家药监局12月 31 日公布的药品通知件送达信息中,赫然出现九源基因的司美格鲁肽注射液,这一关键信息实则宣告:该产品现阶段的上市申请未获批准。
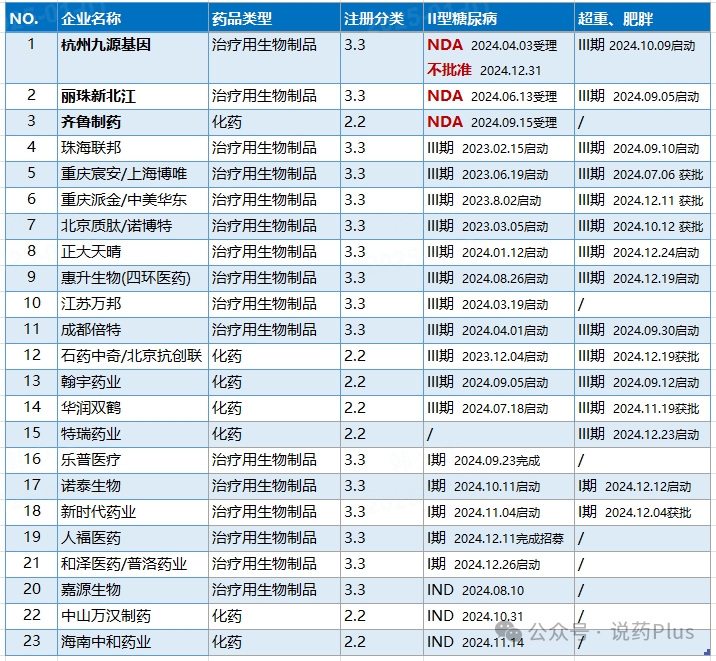
2024年4月3日,国家药监局药品审评中心(CDE)官网公示,杭州九源基因的司美格鲁肽注射液生物类似药上市申请已经获得受理,申报类别为生物制品3.3类,成为国内第一家申报上市的司美格鲁肽生物类似药,申报的适应症为用于成人2型糖尿病患者的血糖控制,一时成为行业瞩目的焦点,奈何如今却面临这般局面,后续走向愈发引人关注。从下表的统计结果来看,国内已披露共23款司美格鲁肽生物类似物在研,其中,九源基因、丽珠、齐鲁3家均已提交上市申请(NDA),另有12家处于III期临床阶段;12家同时申报了降糖和“超重/肥胖”适应症。
自从 GLP- 1 降低血糖的作用被发现以来,GLP-1成为很多药企研究的热门靶点。当前全球GLP-1RA市场已突破200亿美元,预计2031年全球有望达1650亿美元规模。而我国 GLP-1 药物还处于市场培育期,2022年高速增长至约60.5亿元,据 Frost&Sullivan预测,2030年我国GLP-1RA市场规模将达515亿元,呈快速发展态势。
GLP - 1 领域激战正酣,拥挤程度超乎想象,朝着 PD1/PDL1 的火爆态势奔去。同时,众多创新药扎堆研发,司美格鲁肽类似药的NDA波折是个警示。在诸多同质化竞品围剿下,在司美格鲁肽和替尔泊肽强势霸榜的局面下如果没有过硬的头对头临床数据支撑,绝大部分“入局”的药企想脱颖而出、在这“红海”中实现盈利可能太难。
$翰宇药业(SZ300199)$ $常山药业(SZ300255)$ $九源基因(HK|02566)$ #复盘记录# #强势机会# #周度策略# #收盘点评# #投资干货#
本文作者可以追加内容哦 !

