原料药的重大利好要来了?静待官方解释......
原创 邴贵方 邴药说 2025年01月04日 08:48 天津 13人
2025年01月03日,下午17:11国务院办公厅发布了《国务院办公厅关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》引爆了医药同行的朋友圈。小编看了看,涉及到原料药的,仅有这么一句话:优化原料药管理,原料药登记主体可依法变更。(国家药监局牵头,试点地区省级人民政府配合)。

但本着字少事大的原则,是不是原料药的重大利好要来了?大家和小编一起来分析一下。
这句话出现在“优化药品补充申请审评审批。”的条款下。那么应该属于已有批准文号的原料药实行重大变更,难道字面意思就是“已经转“A”的原料药登记主体可以依法变更了?再深层次理解,已经转“A”的原料药的《化学原料药上市申请批准通知书》批文可以交易了?如果是这样,那对于原料药企业绝对是重大的利好!
关于化学原料药能否变更登记人主体? ,小编只看到了CDE共性问题在2023年10月26日的一条问答和2024年06月28日国家药监局对十四届全国人大二次会议第4563号建议的答复。
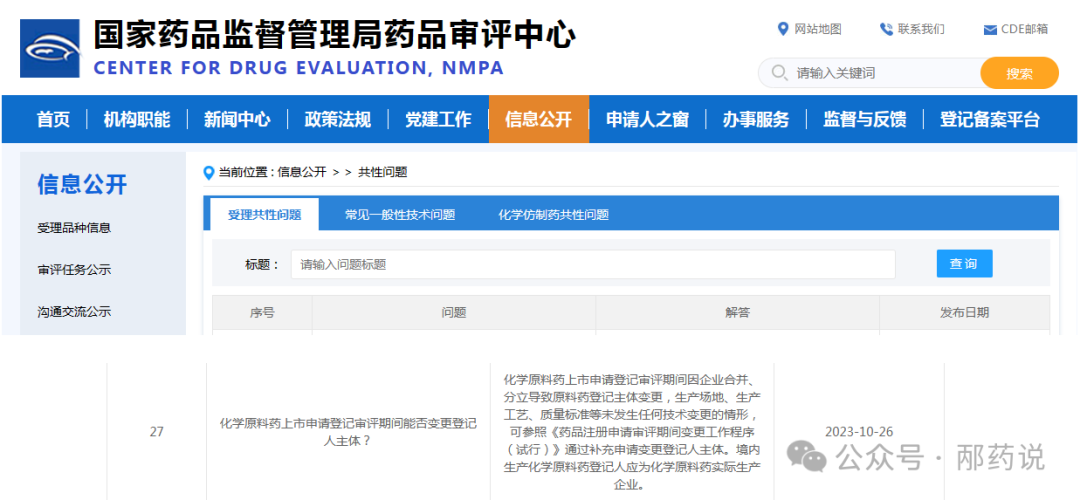
问:化学原料药上市申请登记审评期间能否变更登记人主体?
化学原料药上市申请登记审评期间因企业合并、分立导致原料药登记主体变更,生产场地、生产工艺、质量标准等未发生任何技术变更的情形,可参照《药品注册申请审评期间变更工作程序(试行)》通过补充申请变更登记人主体。境内生产化学原料药登记人应为化学原料药实际生产企业。
但这里也明确了变更的类型“企业合并、分立”,指的就是原本是同一企业,或者有极强关联性的企业。而且问答还明确:境内生产化学原料药登记人应为化学原料药实际生产企业。
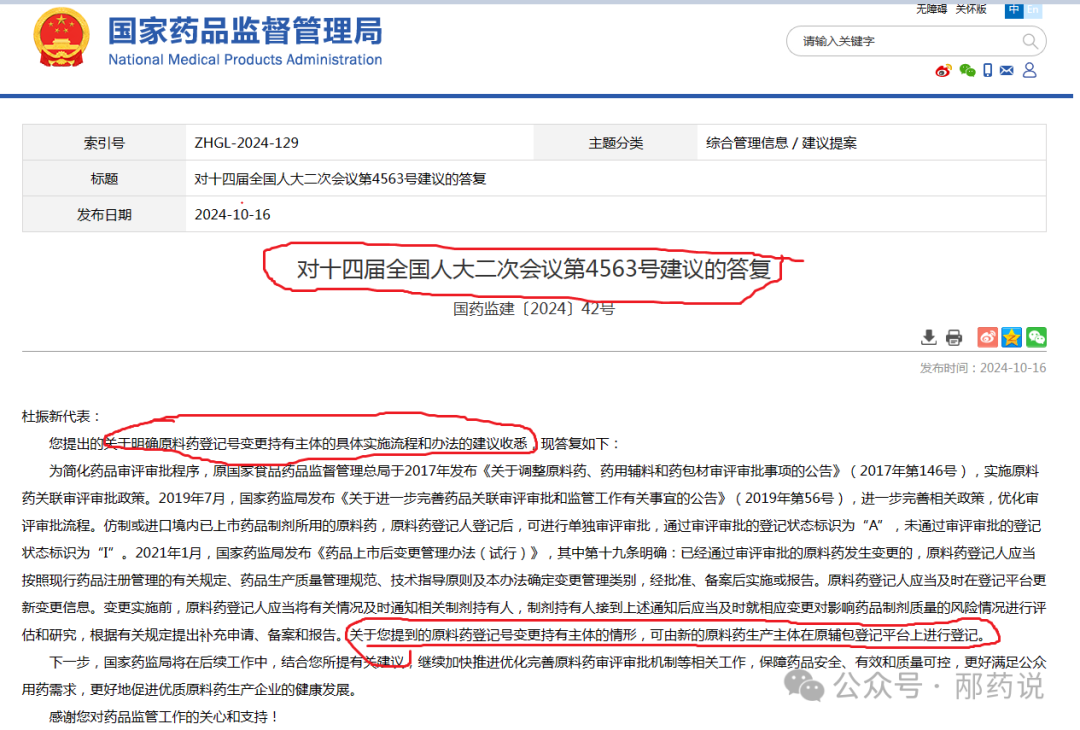
国家药监局对十四届全国人大二次会议第4563号辰欣药业的杜振新董事长的答复也是比较含糊。杜振新提出的关于明确原料药登记号变更持有主体的具体实施流程和办法。药监局回答:关于您提到的原料药登记号变更持有主体的情形,可由新的原料药生产主体在原辅包登记平台上进行登记。
自2017年11月国家药监局不再单独受理原料药的注册申请,CDE建立了原辅包登记平台与数据库,企业可以通过登记平台提交原料药登记资料并获得原料药登记号,待关联药品制剂提出注册申请后一并审评。而后续修订实施的《药品管理办法》《药品注册管理办法》《药品生产监督管理办法》也明确规定,持有人制度不适用于原料药,原料药只发批准通知书,没有药品注册证。《药品生产监督管理办法》第四十二条规定,经批准或者通过关联审评审批的原料药应当自行生产,不得再行委托他人生产。这一规定构成了当前原料药委托生产的法律禁令。按照现行法律框架,若某医药企业出于商业考量欲持有特定原料药,则必须满足原料药的生产资质要求,即原料药的登记主体与实际生产主体必须保持高度一致。然而,对于主营业务并非原料药生产,而是专注于制剂生产或代理业务的医药企业而言,为单一原料药单独建设生产设施并全面满足其生产条件显然不切实际。在此情境下,唯有通过委托生产方能满足其商业需求,但这对制剂生产企业及药品上市许可持有人(MAH)而言,无疑构成了极大的限制与挑战。
但这样的需求是实实在在存在的,于是现实世界中的实施和变通的方法就是:如果有持有人想投资开发原料药,需要委托具备条件的企业作为申报主体申请原料药登记号,受托企业为名义持有人并负责生产,受托企业仅获加工费。产生的一切费用由委托人负责。产生的最大的法律困境是:自己的原料药,需要登记在他人名下,实质上也是构成了原料药登记号的代持。这也导致原料药持有人的“药品管理法律项下的法定权利”变更为“民事法律关系项下的合同权利”。
但这种代持的变通方法违反药品监管的法律规定吗?与受托生产企业发生合同纠纷怎么办?最最重要的这样导致原料药无法像药品批准文号一样进行转让交易了。
那么《国务院办公厅关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》提到的原料药登记主体可依法变更,是不是就是原料药的批文可以交易了?
所以静待官方的解释……
另外呼吁,随着环境监管日益的趋严,原料药生产场地的变更,同省市迁址和跨省市的变更场地都亟需出台相关规定!
静待吧!!!!!!
本文作者可以追加内容哦 !

