为了证明 AlphaFold3基于合理结构的药物设计的潜力,该团队研究了免疫检查点蛋白TIM-3,在 2021年发表后被确定为癌症免疫治疗的潜在点。
在Isomorphic Labs团队发文之前,蛋白质数据库中不存在 TIM-3的小分子结合晶体结构,并且这些结构不在 AlphaFold3的训练集中。
团队使用 AlphaFold3评估了这个蛋白,在没有向AlphaFold 3提供任何关于姿势、结构或口袋的额外信息的情况下,预测的结构与己发表的实验结构一致。
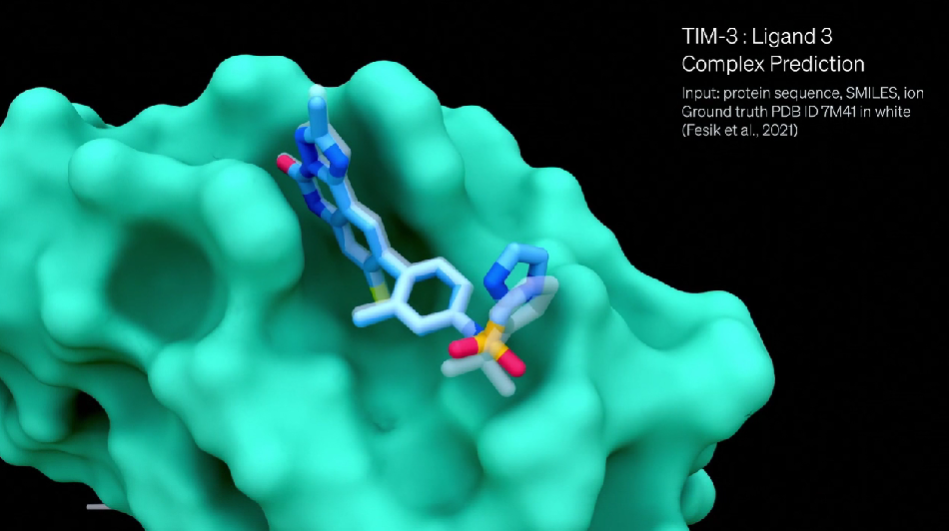
通过这个例子,AlphaFold 3证明了它可以准确地描述药物分子结构设计的进展。
目前该公司已分别与礼来和诺华开展了药物研发合作,分别获得了4500万美元与3750万美元的预付款,这两笔交易涉及到多靶点的小分子药物。
仅从这两次合作中,Isomorphic Labs就有资格获得高达30亿美元的基于业绩的里程碑付款。
据这位高管称,两家企业合作推出的第一批药物可能会“在未来两年内”到达。

没开源,且使用有限制
Hass 表示,对于 AlphaFold 3,目前没有计划发布完整代码。
这也是受到很多科学家们诟病的地方,毕竟AlphaFold2是完全开源,这一举动极大地促进了计算蛋白质的进步。
“没有代码的计算论文不应该被接受,”加州大学旧金山分校弗雷泽实验室的结构和计算生物学家Stephanie Wankowicz在社交媒体上发帖说。“此外,访问受到限制阻碍了开放科学的进步。”
好在DeepMind为该模型发布了一个名为AlphaFold Server 的公共接口,该接口对可以进行实验的分子施加了限制,并且只能用于非商业目的。
不过,使用这个模块也是有限制的,科学家对AlphaFold3每天只能进行10次预测,而且无法获得可能与药物结合的蛋白质结构。
对于药物研发而言,预测分子如何相互作用是一件非常重要的事情,因为大多数药物的作用原理是与目标蛋白质结合。
也就是说,DeepMind出于商业考量放弃了科学开源精神,转而让其创办的 Isomorphic Labs 和礼来、诺华等顶级制药公司达成了价值30亿美元的合作。
如今,全球科学家已经紧锣密鼓地使用AlphaFold3进行各种基准测试。
例如有科学家用AlphaFold3识别MutH 或 MutL 的相互作用位点,得到的结果和试验完全一致,而他博士论文中的绝大部分精力耗费在这上面,这位科学家称,AlphaFold3太疯狂了!
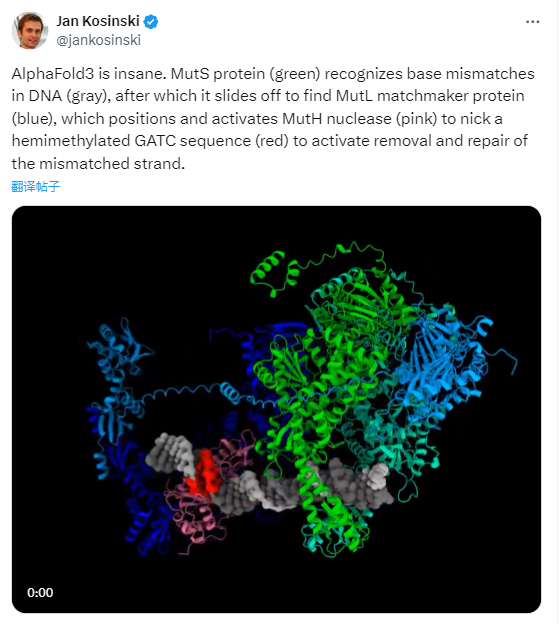
但无论开源与否,AlphaFold 3 的开发都代表着AI计算模型对生物分子结构和相互作用理解的一个重要里程碑。
通过提供复杂生物系统的精确 3D 模型,它为药物发现、蛋白质工程和生命科学的基础研究开辟了新的可能性。
本文作者可以追加内容哦 !

