4月3日,诺华宣布其高选择性内皮素A受体(ETA)拮抗剂阿曲生坦(atrasentan,Vanrafia)的上市申请已获FDA加速批准,用于降低有疾病进展风险的原发性免疫球蛋白A肾病(IgAN)成人患者的蛋白尿。这意味着,阿曲生坦成为了首个获批用于减少原发性IgA肾病蛋白尿的选择性ETA拮抗剂。  2023年,诺华以35亿美元收购了Chinook公司,获得了atrasentan和APRIL单抗zigakibart两款IgA肾病药物。同年,atrasentan治疗IgA肾病的III期ALIGN研究在36周期中分析取得积极结果,达到了主要疗效终点,能够显著降低患者蛋白尿。
2023年,诺华以35亿美元收购了Chinook公司,获得了atrasentan和APRIL单抗zigakibart两款IgA肾病药物。同年,atrasentan治疗IgA肾病的III期ALIGN研究在36周期中分析取得积极结果,达到了主要疗效终点,能够显著降低患者蛋白尿。 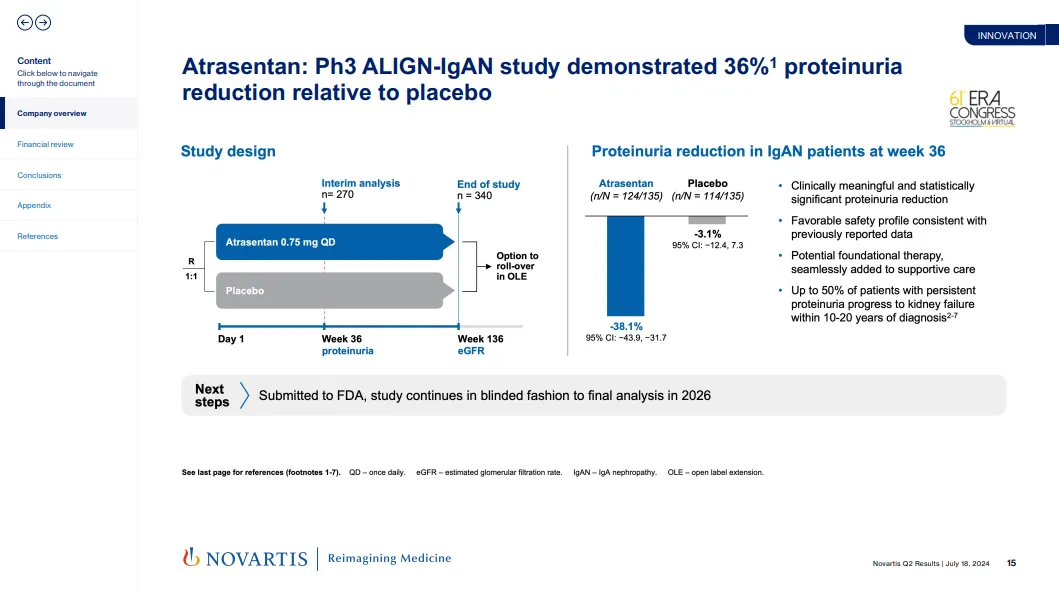 Atrasentan获得加速批准的依据正是基于ALIGN研究的预设中期分析。诺华在新闻稿中表示,atrasentan是否能延缓IgAN 患者肾功能的衰退尚未确定,其能否继续获批可能取决于ALIGN研究的临床获益验证,通过第136周时估计肾小球滤过率(eGFR)的下降来评估atrasentan是否能减缓疾病的进展。eGFR数据预计将于2026年公布。 IgA肾病是一种以免疫球蛋白A为主的免疫复合物在肾小球系膜区沉积为特征的肾小球疾病,也是全球范围内最为常见的原发性肾小球肾炎,常见于年轻人,是全球慢性肾病和肾衰竭的主要原因。 值得一提的是,atrasentan也已在中国申报上市并获优先审评。据估计,全世界每年每百万人中约有25人被新诊断为IgA肾病,而中国是全球IgA肾病发病率最高的国家之一。 伴随着atrasentan的获批,诺华在肾病领域的布局也逐渐丰富。2024年8月,靶向补体旁路途径的first-in-class补体因子B(CFB)抑制剂伊普可泮获FDA批准用于治疗IgA肾病,并已于2025年3月再获FDA批准用于治疗C3肾小球病(C3G),这也是第一个获批上市的C3G疗法。
Atrasentan获得加速批准的依据正是基于ALIGN研究的预设中期分析。诺华在新闻稿中表示,atrasentan是否能延缓IgAN 患者肾功能的衰退尚未确定,其能否继续获批可能取决于ALIGN研究的临床获益验证,通过第136周时估计肾小球滤过率(eGFR)的下降来评估atrasentan是否能减缓疾病的进展。eGFR数据预计将于2026年公布。 IgA肾病是一种以免疫球蛋白A为主的免疫复合物在肾小球系膜区沉积为特征的肾小球疾病,也是全球范围内最为常见的原发性肾小球肾炎,常见于年轻人,是全球慢性肾病和肾衰竭的主要原因。 值得一提的是,atrasentan也已在中国申报上市并获优先审评。据估计,全世界每年每百万人中约有25人被新诊断为IgA肾病,而中国是全球IgA肾病发病率最高的国家之一。 伴随着atrasentan的获批,诺华在肾病领域的布局也逐渐丰富。2024年8月,靶向补体旁路途径的first-in-class补体因子B(CFB)抑制剂伊普可泮获FDA批准用于治疗IgA肾病,并已于2025年3月再获FDA批准用于治疗C3肾小球病(C3G),这也是第一个获批上市的C3G疗法。
 2023年,诺华以35亿美元收购了Chinook公司,获得了atrasentan和APRIL单抗zigakibart两款IgA肾病药物。同年,atrasentan治疗IgA肾病的III期ALIGN研究在36周期中分析取得积极结果,达到了主要疗效终点,能够显著降低患者蛋白尿。
2023年,诺华以35亿美元收购了Chinook公司,获得了atrasentan和APRIL单抗zigakibart两款IgA肾病药物。同年,atrasentan治疗IgA肾病的III期ALIGN研究在36周期中分析取得积极结果,达到了主要疗效终点,能够显著降低患者蛋白尿。  Atrasentan获得加速批准的依据正是基于ALIGN研究的预设中期分析。诺华在新闻稿中表示,atrasentan是否能延缓IgAN 患者肾功能的衰退尚未确定,其能否继续获批可能取决于ALIGN研究的临床获益验证,通过第136周时估计肾小球滤过率(eGFR)的下降来评估atrasentan是否能减缓疾病的进展。eGFR数据预计将于2026年公布。 IgA肾病是一种以免疫球蛋白A为主的免疫复合物在肾小球系膜区沉积为特征的肾小球疾病,也是全球范围内最为常见的原发性肾小球肾炎,常见于年轻人,是全球慢性肾病和肾衰竭的主要原因。 值得一提的是,atrasentan也已在中国申报上市并获优先审评。据估计,全世界每年每百万人中约有25人被新诊断为IgA肾病,而中国是全球IgA肾病发病率最高的国家之一。 伴随着atrasentan的获批,诺华在肾病领域的布局也逐渐丰富。2024年8月,靶向补体旁路途径的first-in-class补体因子B(CFB)抑制剂伊普可泮获FDA批准用于治疗IgA肾病,并已于2025年3月再获FDA批准用于治疗C3肾小球病(C3G),这也是第一个获批上市的C3G疗法。
Atrasentan获得加速批准的依据正是基于ALIGN研究的预设中期分析。诺华在新闻稿中表示,atrasentan是否能延缓IgAN 患者肾功能的衰退尚未确定,其能否继续获批可能取决于ALIGN研究的临床获益验证,通过第136周时估计肾小球滤过率(eGFR)的下降来评估atrasentan是否能减缓疾病的进展。eGFR数据预计将于2026年公布。 IgA肾病是一种以免疫球蛋白A为主的免疫复合物在肾小球系膜区沉积为特征的肾小球疾病,也是全球范围内最为常见的原发性肾小球肾炎,常见于年轻人,是全球慢性肾病和肾衰竭的主要原因。 值得一提的是,atrasentan也已在中国申报上市并获优先审评。据估计,全世界每年每百万人中约有25人被新诊断为IgA肾病,而中国是全球IgA肾病发病率最高的国家之一。 伴随着atrasentan的获批,诺华在肾病领域的布局也逐渐丰富。2024年8月,靶向补体旁路途径的first-in-class补体因子B(CFB)抑制剂伊普可泮获FDA批准用于治疗IgA肾病,并已于2025年3月再获FDA批准用于治疗C3肾小球病(C3G),这也是第一个获批上市的C3G疗法。
Copyright 2025 PHARMCUBE. All Rights Reserved.
欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。
免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。
追加内容
本文作者可以追加内容哦 !

