西达本胺治疗晚期黑色素瘤三期临床试验在17个国家已完成入组!
2025-02-10 16:00:02 来源: 同花顺iNews
同花顺(300033)金融研究中心02月10日讯,有投资者向微芯生物提问, 西达本胺结直肠癌三期临床进展如何?沪亚公司黑色素瘤的进展预计何时可以揭盲呢?
公司回答表示,尊敬的投资者,您好!西达本胺结直肠癌III期临床试验正按计划积极进行受试者招募。公司国际合作伙伴HUYABIO(沪亚生物国际)在全球17个国家开展的西达本胺联合纳武利尤单抗一线治疗晚期黑色素瘤的三期临床试验已完成入组。公司将根据信息披露规则对上述研发项目后续进展情况及时履行信息披露义务,感谢您的关注!
微芯生物于2006年将西达本胺全适应症全球开发权授权于沪亚生物国际全球化布局。
授权于沪亚生物国际全球化布局的收益分配:授权一次性里程碑收益2800万元;临床收益分配额20%。
西奥罗尼单药治疗复发难治小细胞肺癌/晚期实体瘤(美国,公司100%股权)II期十二个临床试验中心推进中,目前已完成65mg剂量组爬坡,尚未出现剂量限制性毒性(DLT),美国FDA 于2025 年 3 月同意更高剂量探索美国人群后续用药剂量;
CS23546(PD-L1 小分子抑制剂)的适应症为治疗晚期肿瘤,还包括其他由PDL1信号介导的免疫相关疾病,计划申报美国临床试验;
CS231295片治疗多种实体肿瘤,尤其是脑部肿瘤方面,预计会显示出独特的优势和潜力,计划申报美国临床试验。
以上产品由微芯生物科技(美国)有限公司(公司100%股权)在美国临床试验并运营。
2024 年我国成年糖尿病患者数量约为 1.48 亿人,占全球患者总数的 25.13%,随着患病率的逐年上升,预计到 2050 年该数字将增加至 1.68 亿人。
糖尿病治疗已进入共病管理时代,脂肪肝是糖尿病的重要合并症。中国尚无脂肪肝治疗药物获批,存在巨大临床治疗需求。西格列他钠已获批2 型糖尿病适应症,积累了丰富真实用药经验,且超过一半的糖尿病患者同时患有代谢相关脂肪性肝病,临床就诊的 MASH 患者大部分已合并糖尿病。西格列他钠可通过降糖与胰岛素增敏、血脂调节、抗炎、抗纤维化等多种机制改善代谢性疾病,多项临床试验显示了西格列他钠治疗 2 型糖尿病及脂肪肝的疗效与安全性。西格列他钠已收录于《内科学》教科书、《中国糖尿病防治指南》,有望成为代谢性疾病综合治疗的基础药物,在庞大的患者群体中具备广阔的应用前景。
糖尿病治疗已进入共病管理时代,代谢性疾病具有广泛的共同病因土壤。胰岛素抵抗是 2 型糖尿病核心发病机制,也是血脂异常、脂肪肝等代谢病共同土壤。超 60%的 2 型糖尿病患者伴有血脂紊乱。因此当前糖尿病临床诊疗急需一款既针对胰岛素抵抗,又综合调控血糖、血脂的药物,以解决糖尿病共病管理的综合需求。西格列他钠的上市,正好弥补了这一临床空白。
西格列他钠单药治疗代谢相关脂肪性肝炎(MASH)的II 期临床试验结果在2024 年美国肝脏研究学会(AASLD)年会上进行口头报告。结果显示西格列他钠有效降低肝脏脂肪分数、减轻肝脏炎症和损伤,并有改善纤维化的趋势,且呈剂量依赖性效应,安全性和耐受良好。
根据世界卫生组织(WHO)发布的《2024年全球肝炎报告》,2022年全球约有2.54亿人感染乙肝。其中,中国约有1600万人患有乙肝病毒,乙肝病毒患者是我国乙肝病毒流行病学调查的最新数据。
2025年2月27日晚间,微芯生物(688321)公告称,其全资子公司成都微芯药业有限公司收到国家药监局签发的《药物临床试验批准通知书》,同意公司产品CS12088片开展治疗成人慢性乙型肝炎的临床试验。
目前的核苷类抗病毒药物可有效控制HBV复制并延缓肝硬化的进展,但很少可以治愈慢性乙肝(很少可以实现HBsAg清除),此外还存在需要患者长期用药以及停药后病毒反弹的缺点。患者依然迫切需要针对HBV生命周期不同阶段的新型抗病毒药物。CS12088以其全新的作用机制,在现有治疗方案的基础上,有望为乙型肝炎的功能性治愈提供新的治疗选择,为慢性乙肝患者带来新的希望。
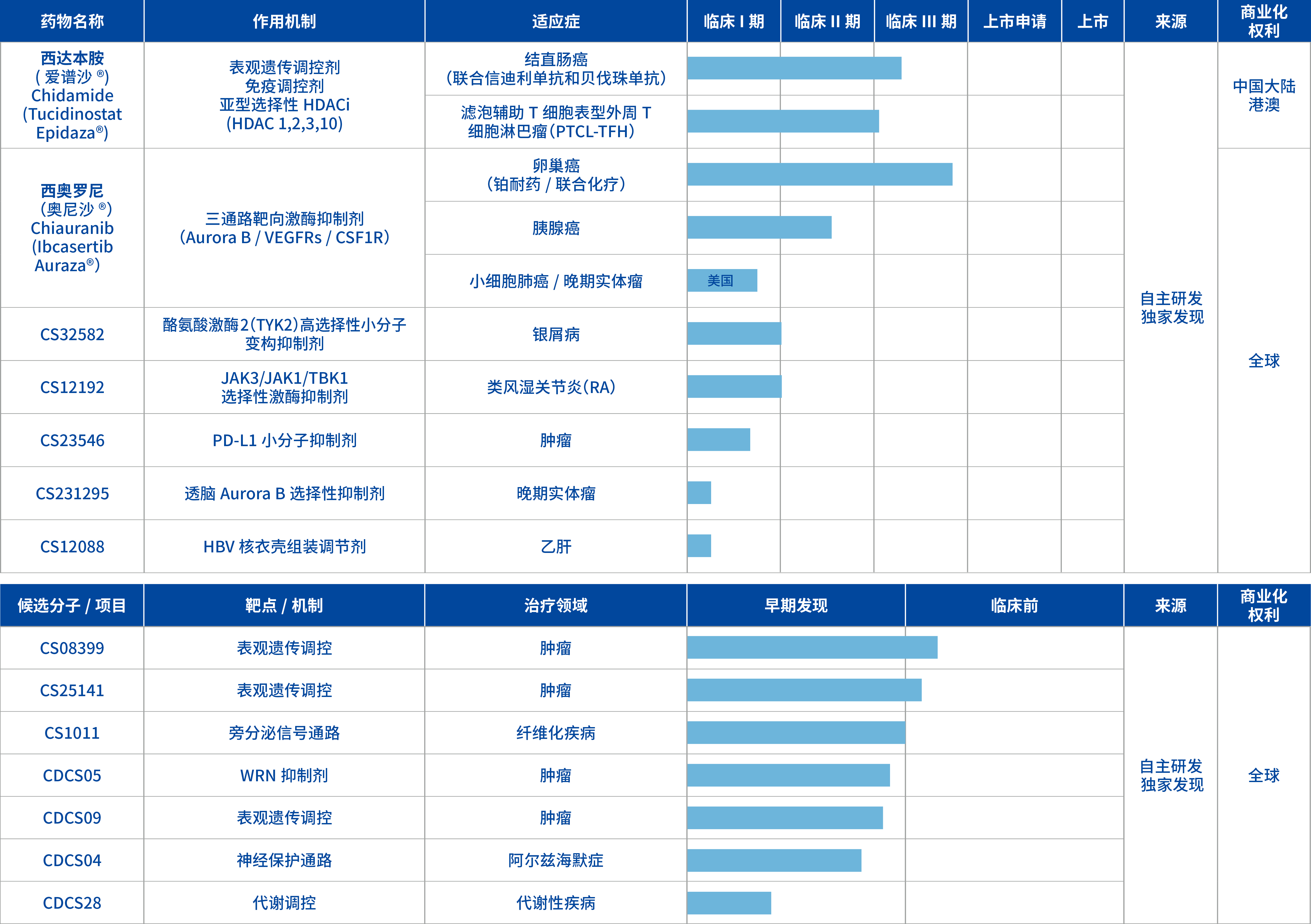
产品线
2024 年,全球范围内与糖尿病相关的健康医疗支出超过 1 万亿美元。糖尿病治疗已进入共病管理时代,脂肪肝是糖尿病的重要合并症。当前糖尿病临床诊疗急需一款既针对胰岛素抵抗,又综合调控血糖、血脂的药物,以解决糖尿病共病管理的综合需求。西格列他钠的上市,正好弥补了这一临床空白。
西格列他钠可通过降糖与胰岛素增敏、血脂调节、抗炎、抗纤维化等多种机制改善代谢性疾病,多项临床试验显示了西格列他钠治疗 2 型糖尿病及脂肪肝的疗效与安全性。西格列他钠已收录于《内科学》教科书、《中国糖尿病防治指南》,有望成为代谢性疾病综合治疗的基础药物,在庞大的患者群体中具备广阔的应用前景。
依据中金企信国际咨询,2030年全球抗肿瘤药物市场规模4,825亿美元。其中2030年美国抗肿瘤药物市场的达2,219 亿美元;中国抗肿瘤药物市场将达到6,831亿元人民币(1美元≈7.1785人民币换算美元951.59亿美元)。中美合计3170.59亿美元,按20%市场份额、70%净利润率,30倍估值,到2030年总股本假设8亿股预计,到2030年微芯生物股价=3170.59亿美元x20%x70%x30/8亿股=1665美元/股。
微芯生物:原创新药的研发、生产与销售:
西奥罗尼单药治疗复发难治小细胞肺癌/晚期实体瘤(美国,公司100%股权)II期十二个临床试验中心推进中;CS23546(PD-L1 小分子抑制剂)的适应症为治疗晚期肿瘤,还包括其他由PDL1信号介导的免疫相关疾病,计划申报美国临床试验;CS231295片治疗多种实体肿瘤,尤其是脑部肿瘤方面,预计会显示出独特的优势和潜力,计划申报美国临床试验。公司国际合作伙伴HUYABIO(沪亚生物国际)在全球17个国家开展的西达本胺联合纳武利尤单抗一线治疗晚期黑色素瘤的三期临床试验已完成入组。
依据中金企信国际咨询,2030年全球抗肿瘤药物市场规模4,825亿美元。其中2030年美国抗肿瘤药物市场的达2,219 亿美元;中国抗肿瘤药物市场将达到6,831亿元人民币(1美元≈7.1785人民币换算美元951.59亿美元)。中美合计3170.59亿美元,按20%市场份额、70%净利润率,30倍估值,到2030年总股本假设8亿股预计,到2030年微芯生物股价=3170.59亿美元x20%x70%x30/8亿股=1665美元/股。
并2024 年全球范围内与糖尿病相关的健康医疗支出超过 1 万亿美元。糖尿病治疗已进入共病管理时代,脂肪肝是糖尿病的重要合并症。当前糖尿病临床诊疗急需一款既针对胰岛素抵抗,又综合调控血糖、血脂的药物,以解决糖尿病共病管理的综合需求。西格列他钠的上市,正好弥补了这一临床空白。
根据世界卫生组织(WHO)发布的《2024年全球肝炎报告》,2022年全球约有2.54亿人感染乙肝。其中,中国约有1600万人患有乙肝病毒,乙肝病毒患者是我国乙肝病毒流行病学调查的最新数据。
CS12088以其全新的作用机制,在现有治疗方案的基础上,有望为乙型肝炎的功能性治愈提供新的治疗选择,为慢性乙肝患者带来新的希望。
问:NASH临床3期预计开展时间,如何看待后续NASH药物竞争格局?
答:公司已经确定了三期NASH临床试验方案,并计划与CDE进行沟通。从NASH的发病机制来看,虽然减重可以降低NASH的负担,但其核心问题在于代谢稳态的破坏。因此,针对病因的治疗需要通过调控糖、脂蛋白和能量代谢来实现,西格列他钠正是通过这种机制发挥作用。PPAR全激动剂这一药理作用机理被认为会带来更优的治疗效果。西格列他钠的二期临床试验数据已投递了美国肝病年会,这项为期18周的研究采用了与现有评价方法一致的主要和次要疗效指标(除肝穿外)。尽管与已批准的某些药物的三期临床试验相比,西格列他钠的二期临床试验并未进行肝活检。但18周的治疗结果显示,其效果与其他药物长达54周甚至更长时间的治疗效果相近。PPAR有三个亚型,它们在功能上存在差异。NASH是一种异质性疾病,涉及炎症、纤维化等不同发病机理,其复杂性要求综合治疗。PPAR的三个亚型都能促进代谢调控,改善脂肪蓄积,其中单激动剂对肝脏脂肪蓄积的改善已有临床证据。此外,PPAR激动剂在炎症抑制和肝星状细胞纤维化过程中也显示出作用,使其成为理想的NASH治疗药物。在非侵入性指标方面,PPAR激动剂、FGF21激动剂和GLP-1/GIP双激动剂的比较显示,GLP-1在代谢方面可能具有优势,但在纤维化方面的表现不太突出。目前看来,这些药物的效果相当,但从长远来看,PPAR激动剂的作用机制可能具有更大的优势。此外,不同作用机制的药物也可以联合使用,例如利用GLP-1类药物实现代谢控制,未来NASH的治疗可能也会像其他慢性疾病一样,通过不同机制的药物联合使用来提高疗效。
西奥罗尼正在开展的 6个临床试验项目:2个III期,4个II期!
1、一线治疗广泛期小细胞肺癌III期临床试验:2024年11月1日,微芯生物宣布其自主研发的原创新药西奥罗尼联合PD - (L)1单抗及化疗一线治疗广泛期小细胞肺癌III期临床试验申请获得批准。西奥罗尼具有多通路的药理机制,能与免疫治疗和化疗产生协同效应,该新方案有望进一步改善广泛期小细胞肺癌患者长期生存状况,展现出巨大的临床治疗潜力。
2、联合化疗治疗巢癌的III期临床试验:截至2025年2月10日,该试验正在积极入组。
3、单药或联合治疗三阴性乳腺癌II期临床试验:处于推进中,该试验旨在探索西奥罗尼在三阴性乳腺癌治疗中的疗效和安全性。
4、单药或联合治疗软组织肉瘤II期临床试验:截至2025年2月10日,该试验已全部完成入组。
5、单药或联合治疗一线癌II期临床试验:截至2025年2月10日,该试验正在积极入组。
6、单药治疗小细胞肺癌/实体瘤的Ib/II期临床试验(美国):该海外临床试验进展顺利,截至2025年2月10日,已完成65mg剂量组爬坡,尚未出现剂量限制性毒性(DLT),美国FDA 于2025 年 3 月同意更高剂量探索美国人群后续用药剂量。
微芯生物国际合作伙伴HUYABIO(沪亚生物国际)在全球17个国家开展的西达本胺联合纳武利尤单抗一线治疗晚期黑色素瘤的三期临床试验已完成入组。——2026年Q2正式上市。
微芯生物:西奥罗尼联合治疗巢癌III 期临床达成首例患者入组
2021-12-21 09:59
来源:微芯生物投资者关系微信公众号
2021年12月20日,深圳微芯生物科技股份有限公司(以下简称“微芯生物”,股票代码:688321.SH)宣布西奥罗尼联合紫杉醇周疗治疗铂难治或铂耐药复发巢癌患者的随机、双盲、对照、多中心III期临床试验,完成首例入组。
本研究由复旦大学附属肿瘤医院(组长单位)吴小华教授牵头,主要评价西奥罗尼联合紫杉醇周疗对比紫杉醇周疗在铂难治或铂耐药复发巢癌患者中的疗效,全国约50家中心计划入组共376例受试者。本研究由组长单位于2021年11月17日成功完成首家启动,安徽济民肿瘤医院于2021年12月09日完成首例受试者ICF(知情同意书)签署,并于2021年12月20日完成了首例入组。
铂难治/耐药复发患者预后差,生存期短,临床治疗十分棘手。虽然二线非铂化疗的用药选择多,但仅有约20%的ORR和约4个月中位 PFS 的疗效获益,因此,为铂难治/耐药复发巢癌患者提供更有效、可及的新机制药物治疗选择,改善患者生存期和生活质量,已成为亟待解决的临床需求。
微芯生物原创新药西奥罗尼于2013 年 8 月获得临床试验批件,目前已开展包括巢癌、小细胞肺癌、肝癌等多种瘤肿的单药和联合用药的临床试验。在巢癌患者中,Ib 期的 CAR102 试验结果显示出西奥罗尼单药在复发难治巢癌中具有初步疗效,与其他抗血管生成药物(贝伐珠单抗、索拉非尼、帕唑帕尼)单药以及化疗单药水平大致类似;
II 期的 CAR201 试验初步分析结果显示,“依托泊苷 西奥罗尼 ”和“紫杉醇 西奥罗尼”治疗铂难治/耐药复发巢癌的 ORR 约为依托泊苷或紫杉醇单药 ORR 的两倍,提示西奥罗尼联合紫杉醇周疗在铂难治/耐药复发巢癌中具有协同抗肿瘤的作用。
2025年2月10日讯,微芯生物国际合作伙伴HUYABIO(沪亚生物国际)在全球17个国家开展的西达本胺联合纳武利尤单抗一线治疗晚期黑色素瘤的三期临床试验已完成入组。——治疗晚期黑色素瘤原创新药海外临床将在2026年Q2正式上市。
全球黑色素瘤治疗市场将以15.5%的年复合增长率(CAGR)高速增长,到2023年市值达到56.4亿美元。将主要发生在全球8个主要国家,包括美国、日本、澳大利亚、欧洲5国(英国、德国、法国、意大利、西班牙)。
拉2个板后在30元上方做平台等待均线系统呈完全多头排列形态,后再启动主升浪百元增发摊薄后将每股净资产值提升到10元上方。
本文作者可以追加内容哦 !

