来源:器械之家,未经授权不得转载,且24小时后方可转载。
近年来,学术专家的“行贿风波”频繁上演。
继月初耶鲁大学医学院博士揭露“美国五大顶级放射学期刊”作者财务信息披露的问题后,近日,行业媒体《KFF Health News》又报道了一起关于“FDA聘请的外部咨询小组成员中,有多名顾问与雅培公司存在财务往来”的事件,涉及金额高达65万美元(约合人民币470万元)。
文章指出,二月初时,外部咨询小组在投票会议上建议FDA批准雅培(Abbott)三尖瓣修复产品“Triclip G4”的上市申请,并表示TriClip设备的益处大于其风险。随后于本月初,FDA给予TriClip审批通过,使其成为美国地区首款获批用于修复渗漏的三尖瓣心脏瓣膜产品。
但事实上,该咨询小组的14名顾问中,有10名成员都曾收到过雅培公司的支付,或是进行过该公司资助的研究,而FDA和雅培均未对这些信息进行披露。这些信息在联邦数据库中轻易就能够查到。
虽然这些支付不代表机构、外部专家或设备制造商有出现不当行为,该数据库也并未显示任何支付与TriClip设备直接相关。但一些了解这一过程的人士,包括曾在FDA顾问委员会任职的人士表示,这些支付应该在2月初的会议上披露出来,无论是作为监管要求还是为了透明度,因为这些资金可能会对资讯小组成员的客观性产生质疑。
华盛顿大学医学院圣路易斯分校的神经学教授、前FDA顾问委员会成员Joel Perlmutter通过电子邮件表示:“由于偏见,他们应该或必须披露这些。”
01
14名成员高比率通过投票
据悉,FDA咨询小组(Advisory committees,简称Adcomm)是FDA负责牵头组建的,由来自学术界、医疗保健领域、行业和公众利益组织等领域的专家组成的临时机构。负责评估药品、医疗器械或食品的临床试验数据、效果和安全性,制定药品和设备的标准以及对FDA的政策和决策提供建议。
今年2月13日,FDA发起公开投票会议,就咨询小组在审查TriClip的临床数据(包括TRILUMINATE随机关键试验)后,进行安全性、有效性,以及收益/风险投票。该小组成员共14名成员,最终投票结果显示:
在产品安全性方面,14名咨询小组成员一致给予通过票;
在产品有效性方面,12名咨询小组成员给予通过票,另外两名成员持反对票;
在产品收益是否大于风险方面,13名咨询小组成员给予通过票,一名成员持反对票。
这表明14名成员中大部分都支持雅培Triclip G4的上市。

财务往来
在会议开始前,FDA官员宣布该资讯小组成员已经接受了潜在财务利益冲突的筛查,并符合政府要求。
但根据KFF健康新闻的发现,资讯小组的14名投票成员中,有10人与雅培公司存在财务往来,总金额约为65万美元。其中,有一位成员与Abbott公司有着近20万美元的支付关联,另一位成员有约10万美元的支付关联并进行过约5万美元的由Abbott支持的研究。此外,还有一位委员会成员从该公司获得了超过18万美元的研究支持。
这些支付信息来自于“Open Payments”数据库,该数据库记录了医生和其他医疗保健提供者与药品和医疗设备制造商之间的财务关系。
FDA通过审查程序确认委员会成员没有潜在的财务利益冲突,并强调了其披露和审查程序的完整性。然而,一些人认为FDA在这方面的做法过于“狭隘”,认为应该更加严格地排除可能影响客观性的利益冲突。
02
全球首个
三尖瓣经导管修复产品获批
资料显示,Triclip G4是第一款获得FDA批准经导管三尖瓣缘对缘修复产品,用于治疗心脏三尖瓣反流(也称为三尖瓣漏)问题。具体针对的是进行了最佳药物治疗,但三尖瓣反流仍然存在的患者。
该系统是基于基于公司畅销的二尖瓣反流产品“MitraClip”的设计构建的,旨在通过抓取心脏对侧较为棘手的瓣膜叶片并将其牢牢固定在一起,以达到修复心脏的三尖瓣,减少或消除心脏瓣膜反流的效果。
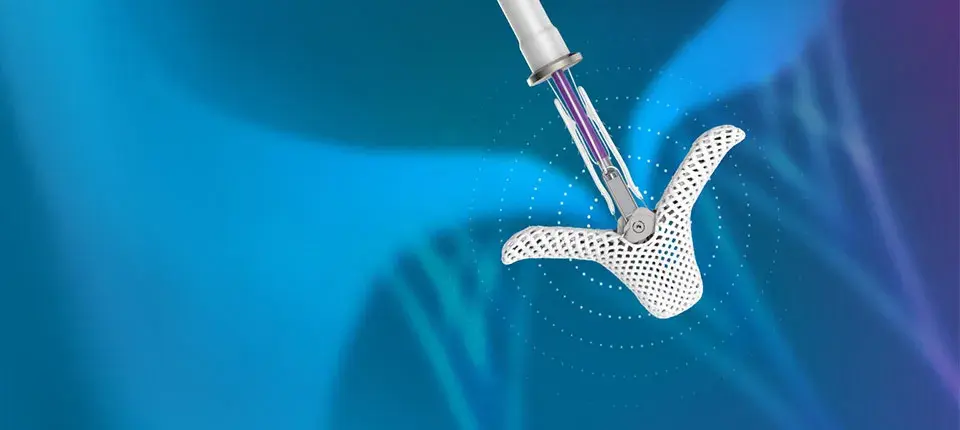
Triclip G4是Triclip系统的最新版本,于2021年4月在欧洲上市,是同类产品中首个获CE认证的系统。今年4月又获得FDA批准在美上市,成为首个通过审批的三尖瓣经导管修复产品。目前TriClip 已在 50 多个国家/地区获得批准,并治疗了 10,000 多名患者。
TriClip G4优势:
经导管三尖瓣修复,无需体外循环(不用心脏暂停);
允许实时定位和重新定位;
经股静脉入路;
可用于标准导管室或混合室
无需术前CT检查;
多种尺寸夹头,适用于不同类型患者;
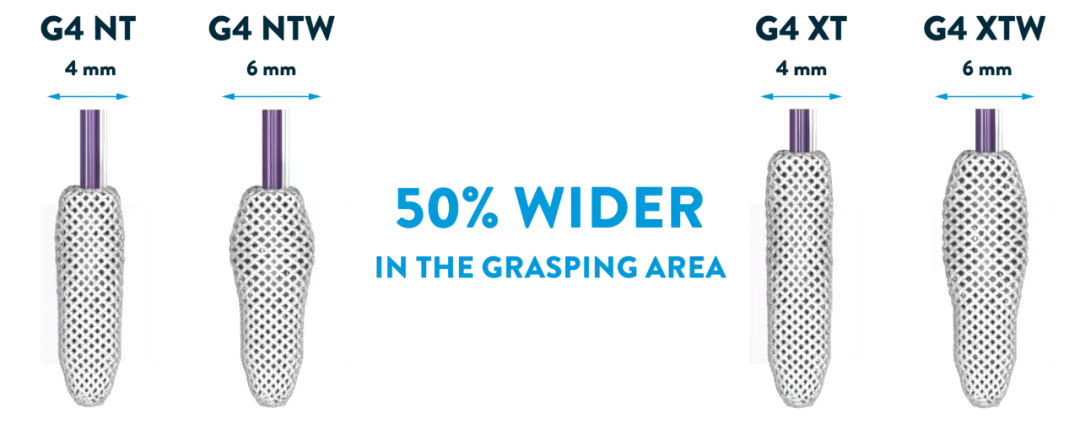
据悉,目前美国约有多达 160 万人患有临床意义上的三尖瓣反流,而在世界范围内,这一数字高达约 7000 万人。值得注意的是,在今年以前,都没有一款介入治疗产品能够获批在美上市。
直到今年2月,爱德华生命科学的EVOQUE获得FDA批准,成为首款经导管三尖瓣置换产品。而此次TriClip G4获批后,美国患者将拥有经导管置换和修复两种新型治疗方式。
那么Triclip与Evoque三尖瓣置换装置该如何选择呢?日前,雅培公司结构性心脏部门的高级医学总监Nadim Geloo在接受采访时是这样回答的:
“我们认为对于大多数患者来说,三尖瓣修复是更好的选择,这是基于很多历史的依据。如果回顾手术文献,在二尖瓣病人的手术中,那些在任何导管设备出现之前进行手术以替换或修复瓣膜的外科医生,绝大多数选择修复瓣膜,因为他们认为修复的结果对患者更好。
如果将这一观点转化到导管设备领域,我们的看法是一样的。在二尖瓣和三尖瓣上,我们认为修复对患者是更好的选择。这是一个较少侵入性的方法。你没有一个大的瓣膜,这有时可能需要更积极的早期抗凝治疗。
但我认为重要的是要知道,患者有这些选择,这才是赢家。”
03
医疗器械领域闹剧不断
近年来,医疗器械领域商业贿赂、学术造假的闹剧不断上演。
前不久,五家欧美顶级放射学术报刊作者财务来源“罗生门”事件涉及的资金高达1.866亿美元(约合人民币13.47亿元)。
据耶鲁大学医学院的Dheeman Futela博士披露,他分别调取了2021年发表在五家期刊上的美国作者的财务披露,包括原始研究和综述文章。并提取了过去三年内公开支付数据库(OPD)中与一般类别、研究和所有权支付类别相关的支付报告,对每位作者进行个别分析,以确定其披露是否与OPD的结果一致。
截取自研究报告主页
这五个行业顶刊分别为:《JACR》、《Radiology》、《AJR》、《JVIR》和《AJNR》。DheemanFutela博士团队从这些杂志刊出的643篇文章中选出了共4076个作者和3406个独立作者进行调研。结果显示:
有1388名作者在过去36个月内收到了行业付款,每个作者收到的平均金额为6,650美元(四分位数为355美元至87,725美元)。
而这1388名收到款项的作者中,只有61人(4.4%)披露了与该行业的所有财务关系,205人(14.8%)只披露了部分,剩余1,122人(81%)未报告任何财务关系。
未披露的付款总额为186,578,350美元,占付款总额的67.2%。据此推算,付款总额为2.77亿美元(约合人民币20亿元)。
此外,调研披露,这五家期刊中的美国作者支付金额最多的行业合作伙伴包括辉瑞(4200万美元)、GE医疗(1800万美元)、默沙东(1500万美元)、艾伯维AbbVie(1300万美元)和阿斯利康制药(1100万美元)。
但这其中,只有4.4%的美国期刊研究作者披露了与该行业的所有财务联系,近81%的作者未报告任何财务关系。
--
虽然这些支付不代表机构、外部专家或设备制造商有出现不当行为,该数据库也并未显示任何支付与TriClip设备直接相关。但无论是作为监管要求还是为了透明度,未能披露财务关系可能会被视为有失公正的做法,因为这些资金可能会对资讯小组成员的客观性产生质疑。
三尖瓣修复产品Triclip G4上市在即,这起罗生门事件会不会对该产品未来的销售有所影响?雅培又将如何面对此次行贿风波?器械之家将持续关注。
本文作者可以追加内容哦 !

