
8月22日,据CDE官网显示,$百济神州-U(SH688235)$1类新药BGB-43395片获批临床,拟用于单药治疗或与氟维司群、来曲唑或其他药物联合治疗晚期或转移性HR+/HER2-乳腺癌及其他实体瘤。
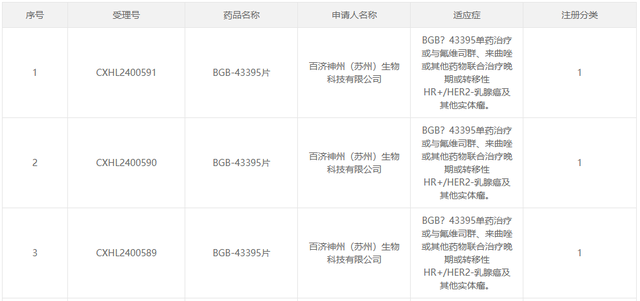
BGB-43395片是由百济神州研发的靶向CDK4的新分子实体,是该公司乳腺癌和妇科癌症管线中的在研产品之一。从作用机理来看,CD4 抑制剂有望实现比 CDK4/6 抑制剂更好的有效性和更低的毒性。2024年2月12日,百济已在国内启动 BGB-43395 的Ⅰ期临床。此前,该药已于2023 年 11 月在法国、澳大利亚、美国启动Ⅰ期临床。
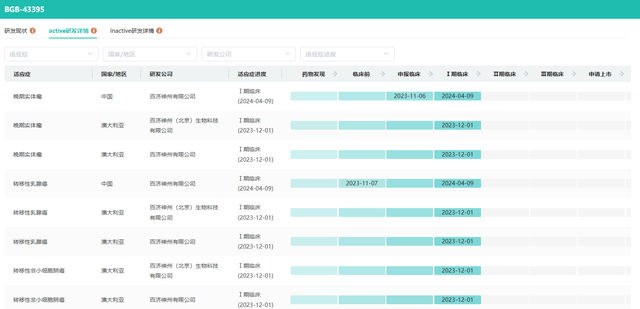
2024年1月首次获批临床,根据中国药物临床试验信息登记与公示平台信息,一项评估BGB-43395单药或与其他药物联合在晚期或转移性 HR+/HER2-乳腺癌及其他实体瘤中国患者中的安全性、耐受性、药代动力学、药效学和初步抗肿瘤活性的1a/1b期研究正在进行中。
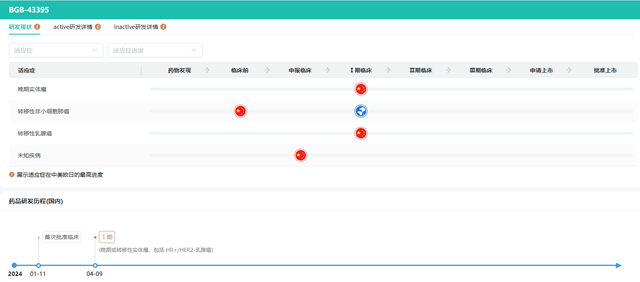
$百济神州(HK|06160)$在日前发布的2024年半年报中披露,BGB-43395单药治疗组以及与氟维司群和来曲唑的联合治疗组在预期有效剂量范围内进行剂量递增,未观察到剂量限制性毒性。至今已入组超过60例患者,有望在2024年第四季度公布1期试验的首次数据读出结果。
据药融云数据库显示,全球范围内仅有三款 CDK4 单靶点抑制剂进入临床,分别为辉瑞/Arvinas 的 Atirmociclib(国内外均处于Ⅲ期)、恒瑞的 HRS-6209(国内 I/II 期)、百济神州的 BGB-43395(国内外均处于Ⅰ期)。
参考来源:
[1] CDE官网
[2] 药融云数据库
<END>
本文作者可以追加内容哦 !

