自身免疫性疾病治疗领域正经历快速发展,靶向免疫抑制药物作为创新治疗手段,受到广泛关注。摩熵咨询近期发布的《自免药物(JAK抑制剂篇)市场研究专题报告》以其深入的行业洞察系统剖析了JAK抑制剂的作用机制、市场竞争格局及靶向药物未来趋势。本文将基于报告核心内容,揭示靶向免疫药物市场的四大关键趋势。
1. 医保政策为自身免疫靶向新药放量提供机遇
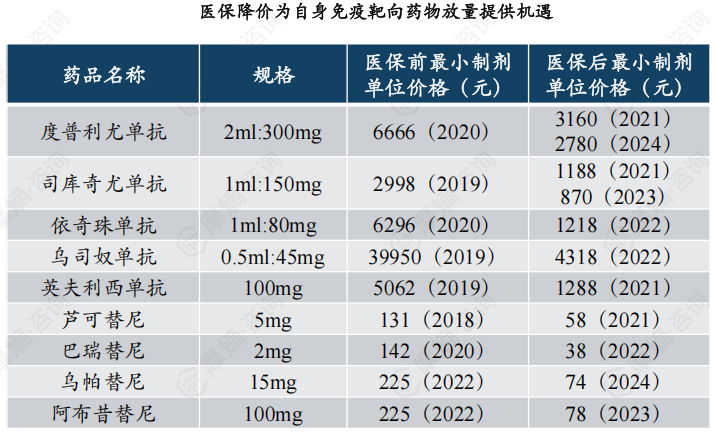
价格是带动自免药物放量的重要重要因素。各个产品纳入医保后放量迅速提升,而未进入医保的药物难以放量,如银屑病的司库奇尤单抗和古塞奇尤单抗形成鲜明对比。同一适应症低价药更受欢迎,如银屑病治疗上诺华的的司库奇尤单抗上市价格仅为3000元/支,相比疗效类似的依奇珠单抗的6300元/支销售更好。
我国自免疾病患者人数众多,但大部分在基层,以银屑病为例,《2022银屑病基层治疗指南》指出我国700万银屑病患者75%首诊在基层,而基层患者难以负担高昂的药品价格,因此医保为自身免疫靶向药物放量提供了机遇。
2. 新药物:全球Ⅲ期及以上JAK抑制剂有17款,多为二代选择性JAK抑制剂
JAK抑制剂凭借口服便捷性与广谱抗炎作用,成为自免领域最热门的小分子靶向药物。2023年中国JAK抑制剂市场规模达21.5亿元,一代产品(托法替布、巴瑞替尼等)占比85.4%。然而,一代药物因泛JAK抑制导致心血管事件等安全性问题,限制其长期应用。
二代选择性JAK抑制剂通过精准抑制亚型(如JAK1、TYK2)显著降低风险,成为研发焦点。据摩熵医药数据库统计,截至2024年12月,全球Ⅲ期及以上在研JAK抑制剂达17款,且多为二代选择性JAK抑制剂。这些新药物在提高疗效和减少副作用方面展现出巨大潜力。
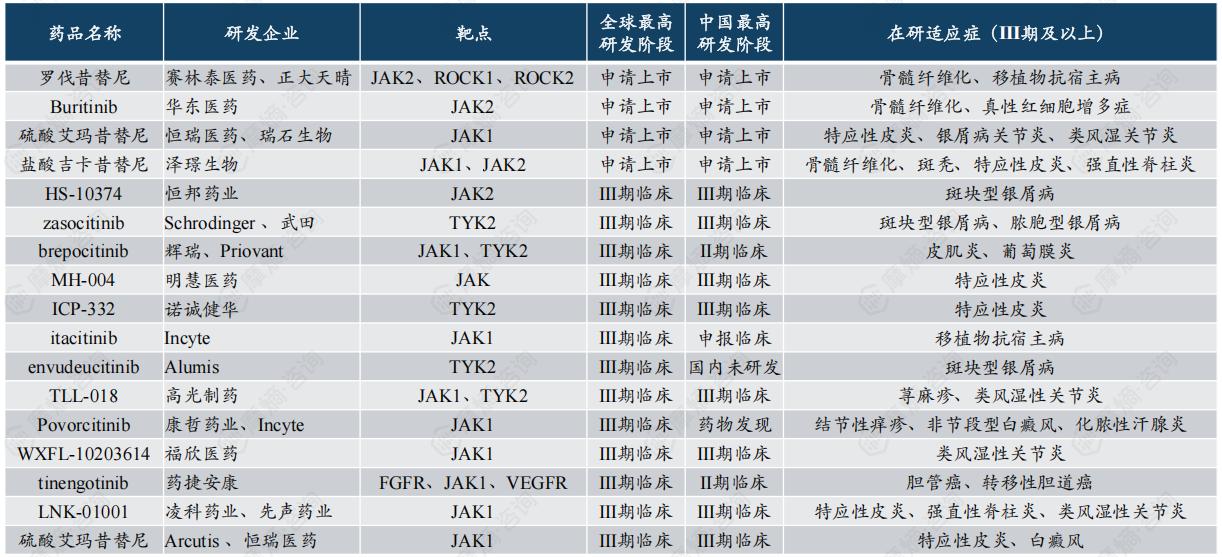 数据来源:摩熵医药数据库
数据来源:摩熵医药数据库3. 新靶点:TSLP成药性得到验证,正大天晴TQC-2731已进入Ⅲ期临床
胸腺基质淋巴生成素(TSLP)最初是从小鼠胸腺基质细胞系中分离出来,是一种与IL-7互为远距离旁系同源的,归属于短链螺旋束Ⅰ型IL-2家族的多效细胞因子。TSLP与多种过敏性疾病,如特应性皮炎、支气管哮喘、嗜酸性粒细胞食管炎有关。Nature Reviews等文献数据显示,TSLP还与慢性炎症性疾病(如慢性阻塞性肺病和乳糜泻)和自身免疫性疾病(如牛皮癣、类风湿性关节炎)有关。
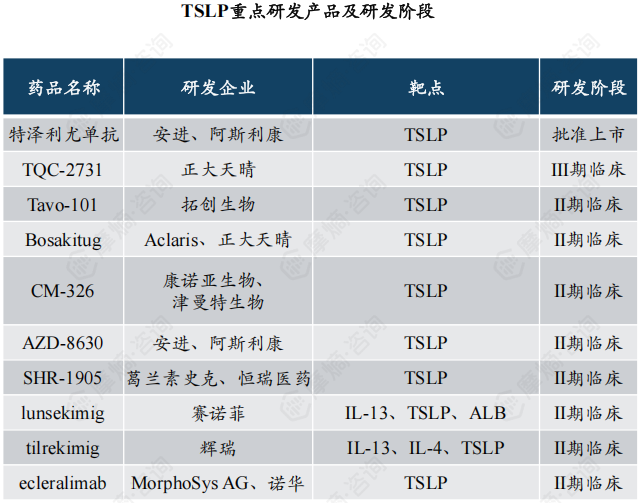
TSLP靶点目前仅有 $安进(NASDAQ|AMGN)$ 安进和 $阿斯利康(US ADR)(NASDAQ|AZN)$ 阿斯利康的特泽利尤单抗在欧盟和日本获批上市,用于治疗重度哮喘,其突破了治疗嗜酸性哮喘的局限,在广泛严重哮喘患者治疗中显示出突出的临床疗效。
本土TSLP药物中,正大天晴的TQC-2731哮喘适应症已经进入Ⅲ期临床,慢性阻塞性肺病、鼻窦炎、鼻息肉等适应症也进入Ⅱ期临床。
4. 新剂型:多款口服靶向药物正在路上
近年来,自身免疫抑制性疾病的靶向治疗领域取得了显著进展,生物制剂的应用尤为突出,成功帮助众多患者实现了疾病的完全或近乎完全缓解。然而生物制剂(注射)仍未能全面满足所有患者的需求,诸如注射恐惧、存储条件限制及携带不便等问题,对部分患者构成了不小的挑战。鉴于此,乌帕替尼片、氘可来昔替尼片等新型口服小分子靶向药物应运而生,为患者提供了新的治疗选择。此外,还有数款口服靶向药物正处于临床研发阶段。
TAK-279:是一种口服变构TYK2抑制剂,由Nimbus Ther-apeutics公司开发,于2022年被武田收购。Ⅱ期临床实验显示:在第12周时,TAK-279 15 mg组和30 mg组分别有53.3%和54.2%的患者达到ACR 20,而安慰剂组仅为29.2%。此外,TAK-279 30 mg组和15 mg组的银屑病面积和严重程度指数75缓解率也显著高于安慰剂组,分别为45.7%和28.3%,安慰剂组为15.4%,具有潜在临床应用价值。
Orismilast:是一种新型口服磷酸二酯酶-4(PDE4)抑制剂,对PDE4B和PDE4D亚型具有更强的选择性。2023年,Union Therapeutics公司报告了orismilast的Ⅱb期临床试验结果。该研究中未发现新的安全信号,证实了PDE4类药物具有良好的安全性。
Orismilast全球临床试验信息查询列表(部分)
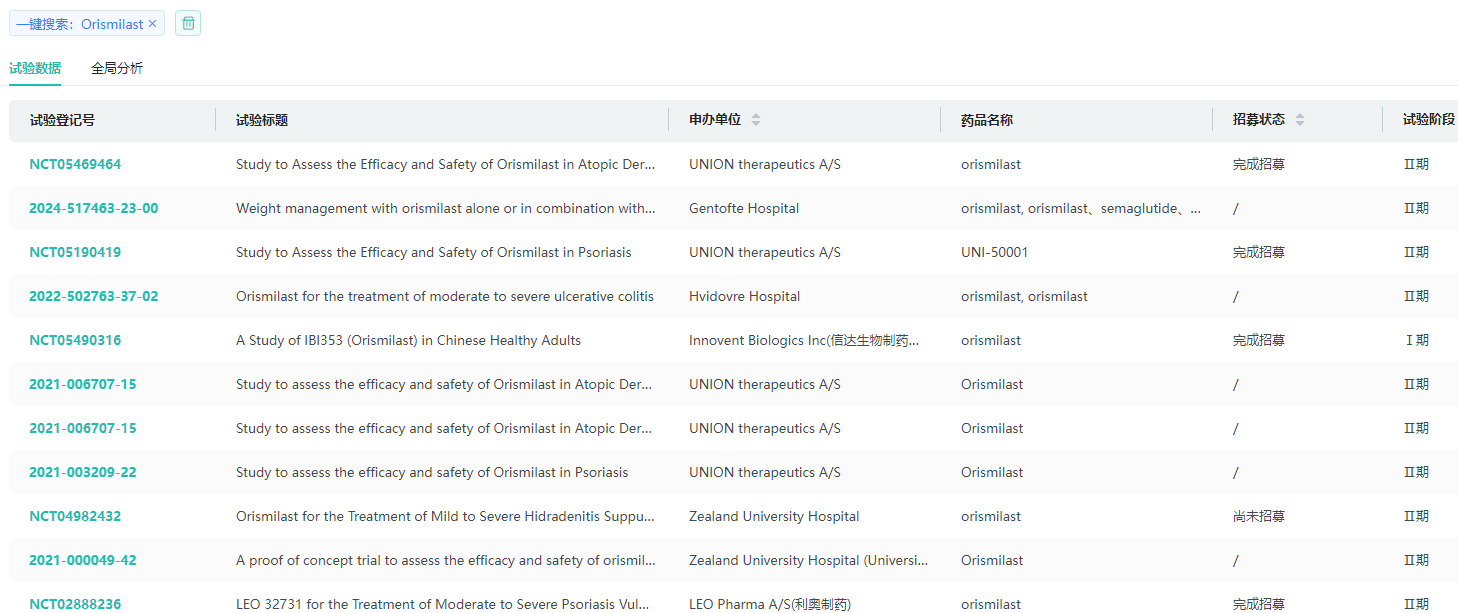 图片来源:摩熵医药全球临床试验数据库
图片来源:摩熵医药全球临床试验数据库SAR441566:是赛诺菲目前正在研究的一款口服TNF抑制剂,通过扭曲可溶性TNF三聚体的构象,阻断TNF与TNFR1的相互作用,但该产品不会影响与细胞膜结合的TNF的信号传导,可以更好降低感染风险并提高疗效。根据国家药监局药品审评中心官网显示, $赛诺菲(NASDAQ|SNY)$ 赛诺菲SAR441566的Ⅱ期临床试验申请获批准,用于治疗中重度斑块型银屑病,以及中重度类风湿性关节炎。
5. 新治疗方式:CAR-T细胞疗法不断发展,研究领域逐渐扩展至自免疾病
近年来,CAR-T细胞疗法在自身免疫性疾病治疗中展现了良好的应用前景,尤其是以CD19为靶点的疗法取得了显著进展。CD19作为B细胞特异性标志物,贯穿前B细胞至成熟B细胞的分化过程,成为B细胞耗竭疗法的关键靶点。为进一步提升疗效,部分研究探索了CD19/BCMA的双靶点策略,也展现出良好的应用潜力。
2021年MOUGIAKAKOS等首次使用CD19 CAR-T细胞疗法治疗1例20岁难治性SLE患者。该患者存在多系统受累,表现为活动性狼疮肾炎、皮疹、关节炎、心包炎和胸膜炎,既往大剂量激素、多种免疫抑制剂及生物制剂治疗无效。研究者在仅保留小剂量激素的情况下,予患者清淋治疗(氟达拉滨+环磷酰胺)后回输自体来源CAR-T细胞。该患者在接受治疗第44天实现临床及血清学的完全缓解,SLE疾病活动度(SLE disease activity index,SLEDAI)评分从16分降为0分。随访6个月内,患者逐渐停用激素,且无疾病复发迹象。这一成功的初步尝试为后续的临床研究奠定了基础。
全球CAR-T细胞疗法TOP10适应症分布
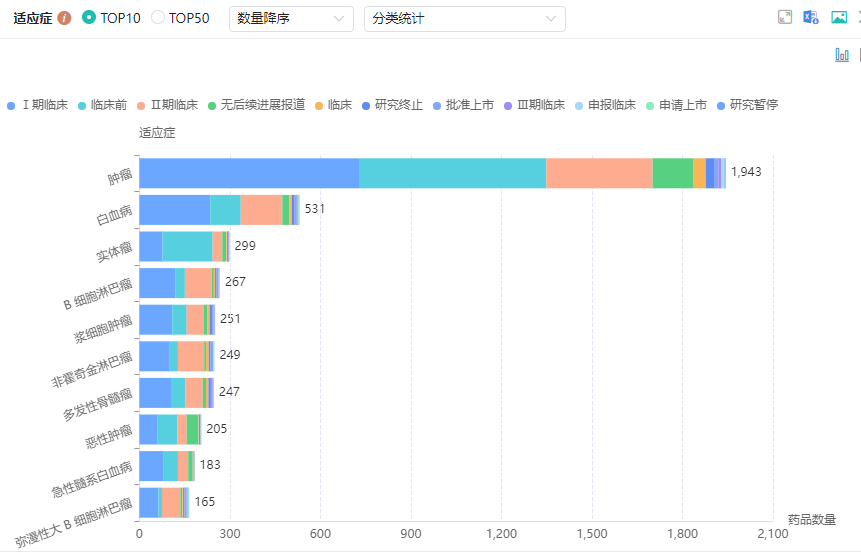 图片来源:摩熵医药全球药物研发数据库
图片来源:摩熵医药全球药物研发数据库2022年该团队进一步纳入5例中位年龄为22岁的难治性SLE患者,在CAR-T细胞回输后第3个月,所有患者的补体及抗双链DNA抗体滴度恢复正常,4例患者SLEDAI评分降至0分,1例患者为2分,在长达17个月的随访中均未出现复发,实现了无药缓解,治疗过程中仅观察到1级CRS事件。为进一步评估其远期疗效及安全性,2024年该团队报道了15例严重自身免疫性疾病患者接受CD19 CAR-T细胞治疗的研究结果,其中包括8例SLE。该研究显示,经过CAR-T细胞治疗后,所有患者在6个月后达到SLE低疾病活动状态,SLEDAI评分为0分,随访至29个月时仍保持无药缓解状态;在安全性方面,6个月的随访过程中仅观察到轻度的上呼吸道感染症状。上述临床研究证实了CAR-T细胞疗法在成人SLE治疗中的有效性、持久性及较好的耐受性。
尽管CAR-T细胞疗法在部分难治性患者中显示出长期无药物缓解的疗效,但仍在生产难度、安全性、持久性等方面存在挑战。未来研究方向将集中于提高治疗的个性化,以期更好地管理疾病复发并减少不良反应。
结语:
靶向免疫抑制药物市场在医保政策支持、新药研发、新靶点探索、新剂型涌现及新治疗方式拓展等多维度驱动下,正迎来前所未有的发展机遇。对于医药企业来说,紧跟市场趋势,加大研发投入,推出更多高效、安全、便捷的治疗药物,将是抢占市场份额、实现可持续发展的关键。
本文作者可以追加内容哦 !


